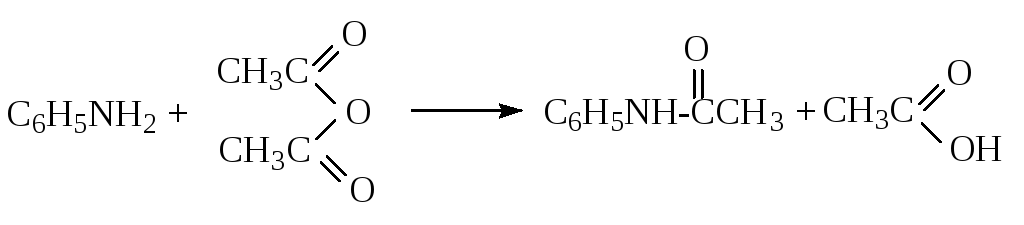
Уксусный ангидрид, химические свойства, получение, (Ch4CO)2O
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Ангидриды карбоновых кислот
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Ангидриды кислот – определение, структура, свойства и применение
Ангидрид представляет собой химический продукт, образующийся при удалении молекулы воды из кислоты. Итак, что такое ангидрид? Атом кислорода соединяет две ацильные группы, которые определяют функциональную группу. Ангидрид означает «без воды». Вы можете описать его как химическое вещество, созданное при удалении воды из другого химического вещества. Ангидрид и вода могут объединяться, образуя основание или кислоту. Смешанный ангидрид образуется из двух разных карбоновых кислот и определяется как имеющий разные группы R в общей структуре, изображенной ниже. Давайте теперь узнаем об ангидридах кислот.
Оксиды неметаллов, реагирующие с водой с образованием кислых растворов, называются ангидридами кислот. Это молекула, которая может образовывать кислые растворы в воде. Это функциональная группа в органической химии, состоящая из двух ацильных групп, соединенных атомом кислорода.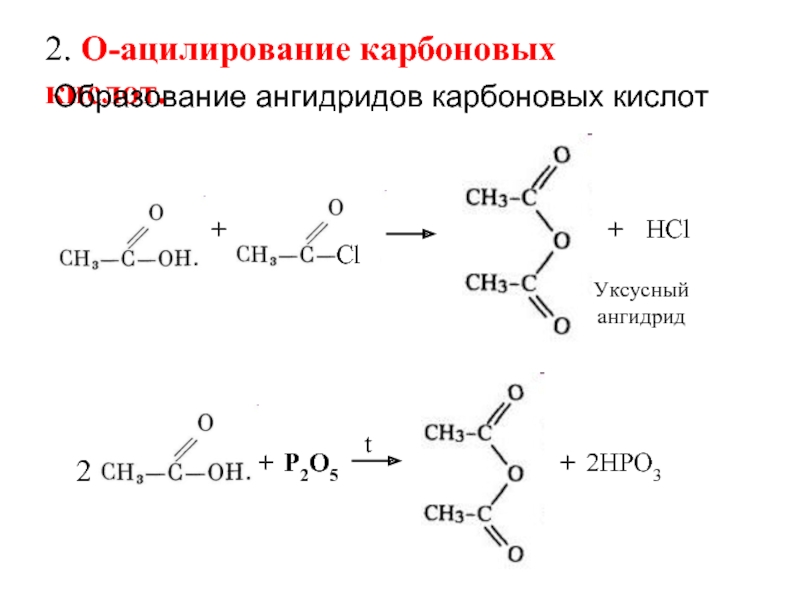 Неметаллы, которые могут реагировать с водой, строго называются ангидридами, а неметаллы, которые не могут реагировать с водой, не считаются ангидридами.
Неметаллы, которые могут реагировать с водой, строго называются ангидридами, а неметаллы, которые не могут реагировать с водой, не считаются ангидридами.
Согласно органической химии, ангидриды органических кислот имеют функциональную группу R(CO)O(CO)R’. Ангидрид органической кислоты часто образуется при удалении одного эквивалента воды из двух эквивалентов органической кислоты в реакции дегидратации.
Структура общего ангидрида кислотыЗдесь R и R‘ — любые алкановые группы.
Формула уксусного ангидридаЭто молекула уксусного ангидрида. R и R’ сверху при замене на группы метана (Ch4) дают нам формулу уксусного ангидрида. Эта молекула является одним из основных примеров ангидридов кислот.
Синтез ангидрида кислоты Ангидриды кислоты представляют собой вещества с двумя ацильными группами (R-C=O), присоединенными к одному и тому же атому кислорода. Когда карбоновая кислота соединяется с хлорангидридом, эта реакция часто приводит к образованию ангидрида в присутствии основания.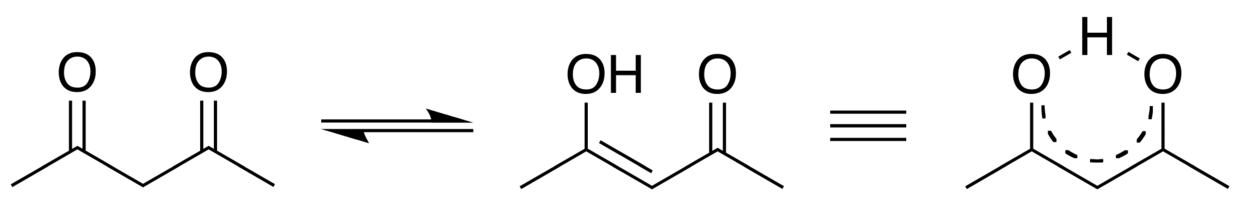 Две карбоновые кислоты нагревают при высокой температуре 800°C или выше для получения ангидрида органической кислоты. На этом этапе молекулы воды удаляются из реакции. Карбоновые кислоты можно использовать для реакции и получения P 2 О 5 .
Две карбоновые кислоты нагревают при высокой температуре 800°C или выше для получения ангидрида органической кислоты. На этом этапе молекулы воды удаляются из реакции. Карбоновые кислоты можно использовать для реакции и получения P 2 О 5 .
Метод дегидратации показывает химическую реакцию синтеза ангидрида кислоты.
Здесь R – любая алкановая группа.
Физические свойства ангидридов кислотРассмотрим типичный пример физических свойств уксусного ангидрида.
Внешний вид – Ангидрид уксусной кислоты, также известный как ангидрид уксусной кислоты, представляет собой бесцветную жидкость с характерным запахом уксуса (уксусной кислоты). Запах возникает, когда уксусный ангидрид соединяется с водяным паром в воздухе и влагой в носу, чтобы преобразовать уксусную кислоту. Эта реакция с водой подробно описана на другой странице.
Растворимость в воде – Уксусный ангидрид соединяется с водой с образованием уксусной кислоты, поэтому нельзя сказать, что он растворим в воде. Водных растворов уксусного ангидрида не существует.
Водных растворов уксусного ангидрида не существует.
Температура кипения – абс. этанол кипит при 140 °С. Это довольно крупные полярные молекулы с междипольной и ван-дер-ваальсовой дисперсионными силами. Однако он не образует водородных связей. Это указывает на более низкую температуру кипения, чем у карбоновой кислоты сопоставимого размера. Например, пентановая кислота является ближайшей кислотой по размеру и кипит при 186 °C.
Реакционная способность ангидридов кислот- Сравнение ангидридов кислот и хлорангидридов (хлорангидридов). Возможно, вы недавно завершили исследование ацилхлоридов и одновременно работаете над ангидридами кислот в качестве ацилхлоридов.
- Вместо того, чтобы пытаться узнать все об ангидридах кислот с нуля, гораздо проще думать о них как о некоем модифицированном хлорангидриде. Именно такой позиции я хочу придерживаться в этом разделе.
- Более внимательное изучение цветовой кодировки на рисунке помогает сравнить структуры ангидридов и хлорангидридов кислот.
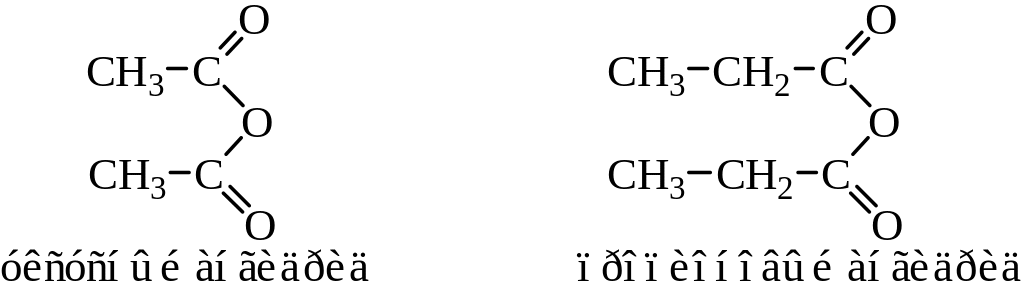
Нижняя красная группа никогда не разрушается в реакции этанового ангидрида. Подобно атому хлора в ацилхлориде, он во многих отношениях выглядит как один атом. Ацилхлориды часто реагируют, заменяя хлор другим веществом. Если взять в качестве примера этанолилхлорид, первая реакция будет следующей:
Образуется газообразный хлористый водород, который впоследствии может реагировать с другими компонентами комбинации. Ангидрид замедляет реакцию, но главное отличие состоит в том, что вместо хлороводорода в качестве побочного продукта образуется уксусная кислота.
Он, как и хлористый водород, может продолжать взаимодействовать с другими элементами окружающей среды. В ацилхлоридных и ангидридных реакциях участвуют вода, спирты и фенолы, аммиак и амины и другие вещества. В каждой из этих конкретных ситуаций существует сильно электроотрицательный элемент с активной неподеленной парой (кислород или азот).
Химические свойства ангидрида кислоты Путем изменения группы -OCOR ангидрид кислоты подвергается реакции нуклеофильного замещения. Более высокая электроотрицательность атома Cl по сравнению с группой -OCOR делает его менее реакционноспособным, чем хлорангидрид.
Более высокая электроотрицательность атома Cl по сравнению с группой -OCOR делает его менее реакционноспособным, чем хлорангидрид.
Здесь R,R| и R 2 – любые алкановые группы.
Образование угольной кислотыУглекислота образуется при взаимодействии диоксида углерода и воды. Химическая формула угольной кислоты приведена ниже.
CO 2 (g) + H 2 O → H 2 CO 3 (AQ)
3 (AQ) 3 (AQ) 3 (AQ). кислая угольная кислота или H 2 CO 3 . Кислотные дожди являются результатом этого процесса. Важен для изменения pH ручьев, рек и океанов. Приведенное выше уравнение показывает, что увеличение количества углекислого газа в воздухе приводит к образованию углекислого газа, опасного для жизни. Основная проблема, над которой мы сейчас работаем, заключается в следующем. Образование серной кислоты:
Основная проблема, над которой мы сейчас работаем, заключается в следующем. Образование серной кислоты: Триоксид серы и вода образуют серную кислоту. Это объяснит химически. Затем при взаимодействии газообразного триоксида серы и воды образуется серная кислота.
SO 3 (G) + H 2 O → H 2 SO 4 (AQ) 9003 4 (AQ)
4 (AQ) 4 (AQ). воздух. Кислотный дождь образуется, когда он реагирует с водой во время дождя. Они очень негативно влияют на экосистему. Узнайте больше об ангидриде уксусной кислоты- Ангидрид уксусной кислоты является одним из простейших примеров ангидридов кислот. Химически формула уксусного ангидрида, также называемого уксусным ангидридом, такова (CH 3 CO) 2 O.
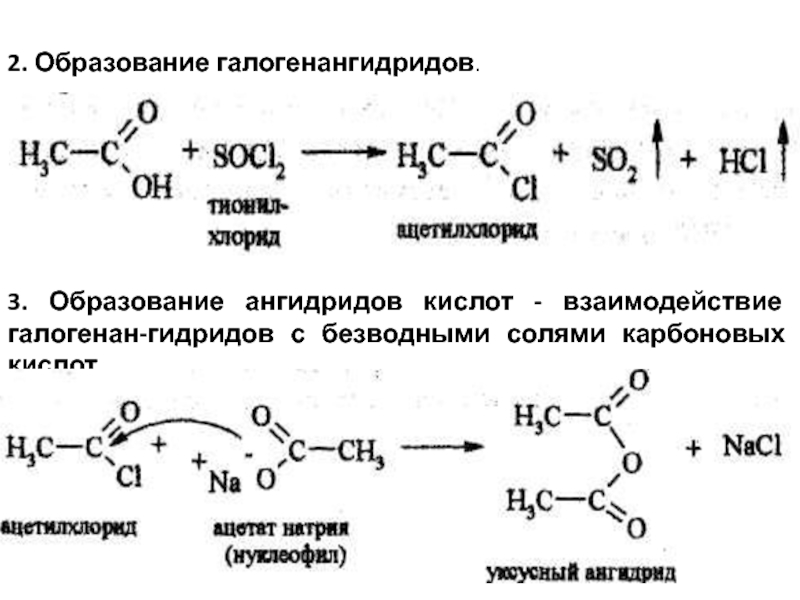 Часто называемый Ac 2 O, это наиболее легко отделяемый ангидрид карбоновых кислот. Это обычный реагент в синтезе органических соединений. Это белая жидкость, которая реагирует с влагой воздуха с образованием уксусной кислоты и имеет сильный запах уксусной кислоты.
Часто называемый Ac 2 O, это наиболее легко отделяемый ангидрид карбоновых кислот. Это обычный реагент в синтезе органических соединений. Это белая жидкость, которая реагирует с влагой воздуха с образованием уксусной кислоты и имеет сильный запах уксусной кислоты. - Уксусная кислота может быть обезвожена при 800 °C с получением уксусного ангидрида. С другой стороны, уксусный ангидрид и соль образуются, когда хлорангидрид реагирует с солью уксусной кислоты, такой как ацетат натрия. Формула уксусного ангидрида также может быть проиллюстрирована как:
- Название IUPAC: ангидрид уксусной кислоты
- Классификация: Ангидрид органических кислот
- Растворим в: воде, бензоле
- Формула: C 4 H 6 O 3
- Плотность уксусного ангидрида: 1,08 г/см³
- Уксусный ангидрид Молярная масса: 102,09 г/моль
- Температура кипения: 139,5 °C
Плотность уксусного ангидрида 1,072 г/мл. Вода не может поглощать уксусный ангидрид. Плотность уксусного ангидрида немного выше, чем у воды, с плотностью 0,9.99 г/мл. Значение pKa уксусного ангидрида, которое меньше нуля и имеет достаточно высокую кислотность, составляет -6,9. Значения pKa ниже нуля встречаются в сильных кислотах. Кислота тем сильнее и тем ниже значение pKa. Установлено, что молярная масса уксусного ангидрида составляет 102,09 г/моль. Молярная масса воды составляет примерно 18,015 г/моль. Следовательно, молярная масса уксусного ангидрида почти в пять раз больше массы воды.
Вода не может поглощать уксусный ангидрид. Плотность уксусного ангидрида немного выше, чем у воды, с плотностью 0,9.99 г/мл. Значение pKa уксусного ангидрида, которое меньше нуля и имеет достаточно высокую кислотность, составляет -6,9. Значения pKa ниже нуля встречаются в сильных кислотах. Кислота тем сильнее и тем ниже значение pKa. Установлено, что молярная масса уксусного ангидрида составляет 102,09 г/моль. Молярная масса воды составляет примерно 18,015 г/моль. Следовательно, молярная масса уксусного ангидрида почти в пять раз больше массы воды.
Как и большинство ангидридов кислот, ангидрид уксусной кислоты представляет собой податливую молекулу неплоской формы. По сравнению с диполь-дипольным отталкиванием двух карбонильных атомов кислорода соединение пи-системы через центральный кислород обеспечивает относительно скромную резонансную стабильность. Существует относительно мало энергетических барьеров для сопряжения вращения между идеальными конформациями без плоских тел.
- Уксусный ангидрид, как предполагает органическая химия, в основном используется для ацетилирования, ведущего к коммерчески важным продуктам.
- Его основное применение — преобразование целлюлозы в ацетат целлюлозы. Ацетат целлюлозы используется для производства сигаретных фильтров и является строительным блоком фотопленки и других материалов с покрытием.
- Он используется в этом процессе, аналогично тому, как салициловая кислота превращается в аспирин, также называемый ацетилсалициловой кислотой.
- Он также используется в качестве модификатора активности путем автоклавной пропитки и последующего ацетилирования для получения прочной и долговечной древесины.
- Ангидрид уксусной кислоты является основным химическим веществом, используемым в качестве ацетилирующего агента при изготовлении запрещенных наркотиков героина и метаквалона.
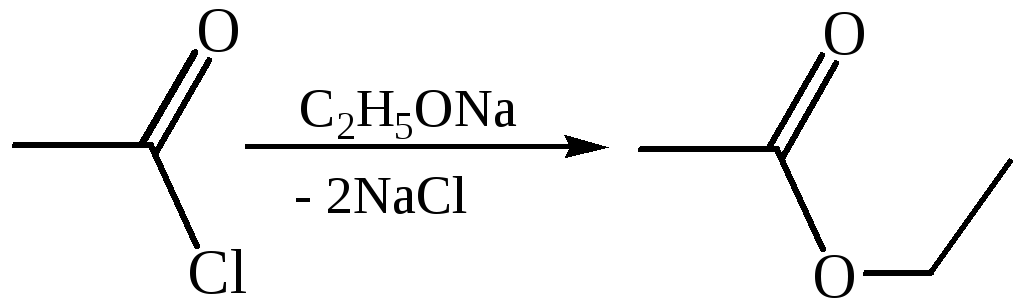
- Ангидриды кислот, являющиеся органическими химическими веществами, известны как ангидриды органических кислот. Вещества, у которых две ацильные группы присоединены к одному и тому же атому кислорода, называются ангидридами кислот. Ангидриды карбоновых кислот формулы (RC(O)) 2 O представляют собой типичный тип ангидридов органических кислот, в которых исходной кислотой является карбоновая кислота. Эта форма симметричного ангидрида обозначается заменой слова кислота в названии исходной карбоновой кислоты словом безводный. Поэтому (Ch4CO)2O также называют уксусным ангидридом.
- Известны смешанные (или несимметричные) ангидриды кислот, в которых происходит реакция между двумя разными карбоновыми кислотами, такими как муравьиный ангидрид уксусной кислоты. Другие формы органических кислот, такие как сульфоновые или фосфоновые кислоты, также могут служить источником одной или обеих ацильных групп в ангидриде.
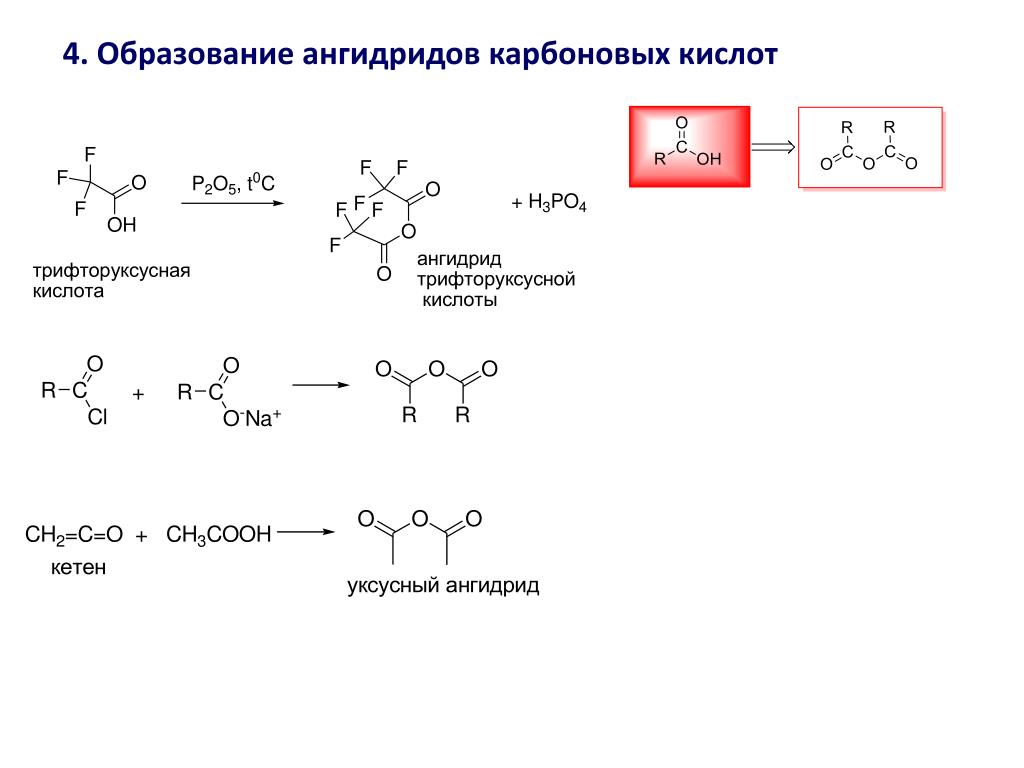 Неорганические кислоты, такие как фосфорная кислота, служат одним из источников ацильных групп в ангидридах.
Неорганические кислоты, такие как фосфорная кислота, служат одним из источников ацильных групп в ангидридах.
- Ангидриды кислот широко используются в органической химии.
- С их помощью производится множество продуктов: фармацевтика, промышленная химия, взрывчатые вещества, парфюмерия.
- Сложные эфиры получают путем ацетилирования спиртов.
- Синтез аспирина (ацетилсалициловой кислоты).
- Героин производится путем деацетилирования морфина.
уксусный ангидрид
| ID | КАС | Имя | Синонимы | Молекулярная формула | Категория |
|---|---|---|---|---|---|
| 1 | Acetic Anhydrides | Acetic Anhydride s | |||
| 2 | ACETIC ANHYDRIDE [JF] | ACETIC ANHYDRIDE [JF] | |||
| 3 | 67341-27-9 | ACETIC ANHYDRIDE, [3H] | [3H] ACETIC ANHYDRIDE ACETIC ANHYDRIDE , [3H] | C4O3T6 | |
| 4 | ACETIC ANHYDRIDE 10X2ML | ACETIC ANHYDRIDE 10X2ML | C4H6O3 | ||
| 5 | 2742-27-0 | ACETIC ANHYDRIDE, [1-14C] | [1-14C] ACETIC ANHYDRIDE ACETIC ANHYDRIDE , [1- 14С] ACETIC ANHYDRIDE -CARBONYL-14C acetic anhydride -carbonyl-14C 1-20 mci*per mmol | C4H6O3 | |
| 6 | 285977-77-7 | ACETIC ANHYDRIDE-13C4, D6 | ACETIC ANHYDRIDE -13C4, D6 | C4D6O3 | Biomolecular MS;Stable Isotopes;AStable Isotopes;Alphabetical Listings;Chemical Labeling Products |
| 7 | acetic anhydride (recovery) | acetic anhydride (recovery) | |||
| 8 | 90980-78-2 | Acetic Anhydride (1,1-13C2) | ACETIC ANHYDRIDE 13C2 ACETIC-1- 13C Ангидрид Уксусной ангидрид (1,1-13C2) 13C помечен Аксусный ангидрид Акционированный ангидрид (1,1′-13C2) ACTIC-13C2-1.  101.102-1.102-1.101.101.1017.7.7.7.7.7.7.7.7.7-ACTID-1.101.101.101.1017.7.7.7.7-Anhydride (1,1′-13C2) ACTIC-1-ANHYDRIDE (1,1′-13C2). 101.102-1.102-1.101.101.1017.7.7.7.7.7.7.7.7.7-ACTID-1.101.101.101.1017.7.7.7.7-Anhydride (1,1′-13C2) ACTIC-1-ANHYDRIDE (1,1′-13C2). | A;Нет;Стабильные изотопы;Алфавитный список | |
| 9 | 98006-45-2 | ACETIC ANHYDRIDE (2,2′-13C2) | ACETIC-2-13C ANHYDRIDE ACETIC ANHYDRIDE (2,2′-13C2) | C4H6O3 | A; стабильные изотопы; алфавитные списки |
| 10 | 285977-78-8 | Акционированная ангидрид-1,1168.168.168.18.18.18.18.168.18.18.18.18.168.1668.168.168.168.168.168.168.168.168.168.168.168.168.18.18.168.18.168.18.168.18.168.18.18.18.168.168.168.16.18.168.168.168.168.168.168.168.16.18 | . | Биомолекулярный МС;Стабильные изотопы;Стабильные изотопы;Алфавитные списки;Химическая маркировка продуктов | |
| 11 | 285977-80-2 | Уксусной ангидрид-2,2′-13C2, D6 | Acetic Anhydride -2,28, D6285 . Алфавитные списки Алфавитные списки | ||
| 12 | 114510-14-4 | Аксусный ангидрид (1,1 ‘, 2,2′-136). 1,1′,2,2’-13C4) | C4H6O3 | Соединения, меченные стабильными изотопами | |
| 13 | 16649-49-3 | (Acetic anhydride)-d6 | — acetic anhydride ACETIC ANHYDRIDE -D6 ( Acetic anhydride )-d6 (2h4) Acetic anhydride Кислота уксусная-d3, ангидрид (~2~H_3_)этановый ангидрид Ди[(2,2,2-2h4)уксусная]ангидрид Бис(2,2,2-2h4) уксусный ангидрид Би[ (2,2,2-2h4)уксусная кислота]ангидрид | C4D6O3 | A;Стабильные изотопы;Стабильные изотопы;Дейтерированные реагенты;Алфавитные списки;Алфавитные списки |
| 14 | Acetic anhydride-13C4 99 atom % 13C | C4H6O3 | |||
| 15 | 108-24-7 | Acetic anhydride | Acetyl oxide Acetyl Anhydride Acetic anhydride АЦЕТИКАЦИДФЕНИЛМЕТИЛЭФИР Ангидрид уксусной кислоты (Контролируемое химическое вещество) | C4 H6 O3 | Реагент для получения производных; Органическое сырье; Соединения карбоновых кислот |
| 16 | АНГИДРИД УКСУСНОЙ-13C4 D6 99 АТОМ % 13C; | C4H5DO3 | |||
| 17 | ACETIC ANHYDRIDE-1 1′-13C2 D6 99 ATOM %& | C4H5DO3 | |||
| 18 | ACETIC ANHYDRIDE/LUTIDINE/TETRAHYDROFURAN | C15h33NO4 | |||
| 19 | Уксусный ангидрид-13C4,d6 97 ат. % D, 99 ат. % 13C % D, 99 ат. % 13C | C4H5DO3 | |||
| 20 | Acetic anhydride-1,1′-13C2,d6 99 atom % 13C, 99 atom % D |
| ID | КАС | Название продукта | Поставщики | Описания |
|---|---|---|---|---|
| 1 | 16649-49-3 | Уксусный ангидрид-d6 | Shanghai Macklin Biochemical Co., Ltd PREMIUM SUPPLIERS Упаковка: 5 г | |
| 2 | 16649-49-3 | Acetic Anhydride-D6 | Shanghai Yuanye Bio-Technology Co., Ltd. ПРЕМИУМ-ПОСТАВЩИКИ Цена (внутренняя, в юанях): 1 мг 24900 | Acetic Anhydride-D6 yuanye B71545 |
| 3 | 114510-14-4 | Acetic anhydride-13C4 | Shanghai Macklin Biochemical Co., Ltd Premium Pulciers Пакет : 50 мг | |
| 4 | 114510-14-4 | Укессуя Ангидрид-13C4 | Shanghai Macklin Biochemical Co., LTD Premium Suppliers Package : 50 мг | |
| 9 5 | 5 | 5 | 5 | .

 com
com