Высшие жирные спирты
Синонимы: ВЖС, Жирные спирты, Октил-дециловый спирт, Додецил-терадециловый спирт, Цетил-стеариловый спирт.
Формула: R-OH (где R – углеводородный радикал, содержащий от 6 до 22 атомов углерода, связанных насыщенными или, реже, ненасыщенными связями)
Природные и синтетические алифатические спирты, содержащие не менее 6 атомов углерода в молекуле. Природные ВЖС преимущественно одноатомные, первичные, насыщенные или ненасыщенные, с чётным числом атомов углерода; в виде эфиров высших жирных кислот они содержатся в растительных маслах, животных жирах, восках животного и растительного происхождения; в виде эфиров уксусной кислоты – в семенах растений, эфирных маслах; в свободном виде встречаются терпеновые спирты. ВЖС состава С6-С11 – бесцветные огнеопасные жидкости с фруктово-цветочным запахом; состава С12 и выше – твёрдые вещества.
Растворимы в эфире и этаноле, нерастворимы в воде.
ВЖС получают гидроформилированием алкенов; синтезом с использованием алюминийорганических соединений; гидрированием эфиров высших жирных кислот; окислением алканов; гидролизом или гидрированием растительных масел и жиров. Применяют ВЖС в качестве флотореагентов, растворителей, текстильно-вспомогательных веществ, пластификаторов полимеров, компонентов смазочных масел, присадок к моторным топливам и маслам, ингибиторов коррозии, а также в парфюмерии и косметике. ВЖС состава С10-С18 используются в производстве ПАВ.
Форма выпуска и внешний вид: низкомолекулярные (до С10) жирные спирты – жидкие, спирты, содержащие более 10 атомов углерода – твердые, воскообразные вещества.
Производство
Линейные жирные спирты с четным числом атомов углерода получают из растительных масел каталитическим гидрогинолизом метиловых эфиров соответствующих жирных кислот или их гидрированием.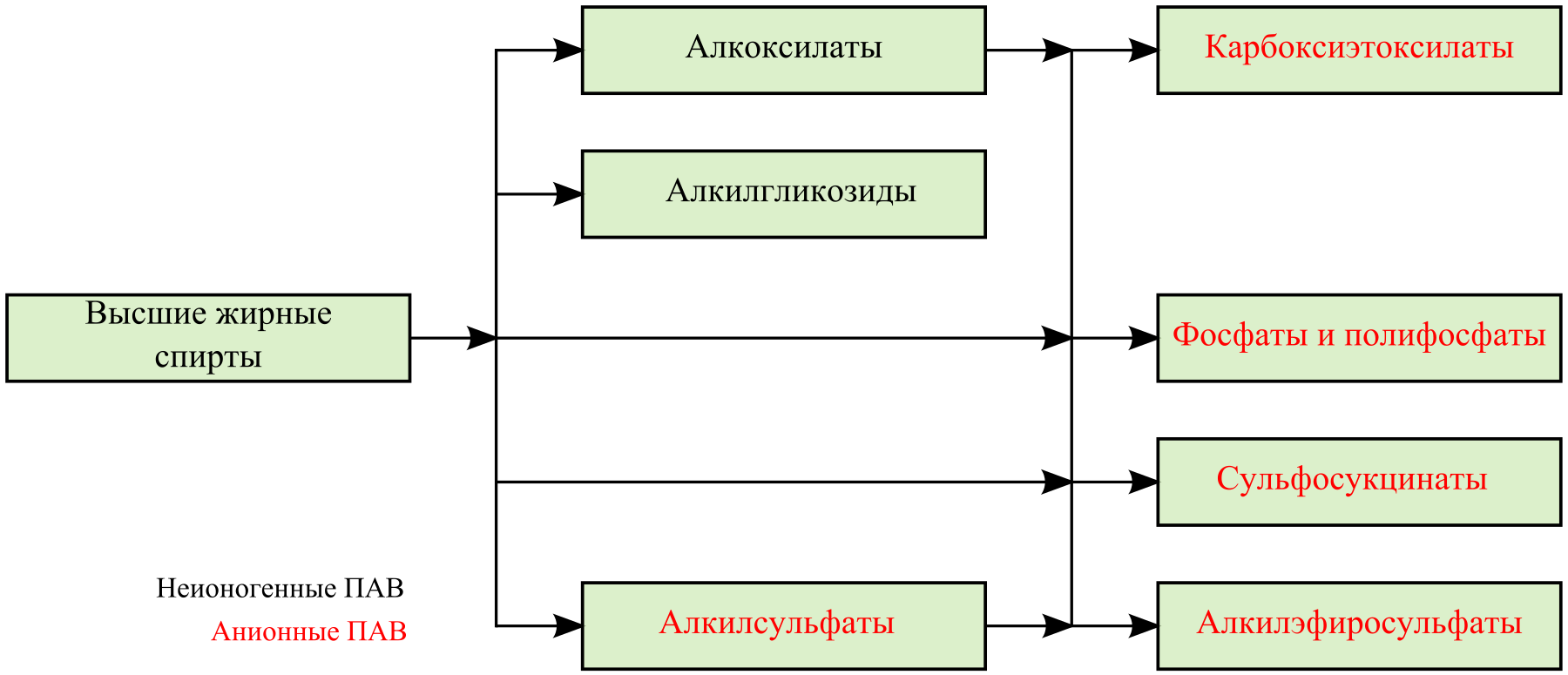
Свойства
Не растворяются в воде, за исключением спиртов С6–10, ограниченно растворимых в воде. Растворяются в эфирах и этаноле. Кислотные свойства практически отсутствуют в виду длины радикала. Обладают химическими свойствами спиртов.
Основные области и способы применения
Спирты С6–8 выполняют роль флотоагентов, с их помощью проводят избирательную экстракцию солей некоторых металлов (кобальта, ванадия, урана) из водных р-ров. Так же могут выступать в роли растворителей лакокрасочных материалов и синтетических смол. Эфиры спиртов С6–10 и дикарбоновых кислот (фталаты, адипинаты, себацинаты) – пластификаторы полимеров. Спирты С10–18 используют в производстве поверхностно-активных веществ. Спирты С10–20 – компоненты пеногасителей, ускорители вулканизации, текстильно-вспомогательные вещества; сырье в производстве пластификаторов, оксидов третичных аминов, ингибиторов коррозии.
Упаковка: Стандартные в зависимости от агрегатного состояния продукта – мешки для твердых или полимерные/стальные емкости для жидкостей.
Правила безопасности и хранение: Хранить продукт следует в сухих проветриваемых помещениях, в дали от источников тепла в оригинальной упаковке.
Высшие жирные спирты
Синонимы: ВЖС, Жирные спирты, Октил-дециловый спирт, Додецил-терадециловый спирт, Цетил-стеариловый спирт.
Формула:
R-OH (где R – углеводородный радикал, содержащий от 6 до 22 атомов углерода, связанных насыщенными или, реже, ненасыщенными связями)
Природные и синтетические алифатические спирты, содержащие не менее 6 атомов углерода в молекуле. Природные ВЖС преимущественно одноатомные, первичные, насыщенные или ненасыщенные, с чётным числом атомов углерода; в виде эфиров высших жирных кислот они содержатся в растительных маслах, животных жирах, восках животного и растительного происхождения; в виде эфиров уксусной кислоты – в семенах растений, эфирных маслах; в свободном виде встречаются терпеновые спирты. ВЖС состава С6-С11 – бесцветные огнеопасные жидкости с фруктово-цветочным запахом; состава С12 и выше – твёрдые вещества.
ВЖС состава С6-С11 – бесцветные огнеопасные жидкости с фруктово-цветочным запахом; состава С12 и выше – твёрдые вещества.
Растворимы в эфире и этаноле, нерастворимы в воде. ВЖС обладают химическими свойствами спиртов.
ВЖС получают гидроформилированием алкенов; синтезом с использованием алюминийорганических соединений; гидрированием эфиров высших жирных кислот; окислением алканов; гидролизом или гидрированием растительных масел и жиров. Применяют ВЖС в качестве флотореагентов, растворителей, текстильно-вспомогательных веществ, пластификаторов полимеров, компонентов смазочных масел, присадок к моторным топливам и маслам, ингибиторов коррозии, а также в парфюмерии и косметике. ВЖС состава С10-С18 используются в производстве ПАВ.
Форма выпуска и внешний вид: низкомолекулярные (до С10) жирные спирты – жидкие, спирты, содержащие более 10 атомов углерода – твердые, воскообразные вещества.
Производство
Линейные жирные спирты с четным числом атомов углерода получают из растительных масел каталитическим гидрогинолизом метиловых эфиров соответствующих жирных кислот или их гидрированием.
Свойства
Не растворяются в воде, за исключением спиртов С6–10, ограниченно растворимых в воде. Растворяются в эфирах и этаноле. Кислотные свойства практически отсутствуют в виду длины радикала. Обладают химическими свойствами спиртов.
Основные области и способы применения
Спирты С6–8 выполняют роль флотоагентов, с их помощью проводят избирательную экстракцию солей некоторых металлов (кобальта, ванадия, урана) из водных р-ров. Так же могут выступать в роли растворителей лакокрасочных материалов и синтетических смол. Эфиры спиртов С6–10 и дикарбоновых кислот (фталаты, адипинаты, себацинаты) – пластификаторы полимеров. Спирты С10–18 используют в производстве поверхностно-активных веществ. Спирты С10–20 – компоненты пеногасителей, ускорители вулканизации, текстильно-вспомогательные вещества; сырье в производстве пластификаторов, оксидов третичных аминов, ингибиторов коррозии.
Упаковка: Стандартные в зависимости от агрегатного состояния продукта – мешки для твердых или полимерные/стальные емкости для жидкостей.
Правила безопасности и хранение: Хранить продукт следует в сухих проветриваемых помещениях, в дали от источников тепла в оригинальной упаковке.
Высшие жирные спирты — Справочник химика 21
Для повышения эффективности газо- н нефтедобычи применяют различные химические реагенты, полученные на базе углеводородов нефти и газа (углеводородные растворители, поверхностно-активные вещества, полимерные реагенты и т. д.), а также отходы производства синтетических жирных кислот и высших жирных спиртов (включая кислые стоки), синтетических каучуков и полиолефинов, побочные продукты производства алкил-ароматических углеводородов, фенола и ацетона, мономеров для синтетического каучука и др. [c.184]Высшие жирные спирты, в молекуле которых содержится свыше 10 атомов углерода, представляют большой практический интерес для ряда отраслей народного хозяйства.
 На основе ВЖС вырабатываются различные поверхностно активные вещества, которые используются в качестве компонентов синтетических моющих средств, флотореагентов, вспомогательных веществ в текстильной промышленности, специальных отделочных препаратов в кожевенной, меховой, обувной и других отраслях промышленности. Высшие жирные спирты фракции Сю и выше приобрели большое значение для синтеза присадок к топливу и смазочным маслам, пластификаторов, гербицидов и некоторых других продуктов.
На основе ВЖС вырабатываются различные поверхностно активные вещества, которые используются в качестве компонентов синтетических моющих средств, флотореагентов, вспомогательных веществ в текстильной промышленности, специальных отделочных препаратов в кожевенной, меховой, обувной и других отраслях промышленности. Высшие жирные спирты фракции Сю и выше приобрели большое значение для синтеза присадок к топливу и смазочным маслам, пластификаторов, гербицидов и некоторых других продуктов. В настоящее время практический интерес для промышленного внедрения могут представить следующие методы производства высших жирных спиртов фракции Сю—Сго [c.137]
Высшие жирные спирты 120 2 [c.196]
Из сказанного выше видно, что масштабы потребления спиртов в очень сильной степени зависят от уровня технико-экономических показателей их производства. Снижение производственных затрат бесспорно приведет к дальнейшему расширению круга потребителей и увеличению масштабов использования высших жирных спиртов. В этой связи важнейшее значение выбор метода и сырья для производства высших спиртов. [c.135]
В этой связи важнейшее значение выбор метода и сырья для производства высших спиртов. [c.135]
Несмотря на чрезвычайно неблагоприятное соотношение цен, масштабы использования высших жирных спиртов для производства синтетических моющих средств не только не сокращаются, а наоборот, хотя и медленно, но неуклонно возрастают-. Дело в том, что синтетические моющие средства, приготовленные на основе натрийалкилсульфатов, являются в ряде случаев почти- незаменимым продуктом. [c.134]
ПРОИЗВОДСТВО высших ЖИРНЫХ СПИРТОВ j — ao [c.132]
Бутиловые спирты применяются также в целом ряде химических производств. Так, к-бутиловым спиртом этерифицируют жирные кислоты для последующего гидрирования эфиров с получением высших жирных спиртов. Нормальный бутанол и изобутанол являются весьма важными веществами при синтезе различных красителей, органических полупродуктов, ядохимикатов эфирного типа, душистых веществ, эссенций, фармацевтических препаратов.
 На базе этих спиртов синтезируют весьма ценные аминовые смолы. В США, например, для производства бутилами-нов и аминовых смол в 1961 г. было использовано 15% от выпуска н-бутилового и 10% от выпуска
На базе этих спиртов синтезируют весьма ценные аминовые смолы. В США, например, для производства бутилами-нов и аминовых смол в 1961 г. было использовано 15% от выпуска н-бутилового и 10% от выпуска Цены на сульфоэфиры высших жирных спиртов не только выше цен на алкиларилсульфонаты, но и подвержены очень резким колебаниям. Если цены на додецилбензолсульфонаты имели явно выраженную тенденцию к понижению, то цены на сульфаты высших жирных спиртов колебались в весьма широких пределах, что определялось исключительно соответствующими изменениями в ценах на жиры. К 1960 г. положение на мировом рынке не изменилось по-прежнему цена на высшие жирные спирты была высока и почти в 2,5 раза превосходила цену на додецилбензол [66] высшие жирные спирты несульфированные — 0,72 доллара за 1 кг, додецилбензол несульфированн
Жирные кислоты и спирты
Косметическая химия
Жирные кислоты и спирты.
Жирные кислоты
Жирные кислоты – это вещества, из молекул которых состоят более сложные молекулы природных жиров и восков, как растительного,
так и животного происхождения.
Химическое строение
К жирным кислотам относятся предельные и непредельные карбоновые кислоты с открытой цепью атомов углерода.
Карбоновые кислоты характеризуются присутствием карбоксильной группы (карбоксила):
Формула карбоксила:
или упрощённо – СООН.
Примерами карбоновых кислот могут служить муравьиная,уксусная или пропионовая кислоты:
По числу углеродных атомов карбоновые кислоты могут быть:
1. Низшими (С1-С3),
2. Средними (С4-С8) и
3. Высшими (С9-С26).
Жирными кислотами, как правило, называют именно высшие карбоновые кислоты, но иногда жирными называют все ациклические карбоновые кислоты.
По степени насыщенности углеродной цепи атомами водорода различают насыщенные (предельные) и ненасыщенные (непредельные) жирные кислоты.
Предельные и непредельные органические вещества
Различие между предельными и непредельными органическими веществами легче проиллюстрировать на примере углеводородов.
В предельных углеводородах соседние атомы углерода связаны простой, одинарной связью.
Например:
При валентности углерода равной четырем, он может устанавливать связи с четырьмя другими атомами. Одна чёрточка соответствует одной связи.
В непредельных углеводородах атомы углерода могут быть связаны двойными и тройными связями. При этом количество атомов водорода в молекуле сокращается.
Так в случае двойных связей мы имеем:
Примером углеводорода с тройной связью является Ацетилен:
Так и в случае жирных кислот. В предельных (насыщенных) кислотах атомы углерода связаны одинарными связями.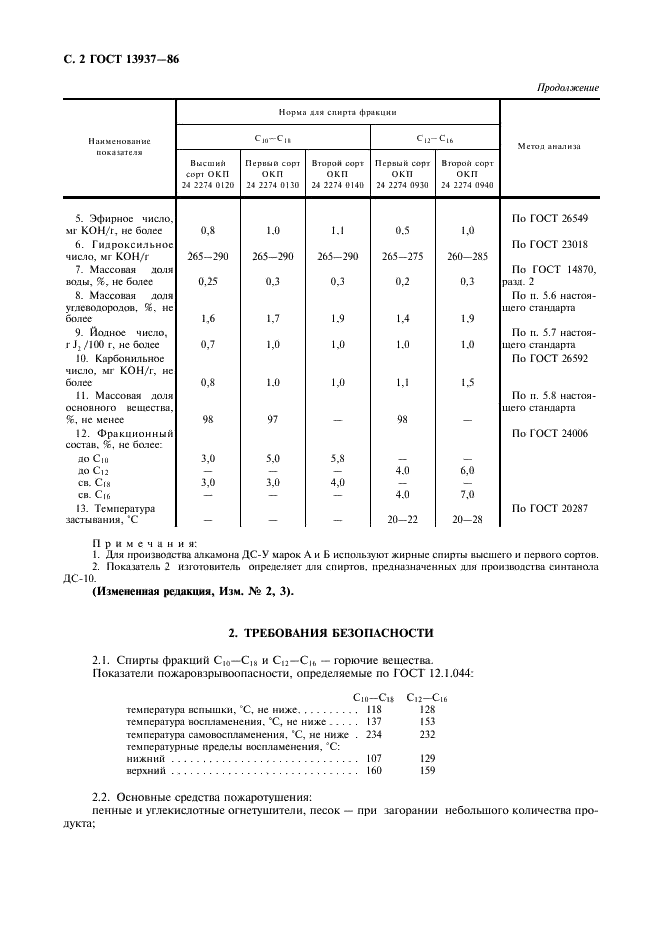
В непредельных жирных кислотах некоторые атомы углерода могут быть связаны двойными связями.
Высшие жирные кислоты.
В состав животных и растительных жиров, в большинстве случаев, входят жирные кислоты с относительно большим числом атомов углерода (С9-С26). Такие жирные кислоты называются высшими жирными кислотами.
Примеры предельных высших жирных кислот:
1. Каприновая кислота — C9h29COOH,
2. Лауриновая кислота — С11Н23СООН,
3. Миристиновая кислота — С13Н27СООН,
4. Пальмитиновая кислота — С15Н31СООН,
5. Стеариновая кислота – С17Н35СООН.
Примеры непредельных высших жирных кислот:
1. Олеиновая кислота — С17Н33СООН, – имеет одну двойную связь,
2. Линолевая кислота – С17Н31СООН, — имеет две двойных связи,
3. Линоленовая кислота – С17Н29СООН. – имеет три двойных связи.
Линоленовая кислота – С17Н29СООН. – имеет три двойных связи.
Структурные формулы соединений, в которых присутствуют длинные углеводородный радикалы, часто изображают следующим образом:
Зависимость свойств жирных кислот от наличия в них предельных и непредельных связей.
Предельные и непредельные жирные кислоты имеют в значительной степени различные свойства.
Так все перечисленные выше предельные жирные кислоты (миристиновая, пальмитиновая, стеариновая и пр.) – твёрдые воскообразные вещества без цвет и запаха.
В таком виде они представляют собой прекрасное сырьё для приготовления различных кремов и эмульсий.
Перечисленные выше непредельные жирные кислоты (олеиновая, линолевая, линоленовая) являются жидкими при комнатной температуре.
Из-за наличия в них двойных связей они менее устойчивы к действию микробов и могут легко разлагаться на вещества с молекулами меньшего размера,
часто имеющие неприятный запах.
Таким образом, непредельные жирные кислоты быстро портятся и поэтому имеют маленький срок хранения.
Поэтому их гидрируют по двойным связям.
Гидрирование (гидрогенизация) — химическая реакция, включающая присоединение водорода к органическому веществу.
В результате из всех трёх вышеназванных ненасыщенных жирных кислот получается стеариновая кислота С17Н35СООН, твёрдая по консистенции. (По этой причине гидрогенезацию жиров называют отвержением жиров.)
Жирные спирты
Напомним, что спиртами называют производные углеводородов, в молекулах которых один или несколько молекул водорода заменены гидроксильными группами (ОН). Например, СН3-ОН (метиловый спирт), С2Н5-ОН (этиловый спирт), С3Н7-ОН (пропиловый спирт).
Так, углеводороду метану соответствует метиловый спирт, а этану — этиловый:
К жирным спиртам относят высокомолекулярные спирты, т. е. спирты, содержащие сравнительно большое количество атомов
углерода и также многоатомные спирты, имеющие несколько гидроксильных групп (ОН).
е. спирты, содержащие сравнительно большое количество атомов
углерода и также многоатомные спирты, имеющие несколько гидроксильных групп (ОН).
Многоатоные спирты глицерин и этиленгликоль:
Эфиры высших жирных спиртов и высших жирных кислот называются восками.
Характерными представителями жирных спиртов являются цетиловый спирт C16h43OH, ради которого раньше велся промысел кашалотов и мирициловый спирт С31Н63ОН, который в связанном виде содержится в пчелином воске.
К жирным спиртам относится широко известный холестерин, основе которого лежит ядро стерана:
Важнейшими спиртами, используемыми при производстве косметики, являются стеариловый спирт С18Н37ОН и цетиловый спирт C16h43OH.
Жирные спирты получают переработкой натуральных жиров и восков.
Они представляют собой жироподобные вещества, хорошо ложащиеся на кожу. Они легко смешиваются с кожным салом и создают прекрасное дополнение к основе кремов, помад и других средств, улучшая их свойства.
Простые омыляемые липиды. Воски и жиры.
Биоорганическая химия
Простые омыляемые липиды. Воски, жиры и масла.
В группу «простых омыляемых липидов» входят Воски, жиры и масла.
О названии
Сначала пару слов о названии «Простые омыляемые липиды».
Простыми они называются потому, что в отличие от «сложных липидов», они включают в свою структуру только атомы углерода (С), водорода (H) и кислорода (О).
Сложные липиды в своём составе дополнительно имеют атомы других элементов. При этом их структура действительно сложнее.
Омыляемыми они называются из-за того, что при гидролизе из них образуются соли высших карбоновых кислот, т.е. мыла.
Воски
Восками называют сложные эфиры одноатомных жирных спиртов и высших жирных кислот.
Сложные эфиры — это такие соединения, где углеводородные радикалы (в данном случае одноатомные жирные спирты и высшие жирные кислоты) соединены между собой через атом кислорода.
Радикалы, при этом, могут быть разными, но их всегда будет связывать атом кислорода.
Реакция образования сложного эфира из кислоты и спирта называется реакцией этерификации.
Воски образуют защитную плёнку на коже человека и животных и предохраняют растения от высыхания.
Примером воска может служить цетиловый эфир пальмитиновой кислоты – главный компонент спермацета. Спермацет содержится в спермацетовом масле. Ранее это масло извлекали из головы кашалотов и использовали
в качестве индифферентной основы для приготовления различных мазей.
Спермацет содержится в спермацетовом масле. Ранее это масло извлекали из головы кашалотов и использовали
в качестве индифферентной основы для приготовления различных мазей.
Другой эфир пальмитиновой кислоты – мирицилпальмитат – содежится в пчелином воске.
Любой природный воск всегда имеет сложный состав. Это не один единственный сложный эфир, это много разных сложных эфиров с различными компонентами.
Пчелиный воск, в своём составе, имеет около 50 веществ. Помимо сложных эфиров это могут быть свободные жирные кислоты, жирные спирты, витамины и пр. Но основу вещества всё равно будут составлять сложные эфиры.
Жиры и масла
По химическому строению жиры близки к воскам. Недаром они объединены в одну группу.
Так же, как и воски, жиры это сложные эфиры высших жирных кислот и спирта.
Но если в состав восков могут входить различные высокомолеклярные одноатомные спирты, то вместо них в состав жиров вседа входит трёхатомный спирт глицерин.
Напомним, что спирты это производные углеводородов, в молекулах которых один или несколько атомов водорода заменены гидроксильными группами (ОН).
Если в молекуле спирта одна гидроксильная группа, то такой спирт называется одноатомным, если их больше – многоатомным.
В составе глицерина три гидроксильных группы. Поэтому это трёхатомный спирт:
Высокомолекулярными (или высшими жирными) называют спирты с относительно большим числом атомов углерода.
Например, приведённые выше цетиловый спирт C16H33OH или мирициловый спирт С31Н63ОН.
Глицерин С3Н5(ОН)3 не относится к высшим жирным спиртам.
Итак, жиры – это сложные эфиры высших жирных кислот и трёхатомного спирта глицерина.
Такие сложные эфиры называют триглицеридами.
Жиры — это триглицериды высших жирных кислот.
В живых организмах жиры, прежде всего, играют роль структурного компонента клеток или запасного вещества («жировое депо»). Их энергетическая ценность примерно в 2 раза выше, чем у белков и углеводов.
Наряду с углеводами и белками, жиры — один из главных компонентов питания.
Твёрдые триглицериды обычно называют жирами, жидкие – маслами.
Простые триглицериды содержат остатки одинаковых кислот, смешанные – различных.
По аналогии с восками можно сказать, что природные жиры и масла, как растительные, так и животные – это сложные вещества, состоящие из многих компонентов. Они представляют собой смеси смешанных триглицеридов.
В триглицеридах животного происхождения преобладают остатки насыщенных кислот. Эти триглицериды, как правило, твёрдые вещества.
Напротив жидкие растительные масла содержат в основном остатки ненасыщенных кислот.
Помимо триглицеридов в их состав могут входить свободные жирные кислоты, жирные спирты, сложные липиды, витамины и пр.
Сульфат — высший жирный спирт
Сульфат — высший жирный спирт
Cтраница 1
Сульфаты высших жирных спиртов являются одним из лучших типов синтетических моющих средств и получили широкое применение в промышленности и в быту. Исходные жирные спирты получают из кашалотового жира, кокосового или таллового масла. Синтетические способы основываются на непосредственном окислении парафиновых углеводородов, на восстановлении жирных кислот, полученных окислением парафина, на методе оксосинтеза ( см. стр. Последний способ имеет то преимущество, что позволяет получать спирты с нормальной цепью, что особенно ценно для эффективности моющего действия.
[1]
Исходные жирные спирты получают из кашалотового жира, кокосового или таллового масла. Синтетические способы основываются на непосредственном окислении парафиновых углеводородов, на восстановлении жирных кислот, полученных окислением парафина, на методе оксосинтеза ( см. стр. Последний способ имеет то преимущество, что позволяет получать спирты с нормальной цепью, что особенно ценно для эффективности моющего действия.
[1]
Сульфаты высших жирных спиртов изредка применяют самостоятельно, но они скорее пригодны как осадители катион-активных антистатических веществ при стойкой обработке пластмасс и текстильных волокон. [2]
Сульфаты высших жирных спиртов являются одним из лучших типов синтетических моющих средств и получили широкое применение в промышленности и в быту. Исходные жирные спирты получают из кашалотового жира, кокосового или таллового масла. Синтетические способы основываются на непосредственном окислении парафиновых углеводородов, на восстановлении жирных кислот, полученных окислением парафина, на методе оксосинтеза ( см. стр. Последний способ имеет то преимущество, что позволяет получать спирты с нормальной цепью, что особенно ценно для эффективности моющего действия.
[3]
стр. Последний способ имеет то преимущество, что позволяет получать спирты с нормальной цепью, что особенно ценно для эффективности моющего действия.
[3]
Сульфаты высших жирных спиртов особенно успешно используются для стирки шелка, шерсти и синтетических тканей. [4]
Наилучшими пенообразующими свойствами обладают сульфаты высших Жирных спиртов. Разветвление гидрофобной части молекулы моющего вещества ухудшает пенообразующие свойства. [6]
Представителями истинных сульфокислот являются продукты конденсации высших жирных кислот или сульфатов высших жирных спиртов с низкомолекулярными ароматическими или гидроароматическими сульфокислотами. Эти соединения ( RArSO3H), давно запатентованные36 и описанные в литературе36, являются предшественниками современных алкиларилсульфонатов, произв 1д — ство которых появилось спустя несколько десятков лет и достигло в настоящее время больших размеров. Уже тогда, в 1923 г., Адам37 установил, что алкиларилсульфонаты с низкомолекулярными боковыми цепями, например С3 или С4, обладают лишь капиллярно-активными свойствами, ноне обладают такими моющими свойствами, как соединения, боковые цепи которых содержат 10 — 18 углеродных атомов.
[7]
Уже тогда, в 1923 г., Адам37 установил, что алкиларилсульфонаты с низкомолекулярными боковыми цепями, например С3 или С4, обладают лишь капиллярно-активными свойствами, ноне обладают такими моющими свойствами, как соединения, боковые цепи которых содержат 10 — 18 углеродных атомов.
[7]
В Германии оксосинтез применялся во время второй мировой войны главным образом для производства сульфатов высших жирных спиртов, представляющих собой высококачественные моющие и смачивающие вещества. В качестве сырья исходили из смеси олефннов Си — С17, получаемой термическим крекингом низкоплавкого парафина, образующегося при синтезе Фишера-Тропша. Практически этот процесс во время второй мировой войны применялся в весьма ограниченном объеме. [8]
Несколько позднее основой такого моющего средства стала смесь лаурил-сульфата и алкилбензолсуль фоната. В настоящее время применяются сульфаты высших жирных спиртов, получаемых из жирных кислот сала. Их смесь с определенным количеством алкилбензолсульфоната ( что повышает их слабую растворимость) обладает многими преимуществами по сравнению с любым из этих компонентов, взятым в отдельности.
[9]
В настоящее время применяются сульфаты высших жирных спиртов, получаемых из жирных кислот сала. Их смесь с определенным количеством алкилбензолсульфоната ( что повышает их слабую растворимость) обладает многими преимуществами по сравнению с любым из этих компонентов, взятым в отдельности.
[9]
Цены на сульфоэфиры высших жирных спиртов не только выше цен на алкиларилсульфонаты,
Frontiers | Анализ метаболического потока 13C для систематической метаболической инженерии S. cerevisiae при избыточном производстве жирных кислот
1. Введение
Несмотря на несколько успехов (Keasling and Chou, 2008; Goh et al., 2014), производство возобновляемых, экономичных и экологически устойчивых видов топлива и химикатов путем микробной ферментации остается сложной задачей (Sims et al., 2010). Особый интерес вызывает производство биотоплива второго поколения, которое может принести значительные экологические выгоды в виде снижения глобальной зависимости от сырой нефти и минимизации производства CO 2 (Naik et al. , 2010). Биотопливо и биопродукты второго поколения также обладают более высокой плотностью энергии и улучшенными эксплуатационными и эксплуатационными характеристиками (например, смешиваемость с водой) по сравнению с этанолом, произведенным из кукурузного сырья (Fortman et al., 2008). Некоторые типы биотоплива второго поколения могут быть произведены из жирных кислот, полученных путем ферментации сахаров, в которых свободные жирные кислоты могут быть преобразованы в алканы путем каталитической этерификации или декарбоксилирования (Fjerbaek et al., 2009). И наоборот, организм-хозяин может быть сконструирован для преобразования жирных кислот в этиловые эфиры жирных кислот [FAEE, Steen et al.(2010a)]. Более того, необработанные жирные кислоты со средней длиной цепи (C6 – C14) обычно используются в промышленности в качестве источников для биопродуктов, помимо биотоплива: смазочных материалов, косметики и фармацевтических препаратов. Свободные жирные кислоты также можно непосредственно гидрогенизировать с образованием жирных спиртов (Voeste and Buchold, 1984).
, 2010). Биотопливо и биопродукты второго поколения также обладают более высокой плотностью энергии и улучшенными эксплуатационными и эксплуатационными характеристиками (например, смешиваемость с водой) по сравнению с этанолом, произведенным из кукурузного сырья (Fortman et al., 2008). Некоторые типы биотоплива второго поколения могут быть произведены из жирных кислот, полученных путем ферментации сахаров, в которых свободные жирные кислоты могут быть преобразованы в алканы путем каталитической этерификации или декарбоксилирования (Fjerbaek et al., 2009). И наоборот, организм-хозяин может быть сконструирован для преобразования жирных кислот в этиловые эфиры жирных кислот [FAEE, Steen et al.(2010a)]. Более того, необработанные жирные кислоты со средней длиной цепи (C6 – C14) обычно используются в промышленности в качестве источников для биопродуктов, помимо биотоплива: смазочных материалов, косметики и фармацевтических препаратов. Свободные жирные кислоты также можно непосредственно гидрогенизировать с образованием жирных спиртов (Voeste and Buchold, 1984).
Предыдущие инженерные попытки с Saccharomyces cerevisiae (Rodriguez et al., 2016) для производства биотоплива на основе жирных кислот (Runguphan and Keasling, 2014) из сахаров, например, включали сверхэкспрессию всех трех генов биосинтеза жирных кислот, а именно , ацетил-КоА-карбоксилаза ( ACC1 ), синтаза жирных кислот 1 ( FAS1 ) и синтаза жирных кислот 2 ( FAS2 ), а также нокаутирующие жирные ацил-КоА синтетазы 1 и 4 ( FAA1 и FAA4 ).Изменение терминального превращающего фермента в сконструированном штамме привело к образованию свободных жирных кислот с титром ~ 400 мг / л, жирных спиртов ~ 100 мг / л и этиловых эфиров жирных кислот (биодизель) с концентрацией ~ 5 мг / л. непосредственно из простых сахаров при выращивании во встряхиваемой колбе. Более поздняя работа (Zhou et al., 2016) позволила достичь титра свободных жирных кислот 1 г / л при культивировании во встряхиваемой колбе и 10,4 г / л при культивировании с подпиткой. Помимо блокирования активации и деградации жирных кислот и сверхэкспрессии ACC1 , клетка была дополнительно сконструирована путем введения оптимизированного пути ацетил-КоА и экспрессии более эффективной синтазы жирных кислот. Несмотря на этот прогресс, для получения коммерчески жизнеспособных штаммов необходимы более высокие урожаи, титр и продуктивность. Кроме того, для достижения этой цели было бы желательно разработать систематические методы. Эти систематические методы не должны в значительной степени полагаться на подробные биохимические знания выбранного хозяина или пути, а, скорее, быть обобщаемыми и предлагать неинтуитивные инженерные подходы.
Несмотря на этот прогресс, для получения коммерчески жизнеспособных штаммов необходимы более высокие урожаи, титр и продуктивность. Кроме того, для достижения этой цели было бы желательно разработать систематические методы. Эти систематические методы не должны в значительной степени полагаться на подробные биохимические знания выбранного хозяина или пути, а, скорее, быть обобщаемыми и предлагать неинтуитивные инженерные подходы.
Метаболическое моделирование позволяет систематически определять генетические модификации, которые могут повысить урожайность.Моделирование метаболизма на основе потоков особенно хорошо подходит для этой цели, поскольку метаболические потоки описывают, как углерод перемещается от корма к конечному продукту. Анализ баланса потоков (FBA) ранее успешно использовался для этой цели (Asadollahi et al., 2009; Park et al., 2009). FBA получает потоки, используя сеть клеточного метаболизма, которая включает все реакции или, по крайней мере, столько, сколько может быть выведено из генома посредством метаболической реконструкции, которая дает стехиометрическую модель в масштабе генома (Thiele and Palsson, 2010). Эта модель в масштабе генома сочетается с предположением о линейном программировании (LP), согласно которому метаболизм настраивается из-за эволюционного давления, чтобы максимизировать скорость роста [или могут использоваться другие эволюционные предположения, см. Schuetz et al. (2007)]. Двухуровневый анализ метаболического потока 13 C (2S- 13 C MFA) улучшает FBA за счет сохранения метаболической сети в масштабе генома, но отбрасывает эволюционное предположение в пользу ограничений 13 C из клеточных метаболитов, измеренных экспериментально (Мартин и другие., 2015). Это достигается путем моделирования потоков на двух разных уровнях разрешения: для основных метаболитов и реакций используется как стехиометрия, так и информация об углеродной маркировке, тогда как для остальных неосновных метаболитов и реакций отслеживается только стехиометрия, и их вклад в основной маркировка набора считается незначительной. Этот многомасштабный подход действителен до тех пор, пока метаболический поток течет от ядра к периферическому метаболизму и не течет обратно, предположение, которое подтверждается хорошим соответствием между экспериментально измеренным и вычисленным распределением мечения, полученным в целом с помощью методов 13 C MFA до настоящего времени [которые рассматривают только основные реакции, Moxley et al.
Эта модель в масштабе генома сочетается с предположением о линейном программировании (LP), согласно которому метаболизм настраивается из-за эволюционного давления, чтобы максимизировать скорость роста [или могут использоваться другие эволюционные предположения, см. Schuetz et al. (2007)]. Двухуровневый анализ метаболического потока 13 C (2S- 13 C MFA) улучшает FBA за счет сохранения метаболической сети в масштабе генома, но отбрасывает эволюционное предположение в пользу ограничений 13 C из клеточных метаболитов, измеренных экспериментально (Мартин и другие., 2015). Это достигается путем моделирования потоков на двух разных уровнях разрешения: для основных метаболитов и реакций используется как стехиометрия, так и информация об углеродной маркировке, тогда как для остальных неосновных метаболитов и реакций отслеживается только стехиометрия, и их вклад в основной маркировка набора считается незначительной. Этот многомасштабный подход действителен до тех пор, пока метаболический поток течет от ядра к периферическому метаболизму и не течет обратно, предположение, которое подтверждается хорошим соответствием между экспериментально измеренным и вычисленным распределением мечения, полученным в целом с помощью методов 13 C MFA до настоящего времени [которые рассматривают только основные реакции, Moxley et al. (2009); Kajihata et al. (2015)]. 2S- 13 C MFA сочетает информативные ограничения экспериментов по маркировке 13 C со стехиометрией в масштабе генома для улучшения определения метаболических потоков и установления доверительных интервалов на основе экспериментальных данных. Этот метод позволяет нам ограничивать метаболические потоки без необходимости углеродных переходов для каждой реакции в модели в масштабе генома (Gopalakrishnan and Maranas, 2015a, b) и обеспечивает оценки потоков для периферического метаболизма, такого как производство жирных кислот, которые являются предметом исследования. эта рукопись.
(2009); Kajihata et al. (2015)]. 2S- 13 C MFA сочетает информативные ограничения экспериментов по маркировке 13 C со стехиометрией в масштабе генома для улучшения определения метаболических потоков и установления доверительных интервалов на основе экспериментальных данных. Этот метод позволяет нам ограничивать метаболические потоки без необходимости углеродных переходов для каждой реакции в модели в масштабе генома (Gopalakrishnan and Maranas, 2015a, b) и обеспечивает оценки потоков для периферического метаболизма, такого как производство жирных кислот, которые являются предметом исследования. эта рукопись.
В этой статье мы улучшили штамм S. cerevisiae (WRY2), который ранее был сконструирован для производства свободных жирных кислот (Runguphan and Keasling, 2014). Предыдущие метаболические вмешательства для этого штамма состояли из сверхэкспрессии ацетил-КоА карбоксилазы и синтаз жирных кислот, а также устранения FAA1 и FAA4, участвующих в пути деградации жирных кислот S. cerevisiae . Анализ потока позволил улучшить эту деформацию (см. Рисунок 1).Сначала мы провели эксперименты с индикатором 13 C на WRY2, чтобы мы могли применить 2S- 13 C MFA для определения потоков в модели метаболизма в масштабе генома для нашего эталонного штамма. Мы использовали этот новый подход для определения потоков для WRY2 как до, так и после увеличения продукции ацетил-КоА посредством добавления цитратлиазы АТФ [ACL, Rodriguez et al. (2016)] из Yarrowia lipolytica . Хотя ацетил-КоА является субстратом для производства жирных кислот, введение ACL привело лишь к небольшому увеличению выработки жирных кислот, примерно на 5%.2S- 13 C MFA определил, что наиболее значительным стоком ацетил-КоА после введения ACL является синтез малата. После подавления синтеза малата мы измерили значительное увеличение продукции жирных кислот на 26%. Наконец, поскольку производство жирных кислот увеличивалось по мере того, как мы спроектировали WRY2 за счет добавления ACL и подавления MLS, 2S- 13 C MFA показал, что путь глицерин-3-фосфатдегидрогеназы ( GPD1 ), который конкурирует за углерод с производственным путем ацетил-КоА, действует как большой поглотитель углерода.
cerevisiae . Анализ потока позволил улучшить эту деформацию (см. Рисунок 1).Сначала мы провели эксперименты с индикатором 13 C на WRY2, чтобы мы могли применить 2S- 13 C MFA для определения потоков в модели метаболизма в масштабе генома для нашего эталонного штамма. Мы использовали этот новый подход для определения потоков для WRY2 как до, так и после увеличения продукции ацетил-КоА посредством добавления цитратлиазы АТФ [ACL, Rodriguez et al. (2016)] из Yarrowia lipolytica . Хотя ацетил-КоА является субстратом для производства жирных кислот, введение ACL привело лишь к небольшому увеличению выработки жирных кислот, примерно на 5%.2S- 13 C MFA определил, что наиболее значительным стоком ацетил-КоА после введения ACL является синтез малата. После подавления синтеза малата мы измерили значительное увеличение продукции жирных кислот на 26%. Наконец, поскольку производство жирных кислот увеличивалось по мере того, как мы спроектировали WRY2 за счет добавления ACL и подавления MLS, 2S- 13 C MFA показал, что путь глицерин-3-фосфатдегидрогеназы ( GPD1 ), который конкурирует за углерод с производственным путем ацетил-КоА, действует как большой поглотитель углерода. Мы выбили GPD1 в наших сконструированных штаммах, чтобы было доступно больше потока углерода для производства жирных кислот, и, как и ожидалось, эти штаммы увеличили производство жирных кислот на 33%. В целом генетические вмешательства, примененные в этой работе, увеличили производство жирных кислот примерно на 70%.
Мы выбили GPD1 в наших сконструированных штаммах, чтобы было доступно больше потока углерода для производства жирных кислот, и, как и ожидалось, эти штаммы увеличили производство жирных кислот на 33%. В целом генетические вмешательства, примененные в этой работе, увеличили производство жирных кислот примерно на 70%.
Рис. 1. Обзор метаболических путей S. cerevisiae , имеющих отношение к этому исследованию и метаболическим вмешательствам . Ненативная цитратлиаза АТФ (ACL) была введена с целью увеличения поступления ацетил-CoA (accoa), но продукция жирных кислот существенно не увеличилась (рис. 2).Использование анализа потока показало, что действительно было произведено больше ацетил-КоА, но оно было потеряно в результате синтеза малата (MLS, рис. 3). Подавление этого фермента увеличивало производство жирных кислот (ЖК) на 26% (рис. 2). Повторное использование анализа потока предложило исключить производство глицерина (GPD1) для увеличения производства. Производство ТВС увеличилось на 33% (Рисунок 2). Митохондриальный и пероксисомальный компартменты представлены синими и желтыми кружками соответственно. Аббревиатуры метаболитов соответствуют базе данных BIGG (Schellenberger et al., 2010).
Производство ТВС увеличилось на 33% (Рисунок 2). Митохондриальный и пероксисомальный компартменты представлены синими и желтыми кружками соответственно. Аббревиатуры метаболитов соответствуют базе данных BIGG (Schellenberger et al., 2010).
2. Материалы и методы
2.1. Среда, культивирование и трансформация дрожжей
Родительский штамм для всей генной инженерии, WRY2, был создан, как описано в Runguphan and Keasling (2014). Для конструирования штамма (см. Таблицу 1) прекультуры выращивали с 5 мл среды дрожжевой экстракт + пептон + декстроза (YPD) в стеклянных пробирках при 30 ° C и встряхивании при 200 об / мин. Через 18 ч роста прекультуры использовали для инокуляции культур объемом 50 мл в колбы Эрленмейера на 250 мл.Через 6 часов роста штаммы трансформировали методом ацетата лития (Gietz and Woods, 2002) линейной ДНК, содержащей кассету генетической модификации, как указано ниже. Трансформированные дрожжевые клетки высевали на неселективный агар YPD + 2% и выращивали при 30 ° C в течение 18 часов. Полученные клетки реплики высевали на чашки с агаром YPD + 200 мг / л следующих селективных антибиотиков: гигромицин B (X), нурсеотрицин (X) или G418 (X). Колонии собирали через 2 дня и повторно наносили штрихами на селективную среду.Интеграцию генетических модификаций подтверждали проведением ПЦР колоний на одной колонии размноженного штамма.
Полученные клетки реплики высевали на чашки с агаром YPD + 200 мг / л следующих селективных антибиотиков: гигромицин B (X), нурсеотрицин (X) или G418 (X). Колонии собирали через 2 дня и повторно наносили штрихами на селективную среду.Интеграцию генетических модификаций подтверждали проведением ПЦР колоний на одной колонии размноженного штамма.
Таблица 1. Список штаммов и генотипов .
2.2. Конструкция штамма
ПЦР-амплификацию выполняли с использованием ДНК-полимеразы Prime STAR GXL, используя инструкции производителя (Takara). Праймеры, использованные в этом исследовании, перечислены в таблице 2. Сборки выполняли с использованием мастер-микса для сборки Gibson (New England Biolabs) и трансформировали в компетентные клетки Dh20b для размножения.Плазмидную ДНК очищали с использованием набора QIAprep Spin Miniprep (QIAGEN), и плазмиды секвенировали с 2-кратным покрытием (Quintara). Последовательности ДНК, полученные из S. cerevisiae , амплифицировали из геномной ДНК, полученной с использованием модифицированного протокола Miniprep: 1 мл культуры дрожжевых клеток в среде YPD центрифугировали в пробирке с завинчивающейся крышкой (3000 × г ) и ресуспендировали в буфере P1 ( из комплекта Qiagen). Клетки лизировали добавлением стеклянных шариков и встряхиванием в настольном гомогенизаторе / инструменте для взбивания шариков (FastPrep-24, MP Biomedicals) в течение ~ 1 мин.Полученную суспензию использовали для оставшихся этапов протокола Qiagen Miniprep.
Клетки лизировали добавлением стеклянных шариков и встряхиванием в настольном гомогенизаторе / инструменте для взбивания шариков (FastPrep-24, MP Biomedicals) в течение ~ 1 мин.Полученную суспензию использовали для оставшихся этапов протокола Qiagen Miniprep.
Таблица 2. Список праймеров, использованных в данном исследовании .
Для конструирования GPD1 :: hphMX4 ( GPD1 нокаут) кассету hphMX4 амплифицировали из pAG32 (Goldstein and McCusker, 1999) с праймерами, содержащими 50 п.н., соответствующих хромосомной последовательности, расположенной непосредственно через 5 ‘и 3’ локуса GPD1.
Для конструирования NatMX3-PTEF1m2 :: PMLS1 (подавление MLS1 ) кассету NatMX3-PTEF1m2 амплифицировали из pAG35-PTEF1m2, плазмиды, содержащей кассету NatMX3 непосредственно на 5 ‘от PTEF1m2.pAG35-PTEF1m2 был получен путем рестрикционного клонирования следующим образом: мутантный вариант промотора TEF1 был амплифицирован из p416-TEFm2 (Nevoigt et al. , 2006) с использованием праймеров, фланкированных сайтами рестрикции, и полученный ампликон был лигирован в Bam HI. и сайтов Hin dIII pAG35 (Goldstein and McCusker, 1999).
, 2006) с использованием праймеров, фланкированных сайтами рестрикции, и полученный ампликон был лигирован в Bam HI. и сайтов Hin dIII pAG35 (Goldstein and McCusker, 1999).
Для строительства ura3 :: P PGK1 — Yl ACLb-P TEF1 — Yl ACLa-kanMX4 (добавление ACL), P PGK1 — Yl ACLb-P — TEF0009 Кассета Y1 ACLa-kanMX4 была получена рестрикционным гидролизом плазмиды pCV278 с Pme I.pCV278 получали путем замены промоторов GAL1 / 10 из pCV256 на промоторы PGK1 / TEF1 с использованием реакции сборки Гибсона с 3 фрагментами. Сборка была разработана с использованием программного обеспечения BioCAD Device Editor (Chen et al., 2012), а сборочные праймеры были созданы с помощью программного обеспечения автоматизации проектирования сборки j5 DNA (Hillson et al., 2012) с использованием настроек по умолчанию. Фрагмент, содержащий Yl ACLb-P TEF1 — Yl ACLa-kanMX4, был амплифицирован из pCD256, а промоторы TEF1 / PGK1 были амплифицированы из геномной ДНК дрожжей.
Непосредственно перед производственными экспериментами все штаммы трансформировали pESC-Leu2d-’TesA и высевали на -Leu. Колонии росли через 2 дня, и их использовали для инокуляции минимальной среды с соответствующими выпадающими аминокислотами: CSM с 60 мг / л His, 90 мг / л Lys, 60 мг / л Ura и 60 мг / л Met (среда HKUM).
2.3. 13 C Эксперименты по маркировке
Все жидкие культивирования проводили в минимальной среде (1 × дрожжевое азотное основание, 1,5% глюкоза и 1 М фосфатный буфер в среде HKUM).После предварительного культивирования в течение ночи в среде с минимальным содержанием глюкозы 30 мл культур инокулировали до исходного OD 600 0,05 и выращивали во встряхиваемых колбах на 250 мл при 30 ° C и 250 об / мин. Аликвоты отбирали во время фазы экспоненциального роста глюкозы. Для экспериментов по анализу потока глюкоза в естественном изобилии была заменена смесью 80% глюкозы 1- 13 C и 20% изотополога U- 13 C ( 13 C-обогащение Z99%, Cambridge Usotope Laboratories, США). И более).Отбор проб для измерения метки метаболитов для всех штаммов проводили через 15 ч: 6–8 мл культуры из жидких культур были удалены для измерения метаболитов с помощью LCMS (см. Ниже). Концентрации внеклеточных метаболитов измеряли с помощью ВЭЖХ в двух временных точках: 13 и 15 часов. Эти измерения позже были преобразованы в потоки с использованием значений OD для различных деформаций; коэффициент перевода OD в сухой вес клеток (cdw) составлял 0,835.
И более).Отбор проб для измерения метки метаболитов для всех штаммов проводили через 15 ч: 6–8 мл культуры из жидких культур были удалены для измерения метаболитов с помощью LCMS (см. Ниже). Концентрации внеклеточных метаболитов измеряли с помощью ВЭЖХ в двух временных точках: 13 и 15 часов. Эти измерения позже были преобразованы в потоки с использованием значений OD для различных деформаций; коэффициент перевода OD в сухой вес клеток (cdw) составлял 0,835.
2.4. Измерение шаблонов маркировки (векторов распределения масс, MDV)
Для образцов с метаболитами 5 мл культуры клеток осаждали при 8000 × г в течение 3 минут при 4 ° C и ресуспендировали в 300 мкл метанола, 300 мкл хлороформа и 250 мкл воды.После встряхивания суспензию переносили в 1,7 мл пробирку с завинчивающейся крышкой и добавляли 500 мкл гранул. Взбивание шариков проводили на образцах в течение 10 с 10 раз с 1 мин на льду между образцами. Затем 350 мкл водного слоя удаляли из пробирки и фильтровали через отсекающий фильтр Millipore ™ Amicon Ultra с молекулярной массой 3 кДа при 14000 × г в течение 60 мин при -2 ° C. В проточный поток добавляли воду до общего объема 1 мл. После мгновенного замораживания (жидким азотом) и лиофилизации образцы перед анализом восстанавливали в 50 мкл метанол-вода (50:50, об. / Об.).
В проточный поток добавляли воду до общего объема 1 мл. После мгновенного замораживания (жидким азотом) и лиофилизации образцы перед анализом восстанавливали в 50 мкл метанол-вода (50:50, об. / Об.).
Для измерения внутриклеточных аминокислот жидкостное хроматографическое разделение проводили при 30 ° C на колонке Kinetex HILIC (длина 100 мм, внутренний диаметр 4,6 мм, размер частиц 2,6 мкм; Phenomenex, Torrance, CA, USA) с использованием Система ВЭЖХ серии 1200 (Agilent Technologies, Санта-Клара, Калифорния, США). Объем инъекции для каждого измерения составлял 2 мкл. Поднос для образцов и отделение колонки были установлены на 6 и 40 ° C соответственно. Подвижная фаза состояла из 20 мМ ацетата аммония в воде (растворитель A) и 10 мМ ацетата аммония в 90% ацетонитриле и 10% воды (растворитель B) (степень чистоты для ВЭЖХ, Honeywell Burdick & Jackson, CA, США).Ацетат аммония получали из исходного раствора 100 мМ ацетата аммония и 0,7% муравьиной кислоты (химическая чистота 98–100%, от Sigma-Aldrich, Сент-Луис, Миссури, США) в воде. Аминокислоты были разделены следующим градиентом: от 90 до 70% B за 4 минуты, выдержка при 70% B в течение 1,5 минут, от 70 до 40% B за 0,5 минуты, выдержка при 40% B в течение 2,5 минут, от 40 до 90% B через 0,5 мин, выдержку при 90% B в течение 2 мин. Скорость потока варьировалась следующим образом: поддерживалась на уровне 0,6 мл / мин в течение 6,5 минут, линейно увеличивалась от 0,6 до 1 мл / мин за 0,5 минуты и поддерживалась на уровне 1 мл / мин в течение 4 минут.Общее время работы 11 мин. Параметры масс-спектрометрии можно найти в Bokinsky et al. (2013).
Аминокислоты были разделены следующим градиентом: от 90 до 70% B за 4 минуты, выдержка при 70% B в течение 1,5 минут, от 70 до 40% B за 0,5 минуты, выдержка при 40% B в течение 2,5 минут, от 40 до 90% B через 0,5 мин, выдержку при 90% B в течение 2 мин. Скорость потока варьировалась следующим образом: поддерживалась на уровне 0,6 мл / мин в течение 6,5 минут, линейно увеличивалась от 0,6 до 1 мл / мин за 0,5 минуты и поддерживалась на уровне 1 мл / мин в течение 4 минут.Общее время работы 11 мин. Параметры масс-спектрометрии можно найти в Bokinsky et al. (2013).
Сбор и обработка данных выполнялись с помощью программного пакета MassHunter. Массовое распределение изотопомеров аминокислоты было получено без фрагментации. Исходя из массового распределения изотопомеров аминокислот, потоки рассчитывали с помощью программного обеспечения 2S- 13 C MFA, как описано ниже. Образцы маркировки были измерены для следующих внутриклеточных аминокислот: глицин (Gly), аланин (Ala), валин (Val), треонин (Thr), лейцин (Leu), изолейцин (Ile), аспарагин (Asp), глутамат (Glu). , глутамин (Gln), аргинин (Arg), фенилаланин (Phe) и тирозин (Tyr).
, глутамин (Gln), аргинин (Arg), фенилаланин (Phe) и тирозин (Tyr).
2,5. Концентрации биомассы и внеклеточных метаболитов
Концентрации биомассы определяли путем регистрации OD 600 с помощью спектрофотометра (Novaspec II, Pharmacia Biotech, Упсала, Швеция). Концентрации внеклеточных метаболитов этанола, ацетата, глицерина и глюкозы определяли с помощью системы ВЭЖХ Agilent серии 1200, оснащенной детектором с фотодиодной матрицей, установленным на 210, 254 и 280 нм (Agilent Technologies, Санта-Клара, Калифорния, США). Разделение метаболитов проводили на колонке Aminex HPX-87H с 8% сшивкой (длина 150 мм, 7.Внутренний диаметр 8 мм и размер частиц 9 мкм; Bio-Rad, Ричмонд, Калифорния, США). Объем вводимой пробы составлял 5 мкл. Поднос для образцов и отделение колонки были установлены на 4 и 50 ° C соответственно. Изократическое элюирование проводили 4 мМ серной кислотой при скорости потока 0,6 мл / мин. Система ВЭЖХ была оборудована детектором показателя преломления (Agilent Technologies), который использовался для обнаружения органических кислот и глюкозы. Сбор и анализ данных выполнялись с помощью программного обеспечения Agilent Chemstation.Выходы биомассы получали путем линейной аппроксимации концентраций субстрата или побочных продуктов во время экспоненциального роста как функции соответствующих концентраций биомассы. Затем умножение на скорость роста дало конкретные скорости поглощения глюкозы и секреции побочных продуктов. Физиологические параметры определяли по крайней мере в двух независимых биологических повторностях.
Сбор и анализ данных выполнялись с помощью программного обеспечения Agilent Chemstation.Выходы биомассы получали путем линейной аппроксимации концентраций субстрата или побочных продуктов во время экспоненциального роста как функции соответствующих концентраций биомассы. Затем умножение на скорость роста дало конкретные скорости поглощения глюкозы и секреции побочных продуктов. Физиологические параметры определяли по крайней мере в двух независимых биологических повторностях.
2,6. ГХ – МС анализ свободных жирных кислот
Для получения свободных жирных кислот штаммы предварительно культивировали в аликвотах по 5 мл в минимальной среде (1 × азотное основание дрожжей, 1.5% глюкозы и 1M фосфатного буфера в среде HKUM) в течение ночи и использовали для инокуляции 30 мл минимальной среды (1 × дрожжевое азотное основание, 1,5% глюкоза и 1M фосфатный буфер в среде HLKUM) в культурах из колб объемом 250 мл для достижения начальная ОП 600 0,05. Через 96 ч в 100 мкл дрожжевой культуры добавляли 5 мкл стандарта пентадекановой кислоты (3 мг / мл) и затем смешивали с 10 мкл 40% об. / Об. Раствора гидроксида тетрабутиламмония (TBAH) (Sigma). Затем к образцу добавляли 100 мкл дихлорметана (DCM) / йодметана (MeI), и смесь перемешивали на вортексе в течение 10 с.Органический (нижний) слой переносили в пробирку для ГХМС, и растворителю давали полностью испариться. Затем к экстракту добавляли 100 мкл свежего DCM, и образцы обрабатывали с использованием ранее описанного метода (Steen et al., 2010b) с некоторыми незначительными отличиями. Программа ГХ была следующей: начальная температура 40 ° C поддерживалась в течение 3 минут, после чего следовало повышение до 250 ° C со скоростью 20 ° C / мин, при этом температура поддерживалась в течение 5 минут.
/ Об. Раствора гидроксида тетрабутиламмония (TBAH) (Sigma). Затем к образцу добавляли 100 мкл дихлорметана (DCM) / йодметана (MeI), и смесь перемешивали на вортексе в течение 10 с.Органический (нижний) слой переносили в пробирку для ГХМС, и растворителю давали полностью испариться. Затем к экстракту добавляли 100 мкл свежего DCM, и образцы обрабатывали с использованием ранее описанного метода (Steen et al., 2010b) с некоторыми незначительными отличиями. Программа ГХ была следующей: начальная температура 40 ° C поддерживалась в течение 3 минут, после чего следовало повышение до 250 ° C со скоростью 20 ° C / мин, при этом температура поддерживалась в течение 5 минут.
2,7. Расчет потока
Потоки были рассчитаны через 2S- 13 C MFA (Martín et al., 2015), используя код, который включен в дополнительный материал. В нем можно найти файлы, содержащие всю входную информацию для 2S- 13 C MFA: информацию о маркировке корма, измеренные внеклеточные потоки, углеродные переходы, измеренную информацию о маркировке и файл SBML для модели в масштабе генома [iMM904 (Mo et al. , 2009)]. Подробные инструкции о том, как рассчитать потоки и получить цифры в этой рукописи, можно найти в блокноте jupyter, предоставленном в качестве дополнительных материалов.
, 2009)]. Подробные инструкции о том, как рассчитать потоки и получить цифры в этой рукописи, можно найти в блокноте jupyter, предоставленном в качестве дополнительных материалов.
Для целей подгонки измеренных паттернов мечения, внутриклеточные аминокислоты считались цитозольными, как предполагалось в предыдущих исследованиях (Moxley et al., 2009). Доверительные интервалы для потоков были рассчитаны с помощью анализа изменчивости потока 13 C ( 13 C FVA) путем решения уравнений (16–23) в работе Martín et al. (2015). Эта процедура позволила нам рассчитать все потоки, совместимые с данными маркировки [уравнение (23) в Martín et al. (2015)], а не только потоки, которые наилучшим образом соответствуют данным, — фрагмент информации, имеющий жизненно важное значение для получения достоверных выводов.Доверительные интервалы представлены на протяжении всей рукописи как, например, 0,5 [0,3–0,66], где 0,5 — это поток, который наилучшим образом соответствует имеющимся экспериментальным данным, 0,3 — самый низкий поток, который совместим с данными, а 0,66 — самый высокий поток, совместимый с данными. с данными. Анализ изменчивости внешнего мечения (ELVA) был проведен и использован для определения размера основного набора реакций, как объяснено в Martín et al. (2015).
с данными. Анализ изменчивости внешнего мечения (ELVA) был проведен и использован для определения размера основного набора реакций, как объяснено в Martín et al. (2015).
3. Результаты
3.1. Только ACL минимально увеличивает производство жирных кислот
Цитратлиаза АТФ (ACL) — это фермент, который обычно не присутствует в S.cerevisae (Rodriguez et al., 2016), но у других организмов, таких как растения или маслянистые дрожжи, продуцирует дополнительный цитозольный ацетил-КоА, который в дальнейшем действует как предшественник при производстве жирных кислот или многих тысяч других специализированных метаболитов, включая воски. , стерины и поликетиды. В присутствии АТФ и кофермента А в цитоплазме ACL катализирует расщепление цитрата с образованием ацетил-КоА, оксалоацетата, АДФ и ортофосфата (см. Рисунок 1):
цитрат + АТФ + CoA + h3O → оксалоацетат + ацетил – CoA + ADP + Pi Поскольку фермент ACL продуцирует предшественники ацетил-КоА (Rodriguez et al. , 2016), мы ввели ACLY (из Y. lipolytica ), содержащие плазмиды, в наш штамм WRY2 (см. Методы) для увеличения продукции ацетил-КоА в WRY2, как было показано в случае продукции n -бутанол (Lian et al., 2014). Это привело к небольшому увеличению производства жирных кислот на 5% (рис. 2). Чтобы выяснить, почему ожидаемое увеличение продукции ацетил-КоА не привело к увеличению продукции жирных кислот, мы использовали 2S- 13 C MFA.
, 2016), мы ввели ACLY (из Y. lipolytica ), содержащие плазмиды, в наш штамм WRY2 (см. Методы) для увеличения продукции ацетил-КоА в WRY2, как было показано в случае продукции n -бутанол (Lian et al., 2014). Это привело к небольшому увеличению производства жирных кислот на 5% (рис. 2). Чтобы выяснить, почему ожидаемое увеличение продукции ацетил-КоА не привело к увеличению продукции жирных кислот, мы использовали 2S- 13 C MFA.
Рис. 2. Производство жирных кислот для различных штаммов, изученных в этой рукописи . S. cerevisiae WRY2 — основной штамм, использованный для этих исследований. Ожидалось, что добавление ACL повысит доступность ацетил-КоА, но не увеличит конечное производство. Однако подавление MLS действительно увеличивало производство, как показывает анализ потока. Наивысшая производительность была достигнута за счет прекращения производства глицерина, что привело к увеличению производства в общем технологическом процессе на 70%.Показанные здесь измерения жирных кислот были выполнены в конце 100 часов, а столбики ошибок представляют стандартное отклонение, полученное для трех повторов.
3.2. 2S- 13 C MFA указывает на то, что ацетил-КоА выводится из метаболизма жирных кислот через малат-синтазу
Чтобы диагностировать и исправить небольшое увеличение продукции жирных кислот на фоне увеличения продукции субстрата ацетил-КоА путем добавления ACL-содержащих плазмид к нашему штамму WRY2, мы выполнили 2S- 13 C MFA для определения субстрата ацетил-КоА судьбы.Потоки для реакций производства и потребления ацетил-КоА для сконструированного штамма-продуцента жирных кислот WRY2 и штамма WRY2 с ACL можно найти на Фигуре 3, показывающей общегеномный баланс, определенный с помощью 2S- 13 C MFA. Общее количество ацетил-КоА, продуцируемого штаммом WRY2 ACL (2,42 ммоль / г вес / ч), кажется, почти вдвое больше, чем у штамма WRY2 (1,25 ммоль / г вес / ч) из-за добавления продукции ацетил-КоА с помощью ACL 0,5 ммоль / г вес. / ч и увеличение продукции ацетил-КоА ацетил-КоА синтетазой (ACS) на ~ 0.7 ммоль / гвт / ч. Однако эти оценки потока имеют очень большие доверительные интервалы: 0,52–1,44 ммоль / г дедвейта / час для потока ACS, где наилучшим образом подходит 1,25 ммоль / г дедвейта / час для штамма WRY2 и 1,38–4,85 ммоль / г сухого веса / час для добавки. ACS и ACL потока, где 2,42 — добавление наилучшего соответствия для штамма WRY2 с ACL. Доверительные интервалы представляют собой максимальные и минимальные значения этого потока, совместимые с данными маркировки 13 C (см. Методы). Следовательно, реальный поток для ACS в деформации WRY2 может быть где угодно между 0.52 и 1,44, но лучше всего подходит для данных 1,25, и аналогично реальный поток для добавления ACS и ACL может быть где угодно в интервале 1,38–4,85, но наше лучшее предположение составляет 2,42, основываясь на данных. Эти широкие доверительные интервалы представляют собой тот факт, что для модели в масштабе генома метаболиты могут следовать различными путями к заданному месту назначения, а имеющиеся экспериментальные данные (мечение метаболитов и измеренные обменные потоки) не могут полностью определить, какие из них используются. Это множество доступных путей может быть захвачено 2S- 13 C MFA, но не 13 C MFA (Martín et al., 2015). Таким образом, общий поток ацетил-КоА изменился со значения от 0,52 до 1,44 до значения от 1,38 до 4,85 (что может означать отсутствие изменений), где наши наилучшие совпадения указывают на удвоение с 1,25 до 2,42. Однако мы увидим, что, несмотря на эти большие доверительные интервалы, мы по-прежнему можем использовать эту информацию, чтобы направлять усилия метаболической инженерии для увеличения производства (рис. 2). Следовательно, добавление ACL, по-видимому, увеличивает общую продукцию субстрата ацетил-КоА, но данные показывают, что этот эффект компенсируется увеличением потребления ацетил-КоА малатсинтазы (MALS) примерно на 1.0 ммоль / гСт / ч ([0,47–1,53] конф. Интервал), с небольшим потоком, перенаправленным на ацетил-КоА-карбоксилазу (ACCOACr, путь к метаболизму жирных кислот): 0,49 ммоль / гСт / ч ([0,49–0,83] конф. . интервал) по сравнению с 0,67 ммоль / г р.т. / ч ([0,67–1,93] конф. интервал). Это согласуется с небольшим увеличением производства жирных кислот после добавления ACL (рис. 2).
Рис. 3. Цитозольные балансы ацетил-КоА, полученные из 2S- 13 C MFA для WRY2, WRY2 ACL и WRY2 ACL P TEF1 -MLS1 .Поток реакций образования и потребления ацетил-КоА (accoa) показан в виде диаграммы Санки. Реакции слева на диаграмме производят ацетил-коА, а реакции справа потребляют его, размер стрелки указывает на общий поток. Названия реакций и метаболитов соответствуют правилам базы данных BIGG (Schellenberger et al., 2010). Цифры под названиями реакций указывают на лучшее соответствие данным и доверительные интервалы. Например, ацетил-коА-синтетаза (ACS) для WRY2 показывает, что поток, который лучше всего соответствует данным, равен 1.25, но поток может иметь любое значение от 0,52 до 1,44 (доверительные интервалы). Верхняя диаграмма (WRY2) показывает, что весь ацетил-КоА вырабатывается ACS, а MALS может действовать как поглотитель, хотя это не гарантировано (нижний доверительный интервал равен 0). После добавления ACL (WRY2 ACL) общее количество ацетил-КоА увеличивается, но становится очевидным сток углерода в MALS (нижний доверительный интервал 0,47> 0), что согласуется с отсутствием увеличения производства жирных кислот (рис. 2). Подавление MALS (WRY2 ACL P TEF1 -MLS1), по-видимому, привело к увеличению потока в метаболизм жирных кислот, для которого реакция ACCOACr является первым шагом.Доверительные интервалы для ACCOACr до и после подавления ([0,67–1,93] против [0,84–3,01]) слишком широки, чтобы сделать такой вывод, но увеличение производства жирных кислот (рис. 2) указывает на то, что это так.
Поскольку анализ потока показал, что дополнительный ацетил-КоА, обеспечиваемый ACL, направляется в реакцию MALS, мы решили, что нашим следующим инженерным шагом будет подавление гена, соответствующего MALS, в надежде, что это увеличит поток углерода в сторону синтез жирных кислот.Хотя было показано, что ген MLS1 , который кодирует цитозольную малатсинтазу, транскрибируется в основном во время роста на источниках углерода C 2 , транскрипция MLS1 также наблюдалась во время роста на глюкозе (Regenberg et al., 2006). Следовательно, делеция или подавление MLS1 должно способствовать увеличению цитозольного поступления ацетил-КоА. Мы обнаружили, что нокаут MLS1 привел к очень медленно растущему штамму (возможно, из-за накопления ацетил-КоА, который может быть токсичным из-за ацетилирования белка).Этот эффект не представлял для нас интереса, поскольку мы сосредоточены на общем производстве жирных кислот, в отличие от Криворучко и др. (2013), которые обнаружили, что нокаут MLS1 является ключевой частью инженерной стратегии по увеличению производства бутанола на основе ацетил-КоА в 6,5 раз. Однако мы обнаружили, что подавление MLS1 (методы), вместо того, чтобы выбивать его, привело к появлению жизнеспособных штаммов и немедленному увеличению выработки жирных кислот примерно на 26% (рис. 2). Хотя это согласуется с нашим предыдущим выводом о том, что реакция MALS является значительным стоком углерода, доверительные интервалы для потока MALS до и после подавления ([0.47–1,53] vs. [0,35–2,19], рисунок 3) слишком широки, чтобы подтвердить, что поток MALS действительно уменьшился. Хотя наиболее подходящие значения (1,0 по сравнению с 1,19) увеличились, доверительные интервалы обеспечивают диапазон всех возможных потоков, совместимых с доступными экспериментальными данными, и не являются достаточно узкими, чтобы подтвердить или опровергнуть уменьшение потока MALS. Этот случай подчеркивает силу нашего анализа, который позволяет нам судить о степени достоверности наших выводов и о том, когда уместно сделать дальнейшие выводы.
3.3. Нокаут GPD1 улучшает производство жирных кислот
Глицерин-3-фосфатдегидрогеназа (кодируется GPD1 ) катализирует превращение дигидроксиацетонфосфата в глицерин-3-фосфат и играет важную роль в синтезе липидов. Кроме того, он конкурирует за поток углерода с путями синтеза жирных кислот на основе ацетил-КоА, уровни производства которых мы пытаемся максимизировать (рис. 1). Используя 2S- 13 C MFA, мы определили, что поток через реакцию GPD1ir [аббревиатуры реакций соответствуют базе данных BIGG (Schellenberger et al., 2010)] в штаммах WRY2, WRY2 ACL и WRY2 ACL P TEF1 -MLS1 равными 2,45 [2,45–2,45], 0,6 [0,68–0,685] и 1,68 [1,2–1,69] ммоль / гдв / ч. Поэтому, когда мы разработали WRY2 для увеличения потока продукции свободных жирных кислот, конкурирующий путь глицерин-3-фосфатдегидрогеназы отклонял углерод от производства жирных кислот. Если бы этот конкурирующий поток углерода можно было бы уменьшить путем выбивания GPD1, могло бы быть доступно для производства жирных кислот больше потока углерода. Как и ожидалось, штаммы WRY2 ΔGPD1 и WRY2 ΔGPD1 ACL имели более высокую продукцию жирных кислот, чем WRY2 и WRY2 ACL, на 22 и 56% соответственно (рис. 2).
Подтверждая нашу интуицию о том, что выбивание GPD1 позволяет увеличить поток углерода в синтез жирных кислот на основе ацетил-КоА, профили потока 2S- 13 C MFA на наших нокаутных штаммах GPD1 предполагают увеличение производства ацетил-КоА (Рисунок 4 ). Несмотря на широкие доверительные интервалы для потоков, мы можем видеть, что общий поток в производство жирных кислот (ACCOACr на рисунках 3 и 4) удваивается благодаря представленному здесь инженерному процессу ([0,49–0,83] для WRY2 на рисунке 3 по сравнению с [1 .43–3.39] для WRY2 ΔGPD1 ACL P TEF1 -MLS1 на рисунке 4). Как и ожидалось, меньше глицерина продуцируется штаммами, у которых был выбит GPD1 (рис. 5).
Рисунок 4. Цитозольные балансы ацетил-КоА, полученные из 2S- 13 C MFA для штаммов с нокаутом GPD1 . Поток реакций производства и потребления ацетил-КоА (accoa) показан в виде диаграммы Сэнки, как на рисунке 3. Несмотря на большие доверительные интервалы для рассчитанных потоков, можно сделать несколько выводов.Общий поток через ACCOACr, например, удваивается посредством полного процесса проектирования, представленного здесь: сравните [0,49–0,83] для WRY2 на рисунке 3 с [1,43–3,39] для WRY2 ΔGPD1 ACL P TEF1 -MLS1 на этом рисунке. Кроме того, эффект нокаута GPD1 определенно увеличивает поток через ACCOACr ([0,49–0,83] для WRY2 на Рисунке 3 по сравнению с [0,97–4,38] для WRY2 ΔGPD1). Кроме того, эффект ACL включает определенную активацию реакции MALS как поглотителя углерода (эффект, аналогичный показанному на рисунке 3).
Рис. 5. Скорость роста и внешние концентрации метаболитов: показаны внешние концентрации метаболитов для этанола, глицерина и ацетата для штаммов, изучаемых в этой рукописи . Биомасса для этих штаммов отображается в виде оптической плотности при 600 нм (OD 600 ). Все измерения представляют собой среднее значение для трех биологических повторов.
3.4. Скорость роста и внешние концентрации метаболитов
Поскольку мы спроектировали WRY2 для увеличения производства жирных кислот, мы обнаружили, что скорость роста и конечная биомасса через 62 часа изменились незначительно (рис. 5).В целом, нам удалось повысить выработку жирных кислот с 460 до 780 мг / л, что на 70% больше, за счет добавления ACL, подавления MALS и нокаута GPD1 , но это метаболическое бремя было недостаточно большим, чтобы замедлить рост наших штаммов. Аналогичным образом, концентрации внешних метаболитов между штаммами были качественно аналогичными, при этом измеренные концентрации метаболитов усреднены по трем биологическим повторениям, показанным с течением времени на рисунке 5.
4. Обсуждение
В этом исследовании мы показали, что можем использовать профили потока, полученные из 2S- 13 C MFA, для руководства и устранения неполадок в процессе биоинженерии, направленного на увеличение выхода продукта.Профили потока, полученные из 2S- 13 C MFA, описывающие балансы ацетил-CoA (которые, как считается, являются ограничивающим фактором), предоставили действенное понимание усилий метаболической инженерии, которые привели к увеличению производства жирных кислот на 70%. Хотя доверительные интервалы потоков велики, их все же можно успешно использовать для управления инженерными усилиями. Первоначально базовый штамм был дополнен ACL в надежде произвести больше ацетил-КоА. Профили потока показывают, что ACL эффективен в увеличении продукции ацетил-КоА, порядка ~ 0.На 5 ммоль / г вес / час выше, чем для одного штамма WRY2. Однако это дополнительное предложение ацетил-КоА не направляется на производство жирных кислот, а, скорее, направляется на производство малата через MALS. Снижая активность малатсинтазы, мы смогли увеличить выработку жирных кислот на 26%. Точно так же потеря углерода через GPD1 предполагает, что отключение этой реакции увеличит производство. Этот нокаут привел к увеличению образования ацетил-КоА, а также к увеличению продукции жирных кислот на 70% по сравнению с эталонным штаммом в сочетании с подавлением ACL и MALS.
Вероятно, можно будет увеличить уровень производства свободных жирных кислот. Измерения метаболитов и биомассы качественно очень похожи для всех наших сконструированных штаммов, что указывает на то, что метаболическая нагрузка по производству свободных жирных кислот на уровнях производства, достигнутых в этой рукописи, не является серьезной, даже если мы увеличили производство жирных кислот на 70%. На темпы роста еще не повлияли предпринятые шаги метаболической инженерии, что, вероятно, указывает на то, что максимальные уровни производства не были достигнуты.
Возможный способ дальнейшего увеличения производства включает использование другого типа гена ACL. Происхождение гена ACL, использованного в рукописи, — это Y. lipolytica , который представляет собой облигатные аэробные маслянистые дрожжи, способные накапливать большие количества липидов, преимущественно триацилглицеринового типа (Papanikolaou et al., 2002). Хотя ранее было показано, что ACL из Y. lipolytica обеспечивает активность цитратлиазы АТФ при экспрессии в плазмидах S. cerevisiae (Rodriguez et al., 2016), ACL из Aspergillus nidulans , как известно, примерно в пять раз активнее в цитоплазме (Rodriguez et al., 2016) S. cerevisase . Значительное увеличение продукции жирных кислот могло бы быть возможным, если бы штаммы, изученные в этой рукописи, были воссозданы с геном ACL из A. nidulans , как было показано при использовании ACL из Mus musculus (Zhou et al. ., 2016). Однако следует отметить, что такое увеличение производства было получено, когда модель M.musculus ACL был объединен с дальнейшей разработкой в поставке ацетил-КоА и более эффективной синтазы жирных кислот.
Другая стратегия повышения продуктивности может включать обход пируватдегидрогеназы (ПДГ) (Kozak et al., 2014; Lian et al., 2014). Наши результаты согласуются с доступностью предшественника жирной кислоты ацетил-КоА в качестве фактора, ограничивающего производство жирных кислот для штаммов S. cerevisiae , изученных в этой рукописи. Метаболизм ацетил-КоА у дрожжей сильно разделен на четыре пространственные области: цитозоль, митохондрии, пероксисомы и ядро.Ацетил-КоА в цитоплазме продуцируется субстратом ацетальдегидом, образованным декарбоксилированием пирувата. К сожалению, большая часть гликолитического потока направляется на производство этанола из-за эффекта Крэбтри (Van et al., 1998) при выращивании на глюкозе. Это ограничивает доступность ацетил-КоА в цитозоле, при этом более ранние исследования показали, что такие стратегии, как создание обхода ПДГ в S. cerevisiae , усиливают цитозольную поставку ацетил-КоА, что приводит к увеличению производства продуктов, производных ацетил-КоА, таких как как изопреноиды аморфадиена (Shiba et al., 2007) и α -сантален (Chen et al., 2013) и полигидроксибутират (Kocharin et al., 2012). Подобная инженерная стратегия может быть использована для дальнейшего улучшения производства жирных кислот в наших наиболее продуктивных штаммах.
Авторские взносы
AG, WR, EB, GW, CD и JG проводили эксперименты. Компания AG произвела расчеты потоков. Газету написали DA, HM, AG, JK и CD.
Заявление о конфликте интересов
JK имеет финансовые интересы в Амирис и Лигос.Остальные авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Финансирование
Эта работа, проведенная Объединенным институтом биоэнергетики, была поддержана Управлением науки, Управлением биологических и экологических исследований Министерства энергетики США по контракту № DE-AC02-05Ch21231. Правительство Соединенных Штатов оставляет за собой право, а издатель, принимая статью к публикации, подтверждает, что Правительство Соединенных Штатов сохраняет за собой неисключительную, оплаченную, безотзывную и всемирную лицензию на публикацию или воспроизведение опубликованной формы этой рукописи или разрешение другие делают это в целях правительства США.
Дополнительные материалы
Дополнительные материалы к этой статье можно найти в Интернете по адресу https://www.frontiersin.org/article/10.3389/fbioe.2016.00076
Дополнительный файл 1 — Zip-файлы, включая файлы кода и 2S- 13 C MFA Jupyter Notebook
Код, используемый для получения результатов (требуются лицензии GAMS и CONOPT), вместе с записной книжкой jupyter [Perez and Granger (2007), www.jupyter.org], которая производит все рисунки потока, используемые в этой рукописи.
Список литературы
Асадоллахи, М. А., Мори, Дж., Патил, К. Р., Шалк, М., Кларк, А., и Нильсен, Дж. (2009). Повышение производства сесквитерпена в Saccharomyces cerevisiae с помощью метаболической инженерии in silico. Metab. Англ. 11, 328–334. DOI: 10.1016 / j.ymben.2009.07.001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бокинский, Г., Байду, Э. Е. К., Акелла, С., Бурд, Х., Уивер, Д., Алонсо-Гутьеррес, Дж. И др.(2013). Остановка роста, вызванная HipA, и толерантность к β-лактаму в Escherichia coli опосредуются RelA-зависимым синтезом ppGpp. J. Bacteriol. 195, 3173–3182. DOI: 10.1128 / jb.02210-12
CrossRef Полный текст | Google Scholar
Брахманн, К. Б., Дэвис, А., Кост, Г. Дж., Капуто, Э., Ли, Дж., Хитер, П. и др. (1998). Дизайнерские штаммы с делециями, полученные из Saccharomyces cerevisiae S288C: полезный набор штаммов и плазмид для опосредованного ПЦР разрушения генов и других приложений. Дрожжи 14, 115–132. DOI: 10.1002 / (sici) 1097-0061 (19980130) 14: 2 <115: aid-yea204> 3.0.co; 2-2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чен, Дж., Денсмор, Д., Хэм, Т. С., Кислинг, Дж. Д., и Хиллсон, Н. Дж. (2012). DeviceEditor визуальный биологический холст САПР. J. Biol. Англ. 6, 1. doi: 10.1186 / preaccept-1967068768635731
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чен, Ю., Давиет, Л., Шалк, М., Сиверс, В., и Нильсен, Дж. (2013). Создание фабрики платформенных клеток путем разработки метаболизма ацетил-КоА дрожжей. Metab. Англ. 15, 48–54. DOI: 10.1016 / j.ymben.2012.11.002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Fjerbaek, L., Christensen, K. V., and Norddahl, B. (2009). Обзор текущего состояния производства биодизеля с использованием ферментативной переэтерификации. Biotechnol. Bioeng. 102, 1298–1315. DOI: 10.1002 / бит. 22256
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Фортман, Дж., Chhabra, S., Mukhopadhyay, A., Chou, H., Lee, T. S., Steen, E., et al. (2008). Биотопливо, альтернативное этанолу: прокачка микробной скважины. Trends Biotechnol. 26, 375–381. DOI: 10.1016 / j.tibtech.2008.03.008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гитц Р. Д. и Вудс Р. А. (2002). Трансформация дрожжей методом ацетата лития / одноцепочечной ДНК-носителя / полиэтиленгликоля. Methods Enzymol. 350, 87–96. DOI: 10.1016 / S0076-6879 (02) 50957-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гох, Э.-Б., Байду, Э. Э., Бурд, Х., Ли, Т. С., Кислинг, Дж. Д., и Беллер, Х. Р. (2014). Значительные улучшения в производстве метилкетона в E. coli и сведения о пути, полученные в исследованиях in vitro. Metab. Англ. 26, 67–76. DOI: 10.1016 / j.ymben.2014.09.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гольдштейн, А. Л., и Маккаскер, Дж. Х. (1999). Три новых кассеты доминантной лекарственной устойчивости для разрушения гена в Saccharomyces cerevisiae . Дрожжи 15, 1541–1553. DOI: 10.1002 / (sici) 1097-0061 (199910) 15:14 <1541: help-yea476> 3.0.co; 2-k
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гопалакришнан, С., и Маранас, К. (2015b). Достижение анализа метаболического потока для S. cerevisiae в масштабе генома: проблемы, требования и соображения. Метаболиты 5, 521–535. DOI: 10.3390 / metabo5030521
CrossRef Полный текст | Google Scholar
Гопалакришнан, С., и Маранас, К. Д. (2015a). Анализ метаболического потока 13C в масштабе генома. Metab. Англ. 32, 12–22. DOI: 10.1016 / j.ymben.2015.08.006
CrossRef Полный текст | Google Scholar
Хэм, Т. С., Дмитрив, З., Плахар, Х., Чен, Дж., Хиллсон, Н. Дж., И Кизлинг, Дж. Д. (2012). Реализация проекта и практика JBEI-ICE: платформа и инструменты для регистрации биологических компонентов с открытым исходным кодом. Nucleic Acids Res. 40, e141 – e141. DOI: 10.1093 / nar / gks531
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кадихата, С., Matsuda, F., Yoshimi, M., Hayakawa, K., Furusawa, C., Kanda, A., et al. (2015). Анализ метаболического потока Saccharomyces cerevisiae на основе 13C с уменьшенным эффектом крабтри. J. Biosci. Bioeng. 120, 140–144. DOI: 10.1016 / j.jbiosc.2014.12.014
CrossRef Полный текст | Google Scholar
Кислинг, Дж. Д., и Чжоу, Х. (2008). Метаболическая инженерия обеспечивает производство биотоплива нового поколения. Нац. Biotechnol. 26, 298–299. DOI: 10.1038 / nbt0308-298
CrossRef Полный текст | Google Scholar
Кочарин, К., Чен, Ю., Сиверс, В., и Нильсен, Дж. (2012). Разработка метаболизма ацетил-КоА для улучшения производства полигидроксибутирата в Saccharomyces cerevisiae . AMB Exp. 2, 52. DOI: 10.1186 / 2191-0855-2-52
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Козак, Б. У., ван Россум, Х. М., Луттик, М. А. Х., Акройд, М., Бенджамин, К. Р., Ву, Л. и др. (2014). Разработка источника ацетил-кофермента: функциональная экспрессия бактериального пируватдегидрогеназного комплекса в цитозоле Saccharomyces cerevisiae . MBio 5, e1696 – e1614. DOI: 10.1128 / mbio.01696-14
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Криворучко, А., Серрано-Аматриан, К., Чен, Ю., Сиверс, В., и Нильсен, Дж. (2013). Улучшение производства биобутанола в сконструированном Saccharomyces cerevisiae путем изменения метаболизма ацетил-КоА. J. Ind. Microbiol. Biotechnol. 40, 1051–1056. DOI: 10.1007 / s10295-013-1296-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лиан, Дж., Си Т., Наир Н. У. и Чжао Х. (2014). Дизайн и конструирование ацетил-КоА, продуцирующего штаммов Saccharomyces cerevisiae . Metab. Англ. 24, 139–149. DOI: 10.1016 / j.ymben.2014.05.010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мартин, Х. Г., Кумар, В. С., Уивер, Д., Гош, А., Чубуков, В., Мухопадхьяй, А., и др. (2015). Метод ограничения моделей в масштабе генома данными маркировки 13C. PLoS Comput. Биол. 11: e1004363.DOI: 10.1371 / journal.pcbi.1004363
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мо, М. Л., Палссон, Б. О, и Херргорд, М. Дж. (2009). Связь внеклеточных метаболомных измерений с состоянием внутриклеточного потока у дрожжей. BMC Syst. Биол. 3:37. DOI: 10.1186 / 1752-0509-3-37
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Моксли, Дж. Ф., Джуэтт, М. К., Антоневич, М. Р., Виллаш-Боас, С. Г., Альпер, Х., Уиллер, Р. Т., и другие. (2009). Связывание фенотипов метаболического потока с высоким разрешением и регуляции транскрипции в дрожжах, модулируемых глобальным регулятором Gcn4p. Proc. Natl. Акад. Sci. США 106, 6477–6482. DOI: 10.1073 / pnas.08110
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Наик, С., Гоуд, В. В., Рут, П. К., и Далай, А. К. (2010). Производство биотоплива первого и второго поколения: всесторонний обзор. Обновить. Sust. Energ. Ред. 14, 578–597.DOI: 10.1016 / j.rser.2009.10.003
CrossRef Полный текст | Google Scholar
Невойгт, Э., Конке, Дж., Фишер, К. Р., Альпер, Х., Шталь, У., и Стефанопулос, Г. (2006). Разработка кассет замены промотора для точной настройки экспрессии генов в Saccharomyces cerevisiae . заявл. Environ. Microbiol. 72, 5266–5273. DOI: 10.1128 / aem.00530-06
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Папаниколау, С., Шевало, И., Комайтис, М., Марк, И., и Аггелис, Г. (2002). Производство одноклеточного масла путем выращивания Yarrowia lipolytica на промышленном производном животного жира в периодических культурах. заявл. Microbiol. Biotechnol. 58, 308–312. DOI: 10.1007 / s00253-001-0897-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Парк, Дж. М., Ким, Т. Ю., и Ли, С. Ю. (2009). Основанное на ограничениях метаболическое моделирование в масштабе генома для системной метаболической инженерии. Biotechnol.Adv. 27, 979–988. DOI: 10.1016 / j.biotechadv.2009.05.019
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ф. Перес и Б. Э. Грейнджер (2007). IPython: система для интерактивных научных вычислений. Вычисл. Sci. Англ. 9, 21–29. DOI: 10.1109 / mcse.2007.53
CrossRef Полный текст | Google Scholar
Регенберг, Б., Гроткьяер, Т., Винтер, О., Фаусбол, А., Акессон, М., Бро, К. и др. (2006). Гены, регулируемые скоростью роста, оказывают глубокое влияние на интерпретацию профилей транскриптомов у Saccharomyces cerevisiae . Genome Biol. 7, R107. DOI: 10.1186 / GB-2006-7-4-107
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Родригес, С., Денби, К. М., Ву, Т. В., Байду, Э. Е. К., Ван, Г., и Кизлинг, Дж. Д. (2016). АТФ-цитратлиаза, опосредованная цитозольным биосинтезом ацетил-КоА, увеличивает продукцию мевалоната в Saccharomyces cerevisiae . Microb. Cell Fact. 15, 48. DOI: 10.1186 / s12934-016-0447-1
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Рунгупхан, W., и Кислинг, Дж. Д. (2014). Метаболическая инженерия Saccharomyces cerevisiae для производства биотоплива и химикатов на основе жирных кислот. Metab. Англ. 21, 103–113. DOI: 10.1016 / j.ymben.2013.07.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шелленбергер Дж., Парк Дж. О., Конрад Т. М. и Палссон Б. О (2010). BiGG: биохимическая, генетическая и геномная база знаний о крупномасштабных метаболических реконструкциях. BMC Bioinformatics 11: 213.DOI: 10.1186 / 1471-2105-11-213
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Schuetz, R., Kuepfer, L., and Sauer, U. (2007). Систематическая оценка целевых функций для прогнозирования внутриклеточных потоков в Escherichia coli . Мол. Syst. Биол. 3, 119. DOI: 10.1038 / msb4100162
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шиба, Ю., Парадайз, Э. М., Кирби, Дж., Ро, Д.-К., и Кизлинг, Дж. Д. (2007). Разработка обходного пути пируватдегидрогеназы в Saccharomyces cerevisiae для получения изопреноидов высокого уровня. Metab. Англ. 9, 160–168. DOI: 10.1016 / j.ymben.2006.10.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Симс Р. Э., Маби В., Саддлер Дж. Н. и Тейлор М. (2010). Обзор технологий биотоплива второго поколения. Биоресурсы. Technol. 101, 1570–1580. DOI: 10.1016 / j.biortech.2009.11.046
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Стин, Э. Дж., Канг, Ю., Бокинский, Г., Ху, З., Ширмер, А., МакКлюр, А., и другие. (2010a). Микробиологическое производство топлива и химикатов на основе жирных кислот из растительной биомассы. Природа 463, 559–562. DOI: 10.1038 / nature08721
CrossRef Полный текст | Google Scholar
Стин, Э., Канг, Ю., Бокинский, Г., Ху, З., Ширмер, А., МакКлюр, А., и др. (2010b). Микробиологическое производство топлива и химикатов на основе жирных кислот из растительной биомассы. Природа 463, 559–562. DOI: 10.1038 / nature08721
CrossRef Полный текст | Google Scholar
Ван, Х.П., Ван, Д. Дж., И Пронк, Дж. (1998). Влияние удельной скорости роста на ферментативную способность пекарских дрожжей. заявл. Environ. Microbiol. 64, 4226–4233.
Google Scholar
Voeste, T., and Buchold, H. (1984). Производство жирных спиртов из жирных кислот. J. Am. Oil Chem. Soc. 61, 350–352. DOI: 10.1007 / bf02678794
CrossRef Полный текст | Google Scholar
Zhou, Y.J., Buijs, N.A., Zhu, Z., Qin, J., Siewers, V., and Nielsen, J.(2016). Производство олеохимических веществ и биотоплива на основе жирных кислот на фабриках по производству синтетических дрожжевых клеток. Нац. Commun. 7, 11709. DOI: 10.1038 / ncomms11709
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Индонезии не удалось убедить ВТО в споре ЕС о жирных спиртах Reuters
Индонезии не удалось убедить ВТО в споре о жирных спиртах в ЕСЖЕНЕВА (Рейтер). В пятницу комиссия Всемирной торговой организации постановила, что Европейский Союз в значительной степени находится в пределах своих прав налагать антидемпинговые пошлины на индонезийские жирные спирты, отклонив большую часть жалоб Индонезии в торговую организацию в Женеве.
В решении комиссии, которое может быть обжаловано, были отклонены две претензии Индонезии об основании ЕС для применения пошлин, но ЕС был обвинен в не раскрытии результатов проверочного визита индонезийской компании PT Musim Mas.
ЕС ввел демпинговые пошлины на экспорт жирных спиртов Musim Mas и Ecogreen Oleochemicals, но снизил пошлины на продукцию Ecogreen до нуля после судебного разбирательства в Европейском суде.
Жирный спирт производится из косточкового масла, производного пальмового масла, и в основном используется в производстве моющих средств и поверхностно-активных веществ, а также в косметике, пищевых продуктах и промышленных растворителях.
Заявление об ограничении ответственности: Fusion Media напоминает вам, что данные, содержащиеся на этом веб-сайте, не обязательно являются точными и актуальными в реальном времени. Все CFD (акции, индексы, фьючерсы) и цены Forex предоставляются не биржами, а маркет-мейкерами, поэтому цены могут быть неточными и могут отличаться от фактических рыночных цен, то есть цены являются ориентировочными и не подходят для торговых целей. Поэтому Fusion Media не несет никакой ответственности за любые торговые убытки, которые вы можете понести в результате использования этих данных.Fusion Media или любое лицо, связанное с Fusion Media, не несут никакой ответственности за убытки или ущерб в результате использования информации, включая данные, котировки, графики и сигналы покупки / продажи, содержащиеся на этом веб-сайте. Будьте полностью осведомлены о рисках и расходах, связанных с торговлей на финансовых рынках, это одна из самых рискованных форм инвестирования.
Обзор мировой торговли жирными спиртами — Отчет о рынке жирных спиртов
15 января 2018
Мировой торговый дефицит жирных спиртов составил 553 доллара США. млн в 2016 году.Это означает, что мировой торговый баланс показал отрицательное значение в в этом году. Согласно другим источникам, мировой рынок жирных спиртов оценивается в 4,72 миллиарда долларов США в 2017 году и, по прогнозам, достигнет 6,01 доллара США. млрд. к 2022 году при среднегодовом темпе роста 5% в период с 2017 по 2022 год. Производство жирных спирты сильно зависят от сырой нефти, поскольку синтетические жирные спирты произведены из продуктов нефтехимии, которые являются производными сырой нефти. Жирный мировой рынок алкоголя растет за счет увеличения потребления тех же продукт в отраслях промышленности на основе поверхностно-активных веществ и широко используется в развивающейся торговле группы в Азиатско-Тихоокеанском регионе.
Давайте всесторонне посмотрим на глобальный рыночный отчет за 2016 год, включая тенденции рынка, страны-экспортеры, импорт анализ по странам и регионам.
О жирных спиртах Рынок
Жирный спирт используется в различных отраслях промышленности, включая производство мыла. и моющие средства, косметика и средства личной гигиены, жидкости для обработки металлов, ароматизаторы и ароматы. Большинство жирных спиртов в природе находятся в виде восков, которые представляют собой сложные эфиры. с жирными кислотами и жирными спиртами.Растущее потребление жирных спиртов в производстве для индустрии красоты и личной гигиены рынок чистых жирных спиртов в мире. Мировой рынок жирного алкоголя ожидается, что выродится здоровая доля пирога с устойчивым ростом нефтехимическая промышленность во всем мире. Увеличился потребительский спрос на экологически чистые продукты, доступные по цене и превосходные качественный.
Жирный алкоголь в мире Статистика
В последние годы на мировом рынке жиров были отмечены взлеты и падения. пять лет.Рынок упал в 2015 году, зафиксировав наименьшую стоимость как импорт, так и экспорт. Однако жирный спирт, в том числе промышленный монокарбоновые жирные кислоты и кислоты, получаемые при рафинировании, подпадают под код HS Code 3823 . Давай проверим жирное Статистика мирового импорта-экспорта алкоголя 2012-2016 гг.
Год | Экспорт (млн долларов США) | Импорт (млн долларов США) |
2016 | 7497 | 8051 |
2015 | 6749 | 7465 |
2014 | 8199 | 9608 |
2013 | 7756 | 8396 |
2012 | 8417 | 9017 |
ТОП-10 экспортируемых жирных спиртов Страны мира
По данным экспорта жирного спирта, более 100 стран в мир экспортирует жирные спирты.Мировой экспорт жирных кислот составил до 7497 миллионов долларов США в 2016 году. Мировой экспорт жирного спирта увеличился на 11% в стоимостном выражении за 2015-16 гг. Тем не менее, он также вырос на 4% в с 2012 по 2016 год. Индонезия, Малайзия, Нидерланды, Германия, США, Бельгия и Индия — крупнейшие в мире жирные спирты. экспортеры.
Индонезия и Малайзия вместе представляют 55% мировой экспорт этого продукта. Экспорт жирного алкоголя из Индонезии составил $ 2328 млн. И экспортные продажи этого продукта увеличились на 27% в пересчете на стоимость в течение 2015-16 гг.Экспорт жирного алкоголя из Малайзии составил 1821 миллион долларов США. в 2016 г. и экспортные продажи увеличились на 10% в стоимостном выражении в 2015–16 гг.
Страна | Стоимость (в миллионах долларов США) | Стоимость акций (%) |
Индонезия | 2328 | 31.1 |
Малайзия | 1821 | 24,3 |
Нидерланды | 699 | 9,3 |
Германия | 668 | 8.9 |
США | 412 | 5,5 |
Бельгия | 294 | 3,9 |
Индия | 163 | 2.2 |
Великобритания | 147 | 2,0 |
Таиланд | 101 | 1,4 |
Южная Африка | 93 | 1.2 |
* Приведенная выше статистика основана на отчете
за 2016 год.Вы ищете экспортеров жирного спирта в других странах? страны? Export Genius предоставляет отчет о сделках, включая список активных экспортеры в любой конкретной стране мира. Вы сможете узнать торговую деятельность этих поставщиков и выберите правильного делового партнера для вашего продукта. Кроме того, поиск по всему миру данные о торговле любого конкретного продукта для справки.
Топ 10 жирных спиртов Страны-импортеры в мире
Согласно отчету о торговле жирным алкоголем, в мире более 150 стран импортируют этот продукт. Мировой импорт жирного спирта составил 8051 миллион долларов США в течение 2016 года, а общий объем импорта этого продукта увеличился на 8% в течение 2015-16 гг. Китай, Нидерланды, США, Германия, Сингапур, Малайзия и Индия являются крупнейшими импортерами жирного алкоголя в мире. Китай Импорт жирного спирта составил 1098 миллионов долларов США и составил 13.6% от всего в 2016 году. В приведенной ниже таблице указаны 10 самых жирных алкогольных напитков. стран-импортеров в мире с их стоимостью и долей рынка, зарегистрированными в 2016.
Страна | Стоимость (в миллионах долларов США) | Стоимость акций (%) |
Китай | 1098 | 13.6 |
Нидерланды | 697 | 8,7 |
США | 573 | 7,1 |
Германия | 555 | 6.9 |
Сингапур | 504 | 6,3 |
Малайзия | 495 | 6,2 |
Индия | 402 | 5.0 |
Корея | 354 | 4,4 |
Бельгия | 299 | 3,7 |
Япония | 264 | 3.3 |
* Приведенная выше статистика основана на отчете
за 2016 год.Хотите ли вы поставлять продукцию из жирного спирта в другие страны для расширения вашего бизнеса? Это зависит от поиска реальных покупателей на мировом рынке. Обратитесь к потенциальным рынкам и найдите актуальные импортеры для вашего продукта. Данные о мировой торговле жирным алкоголем подготовлены компанией Export Genius охватывает список импортеров жирных спиртов, которые помогут вам отфильтровать список и выберите правильных деловых партнеров в соответствии с вашими требованиями.
Крупнейшие мировые регионы торговли жирным алкоголем
Ключевыми региональными рынками, изученными в отчете, являются Азия. Тихий океан, Азия, Европа и Америка. Азиатско-Тихоокеанский регион продолжит доминировать рынок на протяжении всего прогнозного периода. Рост региона также может быть объясняется растущим спросом на мыло, моющие и косметические средства. Азия Тихоокеанский регион является крупнейшим в мире рынком и регионом для этого продукта. По жирному статистика торговли алкоголем, экспорт из Азиатско-Тихоокеанского региона составил 4859 миллионов долларов США и Импорт этого продукта в 2016 году составил 4036 миллионов долларов США.Здесь мы предоставляем данные о торговле жирным алкоголем в четырех регионах мира.
Регион | Экспорт (млн долларов США) | Импорт (млн долларов США) |
Азиатско-Тихоокеанский регион | 4859 | 4036 |
Азия | 4623 | 3835 |
Европа | 2191 | 3041 |
Америка | 542 | 990 |
* Приведенная выше статистика основана на отчете
за 2016 год.Подписаться на Fatty Отчет о торговле алкоголем
Отчет о мировой торговле жирным алкоголем, подготовленный Export Genius фокусируется на отраслевом анализе, профилях компаний, списке импортеров и экспортеров, анализ глобального региона и полное представление о конкурентных пейзаж.Вот образец экспорта жирных масел из США для справки. Это включает основные поля данных, которые мы рассматриваем в нашем торговом отчете.
Дата | 28 августа 2016 |
Страна назначения | Китай |
Страна происхождения | США |
Порт отправления | Порт Лонг-Бич, Лонг-Бич, Калифорния |
Порт прибытия | Шанхай |
Грузоотправитель | Контейнерная линия Helvetia |
Адрес отправителя | 16701 Гринс пойнт Парк Др., # 300 Хьюстон, Техас 77060 |
Описание продукта | жирных спиртов Alfol * 8 Alcohol HTS Код: 2905.16.00.50 (без тумана) Вес нетто. 10176 KLG DDC входит в состав морских перевозок. |
Кол. Акций | 64 |
Блок | Барабаны |
Масса | 11648 сом |
Судно | Балтиморский мост |
Объем мирового рынка жирных спиртов представлен в По цене и количеству.Объем рынка определяется количественным стандартом. единиц и общая сумма в основном в долларах США.
Вы можете получить индивидуальный отчет в соответствии с вашими требованиями который анализируется на основе товарных сегментов, целевых рынков, таких как торговые страны, импортеры, экспортеры и другие ресурсы. Вы можете анализировать возможности рынка жирного алкоголя на региональном и глобальном уровне.
Этот отчет направлен на оценку размера рынка и будущего рост рынка на разных ресурсах по типу, региону и применение.Отчет включает углубленное исследование и анализ рынка. ключевые игроки и быстрорастущие сегменты рынка жирных спиртов.
Чтобы купить наш отчет и данные по исследованию рынка, отправьте электронное письмо нам по адресу [email protected] .
По любым вопросам, связанным со СМИ, пожалуйста, свяжитесь с нами по адресу [email protected] .
ВЫСОКИЙ ЖИРНЫЙ СПИРТ | CAMEO Chemicals
Химический лист данных
Химические идентификаторы | Опасности | Рекомендации по ответу | Физические свойства | Нормативная информация | Альтернативные химические названияХимические идентификаторы
В Поля химического идентификатора включать общие идентификационные номера, NFPA алмаз U.S. Знаки опасности Министерства транспорта и общие описание химического вещества. Информация в CAMEO Chemicals поступает из множества источники данных.| Номер CAS | Номер ООН / NA | Знак опасности DOT | USCG CHRIS Код |
|---|---|---|---|
| никто | данные недоступны | ||
| Карманный справочник NIOSH | Международная карта химической безопасности | ||
| никто | никто | ||
NFPA 704
данные недоступны
Общее описание
Восково-белое твердое вещество с легким мыльным запахом.Плавает по воде. (USCG, 1999)
Опасности
Оповещения о реактивности
никто
Реакции воздуха и воды
Нерастворим в воде.
Пожарная опасность
Нет доступной информации.
Опасность для здоровья
Материал практически не токсичен. Попадание в глаза или продолжительный контакт с кожей может вызвать легкое раздражение. (USCG, 1999)
Профиль реактивности
Бромистый ацетил бурно реагирует со спиртами или водой [Merck, 11-е изд.1989]. Смеси спиртов с концентрированной серной кислотой и сильной перекисью водорода могут вызвать взрыв. Пример: Взрыв произойдет, если диметилбензилкарбинол добавить к 90% перекиси водорода, а затем подкисить концентрированной серной кислотой. Смеси этилового спирта с концентрированной перекисью водорода образуют мощные взрывчатые вещества. Смеси перекиси водорода и 1-фенил-2-метилпропилового спирта имеют тенденцию к взрыву при подкислении 70% -ной серной кислотой [Chem. Англ. Новости 45 (43): 73. 1967; J, Org.Chem. 28: 1893. 1963]. Алкилгипохлориты очень взрывоопасны. Их легко получить при взаимодействии хлорноватистой кислоты и спиртов либо в водном растворе, либо в смешанных растворах водно-четыреххлористого углерода. Хлор плюс спирты аналогичным образом дают алкилгипохлориты. Они разлагаются на холоде и взрываются под воздействием солнечного света или тепла. Третичные гипохлориты менее нестабильны, чем вторичные или первичные гипохлориты [NFPA 491 M 1991]. Катализируемые основаниями реакции изоцианатов со спиртами следует проводить в инертных растворителях.Такие реакции в отсутствие растворителей часто происходят с взрывной силой [Wischmeyer 1969].
Принадлежит к следующей реактивной группе (группам)
Потенциально несовместимые абсорбенты
Соблюдайте осторожность: жидкости с этой классификацией реактивной группы известно реагировать с абсорбент перечислено ниже. Дополнительная информация о абсорбентах, включая ситуации, на которые следует обратить внимание …
- Абсорбенты на основе целлюлозы
Ответные рекомендации
В Поля рекомендаций ответа включать расстояния изоляции и эвакуации, а также рекомендации по пожаротушение, противопожарное реагирование, защитная одежда и первая помощь.В информация в CAMEO Chemicals поступает из различных источники данных.Изоляция и эвакуация
Нет доступной информации.
Пожарная
Средства пожаротушения, которые нельзя использовать: Вода может быть неэффективной.Средства пожаротушения: сухой химикат, пена, двуокись углерода (USCG, 1999)
Непожарное реагирование
Нет доступной информации.
Защитная одежда
Очки или маска для лица; резиновые перчатки.(USCG, 1999)
Ткани для костюмов DuPont Tychem®
Нет доступной информации.
Первая помощь
ГЛАЗА: промыть водой; если раздражение не проходит, обратитесь к врачу.КОЖА: стереть, промыть водой с мылом. (USCG, 1999)
Физические свойства
Химическая формула: данные недоступны
Точка возгорания: выше 270 ° F (USCG, 1999)
Нижний предел взрываемости (НПВ): данные недоступны
Верхний предел взрываемости (ВПВ): данные недоступны
Температура самовоспламенения: данные недоступны
Температура плавления: 127 ° F (USCG, 1999)
Давление пара: данные недоступны
Плотность пара (относительно воздуха): данные отсутствуют
Удельный вес: 0.81 год при 77 ° F (USCG, 1999)
Точка кипения: выше 480 ° F при 760 мм рт. (USCG, 1999)
Молекулярный вес: 262 (средн.) (USCG, 1999)
Растворимость в воде: данные отсутствуют
Потенциал ионизации: данные недоступны
IDLH: данные недоступны
AEGL (рекомендуемые уровни острого воздействия)
Нет доступной информации AEGL.ERPGs (Руководство по планированию действий в чрезвычайных ситуациях)
Информация по ERPG отсутствует.PAC (Критерии защитного действия)
Информация о PAC недоступна.Нормативная информация
В Поля нормативной информации включать информацию из Сводный список раздела III Агентства по охране окружающей среды США Списки, химический объект Министерства внутренней безопасности США Стандарты борьбы с терроризмом, и Управления по охране труда и здоровья США Стандартный список управления производственной безопасностью особо опасных химических веществ (подробнее об этих источники данных).Сводный список списков Агентства по охране окружающей среды
Нет нормативной информации.Стандарты по борьбе с терроризмом химического предприятия DHS (CFATS)
Нет нормативной информации.Список стандартов управления безопасностью процессов (PSM) OSHA
Нет нормативной информации.Альтернативные химические названия
В этом разделе представлен список альтернативных названий этого химического вещества, включая торговые наименования и синонимы.
- СПИРТ ВЫСШЕГО ЖИРНОГО
- СТИРИЛОВЫЙ СПИРТ СЫРОЙ
- ВЫСОКИЙ ЖИРНЫЙ СПИРТ
Потребление алкоголя по странам 2020
Алкоголь — это регулируемый наркотик.Он сделан из зерен, овощей или фруктов, подвергнутых ферментации, когда дрожжи или бактерии вступают в реакцию с сахарами в пище, в результате чего образуются этанол и диоксид углерода. Пиво и вино — это ферментированные спирты. Спиртные напитки проходят дополнительный процесс дистилляции, в ходе которого удаляется часть воды, в результате чего концентрация спирта выше и аромат.
Алкоголь классифицируется как депрессант, поскольку он замедляет двигательные функции, время реакции и речь. Алкоголь, употребляемый в небольших количествах, например стакан пива или вина, часто используется для «расслабления» и оказывает более стимулирующий эффект.При употреблении в больших количествах начнут проявляться депрессивные эффекты.
В Соединенных Штатах «напиток» содержит 0,6 унции чистого алкоголя. «Напитком» считается:
- 12 унций пива
- 8 унций солодового ликера
- 5 унций вина
- 1,5 унции 80-процентного (содержание алкоголя) спирта или ликера
Чрезмерное употребление алкоголя включает чрезмерное употребление алкоголя и запой. Пьянство определяется как восемь или более порций в неделю для женщин и 15 или более порций в неделю для мужчин.Пьянство — это за один раз четыре или более порций для женщин и пять или более порций для мужчин.
Хотя периодическое употребление алкоголя считается безвредным, чрезмерное употребление может привести к ряду осложнений для здоровья. Алкоголь может оказывать неблагоприятное воздействие на сердце, включая высокое кровяное давление, инсульт, аритмию и кардиомиопатию. В печени может наблюдаться стеатоз (ожирение печени), алкогольный гепатит, фиброз и цирроз. Кроме того, употребление алкоголя связано с раком головы и шеи, раком пищевода, раком печени, раком груди и колоректальным раком.Алкоголизм — это хроническое заболевание, характеризующееся чрезмерным употреблением алкоголя и чрезмерным употреблением алкоголя.
Алкоголь регулируется такими законами, как минимальный возраст употребления алкоголя (чаще всего 18 или 21 год, но зависит от страны), ограничение открытого ношения за пределами заведений, требование лицензирования спиртных напитков для ресторанов и магазинов и запрет на использование транспортных средств в нетрезвом виде.
Потребление алкоголя в каждой стране сильно различается и зависит от законов, культуры и других особенностей каждой страны.Alcohol.org нашел потребление пива, вина и спиртных напитков на душу населения в каждой стране и пересчитал эти цифры в потребление чистого алкоголя для каждого из этих напитков. Например, одна ручка водки (1,75 литра) — это около 300 миллилитров чистого спирта.
Беларусь потребляет больше всего алкоголя в мире — 14,4 литра на человека в год. Это примерно 48 ручек водки на человека в год. Хотя Министерство здравоохранения Беларуси опровергло эти цифры, правительство ввело постановления, ограничивающие производство, продажу и рекламу алкоголя.К ним относятся ужесточение наказания за вождение в нетрезвом виде, повышение цен на алкоголь и повышение минимального возраста для употребления алкоголя до 21 года. Большинство стран из первой десятки находятся в Европе.
В США годовое потребление чистого алкоголя составляет 8,7 литров на человека, но потребление варьируется в зависимости от штата. Это выше среднего мирового показателя (8,3), но ставит Соединенные Штаты на 25-е место. Минимальный возраст употребления алкоголя в Соединенных Штатах — 21 год, и его соблюдение строго соблюдается.
.