Законы электролиза Фарадея и их применение для расчета количественных характеристик процесса электролиза
Электролизомназывается совокупность электрохимических окислительно-восстановительных реакций, протекающих на электродах при прохождении постоянного электрического тока через раствор или расплав электролита. При этом на катоде происходит процесс восстановления, а на аноде – окисления. Катионы восстанавливаются в ионы более низкой степени окисления или в атомы, например:
Fe3+ + e – → Fe2+ ; (3.54)
Cu2+ + 2 e – → Cu. (3.55)
Нейтральные
молекулы могут участвовать в превращениях
на катоде непосредственно или
взаимодействовать с продуктами катодного
процесса, которые рассматриваются в
этом случае как промежуточные вещества.
2 H2O + 2 e – → H2 + 2 OH–. (3.56)
На аноде окисляются ионы или молекулы, поступающие из объема электролита, например:
4 OH– – 4 e – → 2 H2O + H2; (3.57)
2 Cl– – 2 e – → Cl2,– (3.58)
или принадлежащие материалу анода. в последнем случае анод растворяется, например:
Cu – 2 e – → Cu2+
(растворение медного анода). (3.59)Протекание
электродных реакций зависит от состава
и концентрации электролита, материала
электродов, электродного потенциала,
температуры, гидродинамических условий.
Процессы электролиза описываются законами Фарадея, которые в объединенной форме читаются следующим образом: массы веществ, испытавших электрохимические превращения на электродах, прямо пропорциональны количеству протекшего через электролит электричества и электрохимическим эквивалентам этих веществ:
(3.60)
где m – масса вещества, превратившегося на электроде (выделившегося на электроде),
электрохимический эквивалент – величина характеризующая массу продуктов электролиза, выделившихся на электродах при прохождении через электролит 1 Кл электричества;
q – количество прошедшего электричества, Кл;
F – число Фарадея (96485 Кл/г-экв) – количество
электричества, необходимое для химического
превращения (выделения на электроде) 1
г-экв вещества.
Так как q = I · τ (I – сила тока, А; τ – продолжительность электролиза, с), то уравнение закона Фарадея может быть записано следующим образом:
(3.61)
Химический эквивалент вещества (эквивалентная масса вещества) при окислительно-восстановительном превращении рассчитывается по формуле:
, (3.62)
где М– молярная масса вещества, претерпевающего превращение на электроде, г/моль;
n– количество электронов, участвующих в одном акте химического превращения.
При
электрохимических процессах часто
наблюдаются отклонения от законов
Фарадея: масса действительно полученного
или разложившегося продукта не
соответствует теоретической. Эти
отклонения – кажущиеся и возникают за
счет одновременного протекания побочных
электрохимических процессов; химических
реакций, в которые вступает продукт;
потерь продукта и потерь электроэнергии
на преодоление сопротивления электролизера. Эффективность электрохимического
процесса оценивается выходом
по току Вт:
Эффективность электрохимического
процесса оценивается выходом
по току Вт:
(3.63)
Эта величина может быть выражена в процентах:
. (3.64)
Тогда практическое количество вещества, образующееся при электролизе рассчитывается по формуле:
. (3.65)
П р и м е р 3.18. Какое количество алюминия выделится при электролизе за время 12 ч, если сила тока I =2,5 A, а выход по току составляет 88 %. Молярная масса алюминия М, равная его грамм-атомной массе А, составляет 26,98 г/моль.
Р е ш е н и е
Выделение алюминия при электролизе происходит на катоде при прохождении следующей реакции восстановления:
Al3+ + 3 e – = Al; n = 3.
Химический эквивалент алюминия
рассчитываем по формуле (3. 62):
62):
Э = М / 3 = 26,98 / 3 = 8,99 г/экв.
Продолжительность электролиза τ = 12 час = 12 · 3600 = 43200 с.
По объединенному закону Фарадея (3.61) находим теоретическое количество алюминия, выделяющееся при электролизе в указанных условиях:
г.
Практическое количество выделившегося при электролизе алюминия находим с учетом величины ВТ по формуле (3.65):
П р и м е р 3.19. Определить время, необходимое для выделения при электролизе 1,2 г меди, если сила тока I = 2 A, а выход по току ВТ = 96 %.
Р е ш е н и е
На основании формулы (3.64) находим, на какое теоретическое количество меди необходимо рассчитывать продолжительность электролиза:
Выделение меди при электролизе происходит на катоде при прохождении следующей реакции восстановления:
Сu2+ + 2 e–

Химический эквивалент меди рассчитываем по формуле (3.62):
Э = М / 2 = 63,54 / 2 = 31,77 г/экв.
Из уравнения закона Фарадея (3.61) находим время процесса:
Законы электролиза Фарадея
Первый закон Фарадея
Как уже известно, при электролизе на электродах происходит выделение вещества. Попробуем выяснить, от чего будет зависеть масса это вещества. Масса выделившегося вещества m будет равна произведению массы одного иона m0i на число ионов Ni, которые достигли электрода за промежуток времени равный ∆t: m = m0i*Ni. Масса иона m0i будет вычисляться по следующей формуле:
где М — молярная масса вещества, а Na — постоянная Авогадро.
Число ионов, которые достигнут электрода, вычисляется по следующей формуле:
где ∆q = I*∆t — заряд, прошедший через электролит за время, равное ∆t, q0i — заряд иона.
Для того, чтобы определить заряд иона, используется следующая формула:
где n — валентность, e — элементарный заряд.
Собирая воедино все представленные формулы, получаем формулу для вычисления массы выделившегося на электроде вещества:
Теперь обозначим через k коэффициент пропорциональности между массой вещества и зарядом ∆q.
Этот коэффициент k будет зависеть от природы вещества. Тогда формулу массы вещества можно переписать в следующем виде:
Второй закон Фарадея
Масса вещества, выделившегося на электроде за время, равное ∆t, при прохождении электрического тока пропорциональна силе тока и времени. Коэффициент k называют электрохимическим эквивалентом данного вещества. Единицей измерения служит кг/Кл. Разберемся с физическим смыслом электрохимического эквивалента. Так как:
то формулу электрохимического эквивалента можно переписать в следующем виде:
Таким образом, k — отношение массы иона к заряду этого иона.
Для того, чтобы удостовериться в справедливости закона Фарадея, можно провести опыт. Лабораторная установка, необходимая для него, показана на следующем рисунке. (-19) Кл.
(-19) Кл.
Именно таким способом было впервые получено значение элементарного электрического заряда.
Нужна помощь в учебе?
Предыдущая тема: Электрический ток в жидкостях: ионная проводимость и электролиз
Следующая тема:   Электрический ток в газах: опыт и проводимость газа
Законы электролиза Фарадея | Физика. Закон, формула, лекция, шпаргалка, шпора, доклад, ГДЗ, решебник, конспект, кратко
В 1833 г. М. Фарадей установил:
Масса вещества, которое выделяется при прохождении электрического тока в электролитах на аноде или катоде, прямо пропорциональна заряду, который при этом переносится ионами через электролит:
m = kq,
где m — масса вещества, кг; q — заряд, Кл.
Коэффициент пропорциональности k = m / q называется электрохимическим эквивалентом данного вещества.
Электрохимический эквивалент вещества показывает, какая масса вещества в килограммах выделяется на электроде при прохождении тока, переносящего заряд, равный одному кулону:
k = m / q
Если иметь в виду, что при постоянном токе в цепи q = IΔt, где I — сила тока (ампер), а Δt — время прохождения тока (секунд), то закон Фарадея можно записать в виде
Исходя из современных представлений, закон для электролиза можно установить теоретически. Пусть за время Δt через электролит переносится заряд q. Заряд одного иона q0i = ne, где n — валентность иона, а e — значение элементарного электрического заряда. Следовательно, q = neNi, где Ni — количество ионов, которые достигли электрода.
Следовательно, q = neNi, где Ni — количество ионов, которые достигли электрода.
С другой стороны, масса вещества, выделяющегося на электроде m = m0iNi, где m0i — масса иона, которая может быть определена по молярной массе вещества M и постоянной Авогадро NA:
m0i = M / NA; m = (M / NA) • Ni.
Из уравнения для заряда q = neNi можно определить Ni: Ni = q / ne. Подставив значения Niв выражение для массы, получаем:
m = (M / neNA) • q,
что также является законом Фарадея для электролиза. Итак, электрохимический эквивалент вещества
Итак, электрохимический эквивалент вещества
k = M / neNA,
где все величины для данного вещества являются постоянными.
В последней формуле значение элементарного заряда e и постоянная Авогадро одинаковы для всех веществ. Их произведение назвали постоянной Фарадея:
F = eNA.
Значение постоянной Фарадея:
F = 1,6 • 10-19 Кл • 6,023 • 1023 моль-1 = -9,65 • 104 Кл/моль.
Теперь для электрохимического эквивалента вещества имеем Материал с сайта http://worldofschool.ru
k = (1 / F) • (M / n),
что и является вторым законом для электролиза.
Второй закон электролиза. Электрохимические эквиваленты веществ прямо пропорциональны массам их молей и обратно пропорциональны их валентностям.
Электрохимические эквиваленты веществ прямо пропорциональны массам их молей и обратно пропорциональны их валентностям.
Чтобы удобно было решать многие задачи, оба закона можно объединить в одном выражении (объединенный закон электролиза):
m = (1 / F) • (M / n) • q,
или
m = (1 / F) • (M / n) • IΔt.
На этой странице материал по темам:Закон електролізу формула
Напишите формулу объединенного закона фарадея для электролиза
Электролиз закон фарадея реферат по теме
Формула и формулировка законов фарадея для электролиза
Сформулируйте и запишите формулу первого закона фарадея для электролиза?
Сформулируйте закон Фарадея для электролиза, запишите его формулу.

Запишите формулы объединенного закона электролиза.
Что такое постоянная Фарадея?
Репетитор-онлайн — подготовка к ЦТ
Пример 19. К зажимам электролитической ванны, предназначенной для никелирования изделий, подведено напряжение 1,8 В. Ванна заполнена раствором электролита сопротивлением 3,7 Ом. В процессе электролиза на электродах выделяется двухвалентный никель с молярной массой 59 г/моль, плотность никеля составляет 8,9 г/см3. В раствор помещают некоторое изделие с площадью поверхности 1,2 дм2. Рассчитать, за какое время изделие покроется слоем никеля толщиной 30 мкм. Какая энергия будет израсходована при этом?
Решение. 1. Воспользуемся обобщенным законом Фарадея для электролиза:
m=1F⋅AnIt,
где m — масса никеля, выделившегося на поверхности изделия; A — атомная масса никеля (совпадает с молярной массой, так как никель является одноатомным), A = 59 г/моль; F — постоянная Фарадея, F = 9,65 ⋅ 104 Кл/моль; n — валентность никеля, n = 2; I — сила тока в электролитической ванне; t — время никелирования изделия.
Из данного закона следует, что для расчета времени никелирования изделия
t=nmFAI
необходимо знать силу тока в электролите и массу выделившегося никеля.
Силу тока найдем из закона Ома для участка цепи:
I=UR,
где U — напряжение на зажимах ванны, U = 1,8 В; R — сопротивление электролита, R = 3,7 Ом.
Массу определим с помощью произведения:
m = ρV = ρSh,
где ρ — плотность никеля, ρ = 8,9 г/см3; V — объем никеля, выделившегося на поверхности изделия, V = Sh; S — площадь поверхности изделия, S = 1,20 дм2; h — толщина покрытия, h = 30 мкм.
Подставим выражения для I и m в формулу, определяющую время никелирования изделия:
t=nρShFRAU,
и рассчитаем искомое время:
t=2⋅8,9⋅103⋅1,2⋅10−2⋅30⋅10−6⋅9,65⋅104⋅3,759⋅10−3⋅1,8=6,0 ч.
2. При электролизе расходуется энергия, которую можно найти по формуле
E=U2Rt,
или с учетом формулы для времени никелирования —
E=U2RnρShFRAU=UnρShFA.
Выполним расчет:
E=1,8⋅2⋅8,9⋅103⋅1,2⋅10−2⋅30⋅10−6⋅9,65⋅10459⋅10−3=19 кДж.
Для покрытия изделия слоем никеля указанной толщины требуется 6,0 ч; при этом расходуется электроэнергия 19 кДж.
Законы Фарадея в физике
Законы электролиза
При прохождении электрического тока через электролиты происходит процесс разложения вещества, который называют электролизом. При этом проводники, которые погружены в раствор, называют анодом (положительный электрод) и катодом (отрицательный электрод).
При помощи электролиза получают различные вещества, например, хлор, фтор, щелочи и т.д. При помощи данного процесса производят переработку сырья, которое содержит металлы, очищают металлы. Используя процессы электролиза, наносят тонкие металлические покрытия на разные металлические поверхности.
Формулировка первого закона Фарадея
Масса вещества, которое выделяется на электроде, прямо пропорциональна заряду, который прошел через электролит. В виде формулы данный закон можно представить как:
В виде формулы данный закон можно представить как:
где — полный заряд, который проходит через электролит, за времяt. — сила тока. — коэффициент пропорциональности (электрохимический эквивалент вещества ()), равный массе вещества, которая выделится при прохождении через электролит заряда равного 1 Кл. Величина является характеристикой вещества.
Первый закон для электролиза был получен Фарадеем экспериментально.
Формулировка второго закона Фарадея
Электрохимический эквивалент пропорционален молярной массе вещества () и обратно пропорционален величине его химической валентности (). В математическом виде второй закон Фарадея записывают как:
где Кл/моль — постоянная Фарадея, полученная эмпирически. Величину называют химическим эквивалентом вещества, она показывает, какая масса вещества требуется для замещения одного моля водорода в химических соединениях.
Иногда второй закон Фарадея формулируют так:
Электрохимические эквиваленты веществ пропорциональны их химическим эквивалентам.
Второй закон Фарадея также относят к эмпирическим законам.
Объединенный закон Фарадея для электролиза
Объединенный закон Фарадея записывают в виде:
Физический смысл выражения (3) заключен в том, что постоянная Фарадея количественно равна заряду, который следует пропустить через всякий электролит для того, чтобы на электродах выделилось вещество в количестве, равном одному химическому эквиваленту.
Примеры решения задач
Законы электролиза Фарадея • Джеймс Трефил, энциклопедия «Двести законов мироздания»
При электролизе масса превращенного вещества прямо пропорциональна количеству электричества, прошедшего через электролитическую ячейку.
При прохождении через электролит одного и того же количества электричества масса превращенного вещества зависит от массы и заряда ионов вещества.
Два закона электролиза — это всего лишь небольшая часть вклада Майкла Фарадея в науку. Электролиз — это совокупность процессов, происходящих при пропускании электрического тока через электролит — плавленое ионное вещество (например, плавленая соль) или раствор, в котором присутствуют ионы. Электрический ток проходит через электролит от одного электрода к другому. Положительно заряженные ионы при этом движутся к отрицательному электроду, катоду, а отрицательно заряженные — к положительному электроду, аноду. Химические реакции происходят на электродах. Фарадей провел фундаментальные исследования электролитов и создал законы, в которых говорится, что химические превращения связаны с потоком электронов (то есть электрическим током): чем больше электронов, тем больше химических превращений.
Электрический ток проходит через электролит от одного электрода к другому. Положительно заряженные ионы при этом движутся к отрицательному электроду, катоду, а отрицательно заряженные — к положительному электроду, аноду. Химические реакции происходят на электродах. Фарадей провел фундаментальные исследования электролитов и создал законы, в которых говорится, что химические превращения связаны с потоком электронов (то есть электрическим током): чем больше электронов, тем больше химических превращений.
Электролиз — это важный промышленный процесс, используемый как при получении определенных металлов, так и при конечной обработке поверхностей методом нанесения гальванического покрытия. Примером электролиза в действии может быть электролитическое рафинирование меди после ее выделения из руды. Выступающие в качестве катода тонкие листы чистой меди опускают в электролит, содержащий раствор сульфата меди и серную кислоту, а слитки неочищенной меди подвешивают в этом же растворе, и они действуют как анод. При пропускании электрического тока анод начинает растворяться, и ионы меди, вместе с некоторым количеством ионов железа и цинка, поступают в электролит. Остальные спутники меди, содержавшиеся в слитках (включая значительное количество серебра, золота и платины), выпадают в осадок и накапливаются на дне электролитической ванны. Ионы меди через электролит направляются к катоду и осаждаются на нем. Цинк и железо остаются в растворе.
При пропускании электрического тока анод начинает растворяться, и ионы меди, вместе с некоторым количеством ионов железа и цинка, поступают в электролит. Остальные спутники меди, содержавшиеся в слитках (включая значительное количество серебра, золота и платины), выпадают в осадок и накапливаются на дне электролитической ванны. Ионы меди через электролит направляются к катоду и осаждаются на нем. Цинк и железо остаются в растворе.
В промышленных масштабах в подобных ваннах за месяц можно очистить всего несколько тонн меди, но при этом получается продукт 99,96-процентной чистоты. Более того, благодаря извлечению из осадка благородных металлов окупается весь процесс очистки. Кроме меди, электролитическим методом в промышленных масштабах очищаются также магний, натрий и алюминий.
В описанном выше процессе рафинирования меди атом меди переходит в электролит в виде иона, теряя два электрона. Следовательно, на аноде он принимает два электрона, и ион снова превращается в нейтральный атом меди (можно представить себе, что эти два электрона бегут по проводу, как электрический ток). Согласно первому закону Фарадея, для того чтобы очистить в два раза больше меди, необходимо в два раза больше электронов.
Согласно первому закону Фарадея, для того чтобы очистить в два раза больше меди, необходимо в два раза больше электронов.
Электролиты, закон Фарадея
Электролиты
Определение 1
Явление выделения электрическим током химических составных частей проводника при прохождении тока называется электролизом.
Электролиз может протекать не во всех проводниках. К числу проводников, в которых электролиз не протекает, относят металлы, уголь и другие соединения (Это проводники первого рода). Проводники, в которых электролиз возможен, называют проводниками второго рода или электролитами. К электролитам относят большое количество водных растворов кислот, солей, некоторые жидкие и твердые соединения.
Явление электролиза часто сопровождается химическими реакциями (вторичные реакции), которые не связаны с прохождением тока. В ходе электролиза на отрицательном полюсе (катоде) всегда выделяются металлы и водород, на положительном полюсе (аноде) — остаток химического соединения. Составные части электролита выделяются только на электродах. Явление выделения составных частей электролита на электродах при прохождении электрического тока было исследовано М. Фарадеем.
Составные части электролита выделяются только на электродах. Явление выделения составных частей электролита на электродах при прохождении электрического тока было исследовано М. Фарадеем.
Готовые работы на аналогичную тему
Законы электролиза Фарадея не стоит путать с законом электромагнитной индукции Фарадея, рассматривающим электрический контур и силы в нём. В этом законе говорится о зависимости ЭДС от скорости изменения магнитного потока.
Явление электролиза отражает тот факт, что молекулы растворенного вещества в электролите существуют как две части: ион с положительным знаком и ион с отрицательным знаком. Под воздействием внешнего электрического поля эти ионы движутся: положительные ионы в сторону катода, отрицательные ионы в сторону анода. Таким образом, когда отрицательный ион достигнет анода, то он отдает свой заряд электроду, что ведёт к изменению его заряда. Следовательно, некоторое количество электронов проходят по внешней цепи. Ион становится нейтральным и выделяется на аноде, как атом или молекула. Положительный ион забирает у катода некоторое количество электронов (столько, сколько ему требуется для нейтрализации), что порождает его выделение на катоде.
Положительный ион забирает у катода некоторое количество электронов (столько, сколько ему требуется для нейтрализации), что порождает его выделение на катоде.
Замечание 1
Ионы, знак заряда при которых отрицательный, выделяются на аноде, они были названы Фарадеем анионами, а положительно заряженные ионы получили название катионов.
Законы Фарадея
Фарадей установил экспериментальным путем два основных закона электролиза. В соответствии с первым законом, масса вещества $(m)$, которая выделяется на одном из электродов, прямо пропорциональна заряду $(q)$, который прошел через электролит:
$m=Kq\left(1\right),$
где $K$ — электрохимический эквивалент, который отличается для разных электролитов. $K$ равен массе электролита, которая выделяется при прохождении заряда $q=1Kл$. Основной единицей измерения электрохимического коэффициента является $\frac{кг}{Кл}$.
Кроме того, Фарадей заметил, что электрохимический эквивалент всегда пропорционален молярной массе вещества ($\mu $) и обратно пропорционален валентности $(Z)$. 4\frac{Кл}{моль}$ — фундаментальная физическая постоянная, отражающая отношение электрохимических и физических свойств вещества. Причем известно, что:
4\frac{Кл}{моль}$ — фундаментальная физическая постоянная, отражающая отношение электрохимических и физических свойств вещества. Причем известно, что:
$F=q_eN_A\left(4\right),$ где:
- $q_e$ — заряд электрона,
- $N_A$ — постоянная Авогадро.
Объяснить законы Фарадея можно с точки зрения ионной проводимости. Допустим, что количество ионов, которое выделяется на одном из электродов при электролизе равно $\nu $, заряд одного из ионов равен $q_1$. Следовательно, суммарный заряд, который прошел через электролит, на который действовало внешнее электрическое поле, равен:
$q=q_1\nu \left(5\right).$
Пусть масса одного иона равна $m_1$, тогда масса вещества, которая выделяется на электроде, равна:
$m=m_1\nu \left(6\right).$
Выразим из (5) $\nu $, получим:
$\nu =\frac{q}{q_1}\left(7\right).$
Подставим (7) в (6), имеем:
$m=\frac{m_1}{q_1}q\left(8\right).$
Выражение (8) не что иное как первый закон Фарадея, где:
$K=\frac{m_1}{q_1}=\frac{m_1N_A}{q_1N_A}=\frac{\mu }{q_1N_A}\left(9\right). $
$
Сравним выражения (2) и (9), получим, что:
$q_1=\frac{ZF}{N_A}\left(10\right).$
В выражении (10) мы получили, что заряд иона в электролите пропорционален валентности вещества $(Z)$. Этот результат показывает, что величины электрических зарядов ионов кратны между собой. Минимальный заряд, равный заряду электрона, имеют ионы одновалентных веществ.
Пример 1
Задание: Найдите скорость $v,$ с которой увеличивается слой вещества, являющегося проводником второго рода на плоской поверхности электрода в процессе электролиза при прохождении тока, плотность которого равна $j$. Считать, что электролит имеет валентность равную $Z$, плотность $\rho ,\ молярную\ массу\ \mu .$
Решение:
В качестве основы решения задачи применим объединенный закон Фарадея:
$m=\frac{\mu }{Z}\frac{q}{F}\left(1.1\right),$
где $q=It$, $I$ — сила тока, текущего через электролит, $t$ — время, которое тек ток. Если считать, что осаждение никеля идет равномерно по поверхности металла, то массу выделившегося вещества запишем как:
$m=\rho Sh\ \left(1. 2\right),$
2\right),$
где $\rho $ — плотность никеля, $S$ — площадь поверхности металла, $h$ — толщина слоя никеля. Силу тока, выразим через его плотность:
$I=jS\left(1.3\right).$
Подставим в выражение (1.1) силу тока из (1.3) и массу из (1.2), получим:
$\rho Sh=\frac{\mu}{Z}\frac{jSt}{F}\to \rho h=\frac{\mu}{Z}\frac{jt}{F}\left(1.4\right).$
В том случае, если плотность тока постоянна, то скорость ($v=\frac{h}{t}$) увеличения слоя никеля так же постоянна. Разделим обе части выражения (1.4) на время, имеем:
$\rho \frac{h}{t}=\frac{\mu }{Z}\frac{j}{F}\to v=\frac{\mu }{Z}\frac{j}{\rho F}.$
Ответ: $v=\frac{\mu }{Z}\frac{j}{\rho F}.$
Пример 2
Задание: Через раствор электролита ток силой $I$ тек в течение времени $t$. Какое количество вещества $(\nu)$ выделится на катоде, каково число атомов $(N)$ вещества при этом, если металл имеет валентность $Z$.
Решение:
За основу решения задачи примем объединенный закон Фарадея:
$m=\frac{\mu }{Z}\frac{q}{F}\left(2. 1\right),$
1\right),$
где $q=It$, $I$ — сила тока, текущего через электролит, $t$ — время, которое тек ток. При этом нам известно, что:
$\nu =\frac{m}{\mu }\left(2.2\right).$
Разделим правую и левую части выражения (2.1) на молярную массу ($\mu $) вещества электролита, получим:
$\nu =\frac{1}{Z}\frac{q}{F}=\frac{It}{ZF}\left(2.3\right),$
где $q=It.$ Количество атомов осадка найдем, используя формулу:
$N=\nu \cdot N_A=\frac{It}{ZF}N_A.$
Ответ: $\nu =\frac{It}{ZF},\ N=\frac{It}{ZF}N_A.$
Учебник по химии электролиза по законам Фарадея
Ключевые концепции
- Первый закон:
Масса вещества, полученного при электролизе, пропорциональна количеству используемого электричества.
Пример: электролиз жидкого хлорида натрия дает жидкий металлический натрий и газообразный хлор.
Количество потребляемой электроэнергии (кв.) Масса произведенного натрия (м) Кв / м 28 950 кулонов 6.  9 г
9 г28 950 / 6,9
= 4196Увеличение количества электричества (Q) производит больше граммов натрия (m).
Q / m в этом случае всегда равно 4196.
Q / м — постоянная величина.
Q пропорционален m
, то есть Q ∝ m96 500 кулонов 23,0 г 96 500 / 23,0
= 4196482 500 кулонов 115.0 г 482 500 / 115,0
= 4196Это означает, что для электролитического производства большего количества вещества мы должны использовать больше электричества.
- Второй закон:
1 Количество электричества в кулонах, необходимое для производства 1 моля вещества, представляет собой простое целое число, кратное 2 96 500
То есть количество электричества (Q) в кулонах, разделенное на 96 500, является простым целым числом.
Произвести 1 моль подчеркнутого вещества необходимое количество электроэнергии (Q) Q / 96,500 Na + + e — → Na 96 500 кулонов 96 500/96 500
= 1В каждом примере Q / 96 500 — простое целое число. 
Если n представляет это простое целое число,
и Q — количество электричества в кулонах, тогдаn = Q / 96 500
Cu 2+ + 2e — → Cu 193000 кулонов 193 000/96 500
= 2Fe 3+ + 3e — → Fe 289 500 кулонов 289 500/96 500
= 3Количеству 96 500 присвоено имя Фарадея (или Константа Фарадея) и символ F.
F равно количеству электричества, переносимому одним моль электронов:
F = Число Авогадро × заряд электрона в кулонах
= 6.022 × 10 23 моль -1 × 1.602192 × 10 -19 С
= 96,484 C · моль -1 (обычно округляется до 96,500 C · моль -1 в химии средней школы) - Законы Фарадея для расчетов электролиза:
Q = n (e — ) × F
Q = количество электричества, измеренное в кулонах (C)
n (e — ) = использованные моль электронов
F = Фарадея (постоянная Фарадея) = 96,500 Кл моль -1Мы можем рассчитать массу вещества, полученного во время эксперимента по электролизу, следующим образом:
i) вычисление используемых молей электронов: n (e — ) = Q / F
ii) использование молей электронов для расчета количества молей образующегося вещества с использованием уравнения сбалансированной полуреакции восстановления (или окисления)
iii) использование молей вещества для расчета массы вещества:
масса = моль × молярная масса
Пожалуйста, не блокируйте рекламу на этом сайте.
Без рекламы = для нас нет денег = для вас нет бесплатных вещей!
Рабочие примеры: Q = n (e
— ) F вычисленияВопрос 1. Рассчитайте количество электричества, полученное из 2 молей электронов.
Решение:
(на основе подхода StoPGoPS к решению проблем.)
- Что вас просят сделать?
Рассчитать количество электроэнергии
Q =? C - Какие данные (информацию) вы указали в вопросе?
Извлеките данные из вопроса:
моль электронов = n (e — ) = 2 моль
Постоянная Фарадея = F = 96,500 C моль -1 (технический паспорт) - Какая связь между тем, что вы знаете, и тем, что вам нужно выяснить?
Напишите уравнение:
Q = n (e — ) × F - Подставьте значения в уравнение и решите относительно Q:
Q = 2 × 96 500 = 193 000 С - Правдоподобен ли ваш ответ?
Используйте рассчитанное вами значение Q и постоянную Фарадея F, чтобы вычислить количество молей электронов и сравнить его со значением, указанным в вопросе.

Q = n (e — ) F
193 000 = n (e — ) × 96 500
n (e) = 193,000 ÷ 96,500 = 2
Поскольку нам сказали, что в вопросе 2 моля электронов, мы достаточно уверены, что наше значение Q является правильным. - Назовите свое решение проблемы:
Q = 193 000 ° C
Вопрос 2. Вычислите моль электронов, полученных из 250 C электричества.
Решение:
(на основе подхода StoPGoPS к решению проблем.)
- Что вас просят сделать?
Вычислить моль электронов
n (e — ) =? моль - Какие данные (информацию) вы указали в вопросе?
Извлеките данные из вопроса:
Q = 250 С
F = 96,500 C моль -1 (технический паспорт) - Какая связь между тем, что вы знаете, и тем, что вам нужно выяснить?
Напишите уравнение:
Q = n (e — ) × F
Перепишите уравнение, чтобы найти число молей электронов, n (e — ):
n (e — ) = Q ÷ F - Подставьте значения в уравнение и решите относительно n (e — ):
n (e — ) = 250 ÷ 96 500 = 2.
 59 × 10 -3 моль
59 × 10 -3 моль - Правдоподобен ли ваш ответ?
Используйте рассчитанное вами значение n (e — ) и постоянную Фарадея F, чтобы рассчитать необходимое количество заряда (Q) и сравнить его со значением, указанным в вопросе.
Q = n (e — ) × F
Q = 2,59 × 10 -3 × 96 500 = 250 ° C
Поскольку это значение Q согласуется с приведенным в вопросе, мы достаточно уверены, что наше значение для n (e — ) является правильным. - Назовите свое решение проблемы:
n (e — ) = 2,59 × 10 -3 моль
Рабочие примеры: Расчет количества депонированного вещества
Вопрос 1: Вычислите количество молей металлической меди, которое может быть произведено электролизом расплавленного сульфата меди с использованием электричества 500 C.
Решение:
(На основе подхода StoPGoPS к решению проблем. )
)
- Что вас просят сделать?
Расчет молей металлической меди
n (Cu (s) ) =? моль - Какие данные (информацию) вы указали в вопросе?
Извлеките данные из вопроса:
электролит: CuSO 4 (л)
Q = 500 C
F = 96,500 C моль -1 (технический паспорт) - Какая связь между тем, что вы знаете, и тем, что вам нужно выяснить?
Напишите уравнение реакции восстановления для получения металлической меди из расплавленного сульфата меди:
Cu 2+ + 2e — → Cu (т)Вычислить моль электронов, n (e — ):
n (e — ) = Q ÷ F
= 500 ÷ 96 500
= 5.18 × 10 -3 моль - Определите количество молей Cu (s) , полученных с использованием сбалансированного уравнения реакции восстановления (мольное соотношение):
1 моль электронов дает ½ моля Cu (s)
Следовательно, 5,18 × 10 -3 моль электронов дает ½ × 5,18 × 10 -3
n (Cu (s) ) = 2,59 × 10 -3 моль - Правдоподобен ли ваш ответ?
Используйте рассчитанное вами значение n (Cu (s) ) и постоянную Фарадея F, чтобы рассчитать необходимое количество заряда (Q) и сравнить его со значением, указанным в вопросе.

Q = n (e — ) F
n (e — ) = 2 × n (Cu) = 2 × 2,59 × 10 -3 = 5,18 × 10 -3 моль
F = 96 500
Q = 5,18 × 10 -3 × 96,500 = 500 ° C
Поскольку это значение для Q такое же, как указанное в вопросе, мы достаточно уверены, что наше рассчитанное значение для молей осажденной меди является правильным. - Назовите свое решение проблемы:
n (Cu (s) ) = 2.59 × 10 -3 моль
Вопрос 2. Рассчитайте массу серебра, которая может быть произведена электролизом 1 моль л. -1 AgCN (водн.) , используя 800 C электричества.
Решение:
(на основе подхода StoPGoPS к решению проблем.)
- Что вас просят сделать?
Рассчитать массу наплавленного серебра
м (Ag (s) ) =? грамм - Какие данные (информацию) вы указали в вопросе?
Извлеките данные из вопроса:
электролит: AgCN (водн. )
)
[AgCN (водн.) ] = 1 моль л -1 (стандартный раствор)
Q = 800 С
F = 96,500 C моль -1 (технический паспорт) - Какая связь между тем, что вы знаете, и тем, что вам нужно выяснить?
Напишите уравнение реакции восстановления для получения металлического серебра из водного раствора:
Ag + (водн.) + e — → Ag (s)Вычислить моль электронов, n (e — ):
n (e — ) = Q ÷ F
n (e — ) = 800 ÷ 96 500 = 8.29 × 10 -3 мольОпределите количество молей полученного Ag (s) , используя уравнение сбалансированной реакции восстановления (мольное соотношение):
1 моль электронов дает 1 моль Ag (s)
Следовательно, 8,29 × 10 -3 моль электронов дает 8,29 × 10 -3 моль Ag (s) - Рассчитайте массу Ag (т)
моль (Ag) = масса (Ag) ÷ молярная масса (Ag)
Итак, масса (Ag) = моль (Ag) × молярная масса (Ag)моль (Ag) = 8.
 29 × 10 -3 моль
29 × 10 -3 моль
молярная масса (Ag) = 107,9 г моль -1 (из периодической таблицы)масса (Ag) = 8,29 × 10 -3
моль× 107,9 гмоль -1
= 0,894 г - Правдоподобен ли ваш ответ?
Используйте рассчитанное вами значение m (Ag (s) ) и постоянную Фарадея F, чтобы рассчитать необходимое количество заряда (Q) и сравнить его со значением, указанным в вопросе.
n (e — ) = n (Ag) = масса ÷ молярная масса = 0,894 ÷ 107,9 = 8,29 × 10 -3 моль
Q = n (e — ) F = 8,29 × 10 -3 моль × 96,500 = 800 C
Поскольку это значение Q совпадает с приведенным в вопросе, мы достаточно уверены, что наша расчетная масса серебра верна. - Назовите свое решение проблемы:
м (Ag (s) ) = 0.894 г
Рабочие примеры: Q = n (e
— ) F и Q = It Вопрос 1. Какую массу меди можно было бы отложить из раствора сульфата меди (II) при токе 0,50 А в течение 10 секунд?
Какую массу меди можно было бы отложить из раствора сульфата меди (II) при токе 0,50 А в течение 10 секунд?
Решение:
(на основе подхода StoPGoPS к решению проблем.)
- Что вас просят сделать?
Рассчитать массу осажденной меди
м (Cu (s) ) =? грамм - Какие данные (информацию) вы указали в вопросе?
Извлеките данные из вопроса:
электролит: раствор сульфата меди (II), CuSO 4
ток: I = 0.50 А
время: t = 10 секунд
F = 96,500 C моль -1 (технический паспорт) - Какая связь между тем, что вы знаете, и тем, что вам нужно выяснить?
Рассчитайте количество электроэнергии:
Q = I x t
I = 0,50 А
t = 10 секунд
Q = 0,50 × 10 = 5,0 ° СВычислить моль электронов:
n (e — ) = Q ÷ F
Q = 5.0 С
F = 96,500 C моль -1
n (e — ) = 5,0 ÷ 96,500
= 5,18 × 10 -5 мольРассчитайте количество молей меди, используя уравнение сбалансированной половины реакции восстановления:
Cu 2+ + 2e — → Cu (т)
1 моль меди осаждается из 2 моль электронов (мольное соотношение)
моль (Cu) = ½n (e — )
= ½ × 5,18 × 10 -5
= 2. 59 × 10 -5 моль
59 × 10 -5 моль - Рассчитать массу меди:
масса = моль × молярная масса
моль (Cu) = 2,59 × 10 -5 моль
молярная масса (Cu) = 63,55 г моль -1 (из Периодической таблицы)
масса (Cu) = (2,59 × 10 -5 ) × 63,55
= 1,65 × 10 -3 г
= 1,65 мг - Правдоподобен ли ваш ответ?
Используйте рассчитанное вами значение m (Cu (s) ) и константу Фарадея F, чтобы рассчитать количество требуемого заряда (Q (b) ), и сравните это со значением Q (a) = Он задан. в вопросе.
Q (а) = It = 0,50 × 10 = 5 ° CQ (b) = n (e — ) F
n (e — ) = 2 × n (Cu) = 2 × [m (Cu) ÷ M r (Cu)] = 2 × [(1,65 × 10 -3 ) ÷ 63,55] = 2 × 2,6 × 10 -5 = 5,2 × 10 -5 моль
Q = 5,2 × 10 -5 × 96 500 = 5Поскольку Q (a) = Q (b) = 5 C, мы достаточно уверены, что наша расчетная масса меди верна.

- Назовите свое решение проблемы:
м (Cu (s) ) = 1,65 × 10 -3 г (или 1,65 мг)
Вопрос 2. Рассчитайте время, необходимое для осаждения 56 г серебра из раствора нитрата серебра, используя ток 4,5 А.
Решение:
(На основе подхода StoPGoPS к решению проблем.)
- Что вас просят сделать?
Рассчитать необходимое время
т =? секунды - Какие данные (информацию) вы указали в вопросе?
Извлеките данные из вопроса:
масса серебра = m (Ag (s) ) = 56 г
ток = I = 4,5 А
F = 96,500 C моль -1 (из техпаспорта) - Какая связь между тем, что вы знаете, и тем, что вам нужно выяснить?
Рассчитайте количество осажденных молей серебра:
моль (Ag) = масса (Ag) ÷ молярная масса (Ag)
Масса нанесенного Ag = 56 г
молярная масса = 107.9 г моль -1 (из таблицы Менделеева)
моль (Ag) = 56 ÷ 107,9
= 0,519 мольРассчитайте количество молей электронов, необходимых для реакции:
Напишите уравнение реакции восстановления:
Ag + + e — → Ag (т)
Из уравнения 1 моль Ag откладывается на 1 моль электронов (мольное соотношение)
, следовательно, 0,519 моль Ag (s) откладывается на 0,519 моль электронов.
n (e — ) = 0.519 мольРассчитайте необходимое количество электроэнергии:
Q = n (e — ) × F
n (e — ) = 0,519 моль
F = 96,500 C моль -1
Q = 0,519 × 96,500 = 50,083,5 C - Рассчитайте необходимое время:
Q = I × т
Перепишите уравнение, чтобы найти t:
т = Q ÷ I
Q = 50 083.5 С
I = 4,5 А
т = 50 083,5 ÷ 4,5
= 11,129,67 секунды
t = 11,129,67 ÷ 60 = 185,5 минут
t = 185,5 ÷ 60 = 3,1 часа - Правдоподобен ли ваш ответ?
Используйте рассчитанное вами значение времени в секундах, постоянную Фарадея F и ток, указанный в вопросе, чтобы вычислить массу Ag, которую вы можете поместить, и сравните ее со значением, указанным в вопросе.
Q = It = 4,5 × 11,129,67 = 50083,5 С
Q = n (e — ) F
so, n (e — ) = Q ÷ F = 50083,5 ÷ 96,500 = 0,519 моль
n (Ag) = n (e — ) = 0,519 моль
m (Ag) = n (Ag) × M r (Ag) = 0,519 × 107,9 = 56 г
Поскольку это значение массы серебра такое же, как и в вопросе, мы достаточно уверены, что время в секундах, которое мы рассчитали, является правильным.
- Назовите свое решение проблемы:
т = 11,129.67 секунд (или 185,5 минут, или 3,1 часа)
1. Более формально мы говорим, что для данного количества электричества количество произведенного вещества пропорционально его эквивалентному весу.
2. Цифра ближе к 96 484, но обычно округляется до 96 500 для школьных расчетов по химии.
Электролиз — определение, формула, примеры, применение
Что такое электролиз?
Электролиз — это процесс, при котором на электродах (катоде или аноде) происходят химические изменения из-за прохождения электричества через раствор электролита.В химии процесс электролиза осуществляется путем окислительно-восстановительной или окислительно-восстановительной реакции, при которой вещество теряет или приобретает электроны. Технология электролиза — это коммерчески важный процесс извлечения или очистки металлов (меди, никеля, серебра, золота) из природных руд или минералов с использованием реакции в электролитической ячейке.
Электролиз соляной кислоты
Процесс электролиза и механизм электропроводности раствора соляной кислоты определяют избыток электронов на катоде и недостаток электронов на аноде.
Ион водорода (H + ) в растворе движется к катоду за счет кулоновской силы притяжения и принимает один электрон, чтобы сформировать атом водорода. Аналогичным образом ион хлора из раствора движется к аноду, уходит один электрон, образуя нейтральный атом хлора. Следовательно, одноэлектронный перенос от катода к аноду с помощью растворов соляной кислоты или среды, и из-за проводимости электрического тока или электролиза ионы разлагаются на электроде.Два атома водорода образуют газообразный водород, а два атома хлора образуют молекулу хлора, покидая электролитический раствор.
Закон электролиза Фарадея формула
Первый закон электролиза Фарадея
Первый закон электролиза Фарадея гласит, что степень разложения на электроде (w) прямо пропорциональна количеству пропущенного электрического тока или электричества (Q). Математическая формула первого закона w = ZQ, где w = электрохимическая эквивалентность разлагающихся веществ.Опять же, w = ZIt, где I = сила тока или количество электричества, проходящего в единицу времени, t = время протекания электричества и Z = электрохимический эквивалент.
Математическая формула первого закона w = ZQ, где w = электрохимическая эквивалентность разлагающихся веществ.Опять же, w = ZIt, где I = сила тока или количество электричества, проходящего в единицу времени, t = время протекания электричества и Z = электрохимический эквивалент.
Второй закон электролиза Фарадея
Второй закон электролиза Фарадея гласит, что масса различных веществ, разложившихся на разных электродах под действием данного электричества, пропорциональна их эквивалентной массе. Математическая формула второго закона электролиза, w 1 / w 2 = E 1 / E 2 , где w 1 и w 2 = масса разложившегося вещества, а E 1 и E 2 = эквивалентные веса.
Что такое один фарадей электричества?
Один фарадей определяет количество электричества, необходимое для разложения одного грамма эквивалента электролитического вещества в химии или химической науке, а числовое значение 1F = 96496 кулонов ≈ 96500 кулонов.
Электрохимический эквивалент серебра (атомная масса = 108), Z Ag = 108/96500 = 0,001118 г / кулон. Этот закон использовался для создания кулонометра прибора для определения количества электричества, проходящего через цепь, путем определения количества вещества, разлагающегося на электроде в растворе для электролиза.
Расчет числа Авогадро
При изучении химии второй закон Фарадея помогает определить число Авогадро (N 0 ). Для разложения 1 моля вещества на электроде требуется электричество ZF и количество заряда 1 моль вещества ZeN 0 . Следовательно, ZeN 0 = ZF или N 0 = F / e. Числовое значение числа Авогадро = 96500 / 1,6 × 10 -19 = 6,023 × 10 23 .
Применение электролиза
- Процесс электролиза имеет множество важных промышленных применений для извлечения (электровыделение) или очистки (электролитическое рафинирование) металлов и неметаллов (алюминия, лития, натрия, магния, меди, серебра, золота, фтора, хлора) из руд или соединений.
 .
. - Используется для нанесения покрытий на металлы или гальваники.
- Расплавленный хлорид натрия дает металлический натрий и молекулу хлора, но электролиз водного раствора хлорида натрия дает гидроксид натрия и газообразный хлор. Этот процесс используется для производства водорода и кислорода из водного раствора. В формуле электролиза
- используются топливные элементы, которые производят химическую энергию путем сжигания таких топлив, как водород, окись углерода, метан, пропан, метиловый спирт.Он непосредственно преобразуется в электрическую энергию, используемую в качестве экологически чистого постоянного источника энергии в космических кораблях и атомных подводных лодках.
Закон Фарадея — Chemistry LibreTexts
- Последнее обновление
- Сохранить как PDF
- Участники и авторства
В каждом электрохимическом процессе, спонтанном или нет, определенное количество электрического заряда передается во время окисления и восстановления. Полураакции, которые мы написали для электродных процессов, включают электроны, несущие этот заряд. Скорость передачи заряда можно измерить с помощью устройства, называемого амперметром.
Полураакции, которые мы написали для электродных процессов, включают электроны, несущие этот заряд. Скорость передачи заряда можно измерить с помощью устройства, называемого амперметром.
Амперметр измеряет ток, протекающий в цепи. Единицы измерения тока — амперы (А) (для краткости амперы). В отличие от вольтметра, амперметры позволяют электронам проходить и, по сути, «синхронизируют» их. Затем количество электрического заряда, прошедшего через цепь, можно рассчитать с помощью простого соотношения:
Заряд = ток x время ИЛИ Кулоны = амперы x секунды
Это позволяет связать стехиометрию реакции с электрическими измерениями.Принципы, лежащие в основе этих отношений, были разработаны в первой половине XIX века английским ученым Майклом Фарадеем.
На диаграмме показано, как можно измерить напряжение и ток для типичного гальванического элемента, но расположение одинаково для любого электрохимического элемента. Обратите внимание, что вольтметр помещается поперек канала для электронов (т. Е. Провода), в то время как амперметр является частью этого канала. Таким образом можно использовать вольтметр хорошего качества, даже если может показаться, что он «замыкает» цепь.Поскольку электроны не могут проходить через вольтметр, они просто продолжают движение по проводу.
Е. Провода), в то время как амперметр является частью этого канала. Таким образом можно использовать вольтметр хорошего качества, даже если может показаться, что он «замыкает» цепь.Поскольку электроны не могут проходить через вольтметр, они просто продолжают движение по проводу.
И вольтметр, и амперметр поляризованы. На них нанесены отрицательные и положительные клеммы. Электроны «ожидаются» только в одном направлении. Это важно при измерениях постоянного тока (DC), например, выходящего из (или входящего) электрохимических ячеек.
Закон электролиза Фарадея можно сформулировать так: количество вещества, производимого на каждом электроде, прямо пропорционально количеству заряда, протекающего через элемент.Конечно, это своего рода упрощение. Вещества с различными изменениями окисления / восстановления в отношении электронов / атома или иона не будут производиться в одинаковых молярных количествах. Но если учесть эти дополнительные соотношения, закон верен во всех случаях.
| Пример 1 |
|---|
|
| Пример 2 |
|---|
| Пример 3 |
|---|
| Пример 4 |
|---|
| Пример 5 |
|---|
Авторы и ссылки
Стивен Р.Марсден
Основные расчеты электролиза
Постоянная Фарадея — самый важный бит информации в расчетах электролиза. Убедитесь, что вы действительно понимаете следующую часть.
Кулоны
кулон — это мера количества электричества. Если в течение 1 секунды протекает ток в 1 ампер, значит, прошел 1 кулон электричества.
Если в течение 1 секунды протекает ток в 1 ампер, значит, прошел 1 кулон электричества.
Это означает, что вы можете вычислить, сколько электричества прошло за заданное время, умножив ток в амперах на время в секундах.
Количество кулонов = ток в амперах x время в секундах
Если вам дано время в минутах, часах или днях, тогда вы должны преобразовать это время в секунды, прежде чем делать что-либо еще.
Например, если в течение часа течет ток 2 ампера, то:
Количество кулонов = 2 x 60 x 60 = 7200
(60 минут в час; 60 секунд в каждой минуте)
Это просто!
Фарадей
Электричество — это поток электронов.Для целей расчетов нам нужно знать, как связать количество молей электронов, которые текут, с измеренным количеством электричества.
Заряд, который несет каждый электрон, составляет 1,60 x 10 -19 кулон. Если вам когда-нибудь понадобится использовать его на экзамене, вам будет дана ценность.
1 моль электронов содержит постоянную Авогадро, L, электронов — то есть 6,02 x 10 23 электрон. Вам также дадут это на экзамене, если вам нужно его использовать.
Это означает, что 1 моль электронов должен нести
6.02 x 10 23 x 1,60 x 10 -19 кулон
= 96320 кулонов
Это значение известно как постоянная Фарадея.
Вы можете встретить формулу F = Le , где F — постоянная Фарадея, L — постоянная Авогадро, а e — заряд электрона (в единицах количества кулонов, которые он несет). Мы только что использовали это, фактически не заявляя об этом — это в основном очевидно!
Числа, которые мы здесь используем, округлены.Расчет просто показывает вам, как это решить, если вам нужно, но не дает обычно используемого значения. Для целей экзамена значение постоянной Фарадея обычно принимается равным 9,65 x 10 4 C моль -1 (кулонов на моль).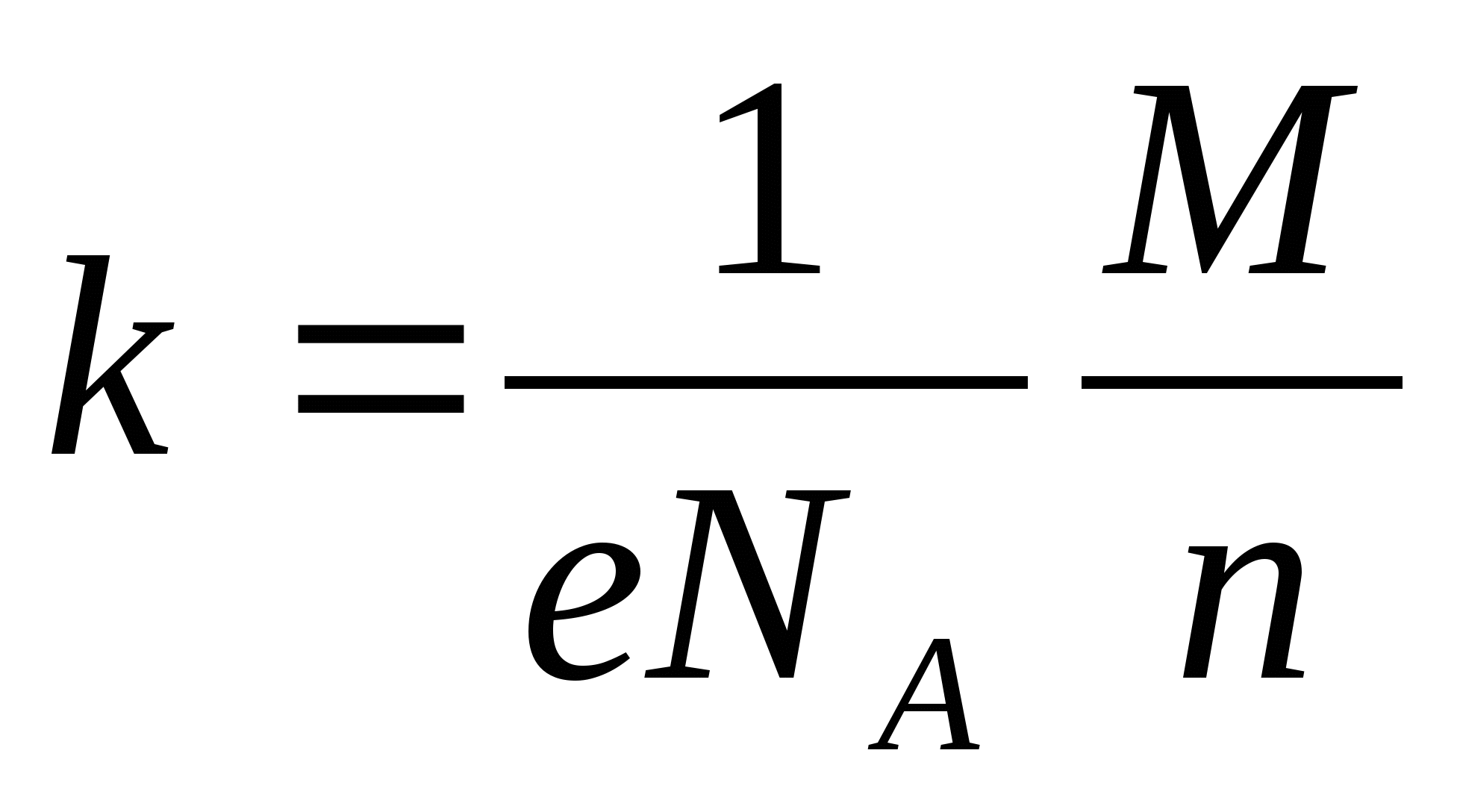 Это еще одно число, которое вам вряд ли придется запоминать.
Это еще одно число, которое вам вряд ли придется запоминать.
То есть 96500 кулонов на моль.
Итак, 96500 кулонов называется 1 фарадей . Обратите внимание на маленькую букву «f», когда она используется как единица измерения.
Всякий раз, когда у вас есть уравнение, в котором имеется 1 моль электронов, это представлено в электрической цепи 1 фарадеем электричества — другими словами, 96500 кулонами.
Законы Фарадея электролиза — Первый закон, Второй закон и его приложения
Законы Фарадея электролиза — это фундаментальные законы, которые описывают значение электролитических эффектов. В этом посте будет обсуждаться, что такое электролиз, каковы законы электролиза Фарадея (первый и второй закон), его применение, преимущества и недостатки.
Подробнее о законах электролиза Фарадея Майкл Фарадей известен своим вкладом в области электрохимии.Он открыл два закона электролиза, согласно которым величина химического изменения или разложения точно пропорциональна количеству электричества, которое передается в растворе.
Рис. 1 — Введение в законы электролиза Фарадея
Во время этого химического изменения (окисления или восстановления) количество осажденного или растворенного вещества пропорционально их химическому эквивалентному весу. Количество заряда, необходимое для этого, равно заряду одного моля электронов, известному как 1 Фарадея, что равно 96 500 Кулонам.Законы в основном устанавливают количественные аспекты электролиза, основанные на электрохимических исследованиях, опубликованных Майклом Фарадеем в 1833 году.
Рис. 2 — Изображение Майкла Фарадея
Что такое электролиз Процесс, в котором Электрическая энергия вызывает несамопроизвольную химическую реакцию, известную как электролиз. Электролиз лежит в основе электросинтеза химических соединений. В этом процессе химические изменения происходят через реакции на электродах, которые контактируют с электролитом, когда через него проходит электрический ток.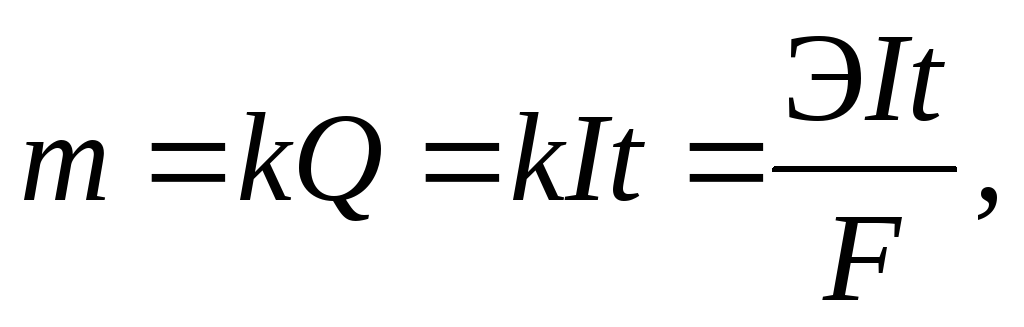
Во время этого процесса положительно заряженные ионы дрейфуют к отрицательному электроду, а отрицательно заряженные ионы дрейфуют к положительному электроду. Положительно заряженные ионы получают электроны, тогда как отрицательно заряженные ионы теряют электроны. Окисление происходит на аноде, а восстановление происходит на катоде.
Рассмотрим Рис. 3, где электроды погружены в водный раствор хлорида натрия. Когда электричество проходит через раствор хлорида натрия, газообразный водород образуется на отрицательном электроде, а газообразный хлорид окисляется до хлора на положительном электроде.
Рис.3 — Электролиз хлорида натрия
Законы электролиза ФарадеяДва закона электролиза:
Первый закон электролиза Фарадея Первый закон в законах Фарадея электролиза гласит, что «количество химической реакции, происходящей на любом электроде из-за воздействия электрической энергии, прямо пропорционально количеству прошедшего через электролит ».
Предположим, что количество вещества, осажденного или растворенного на электродах, равно «m», а «Q» — это количество заряда (электричества), прошедшего через электролит. Согласно Первому закону Фарадея:
, где Z = электрохимический эквивалент
Соотношение между химическим эквивалентом (E), постоянной Фарадея (F) и электрохимическим эквивалентом (Z) определяется уравнением:
Мы знаем что, Q = I xt
Где,
- Q = количество заряда (электричества) в кулонах (Q),
- I = ток в амперах (A),
- t = время (секунды)
Следовательно, уравнение m = ZQ также может быть записано как:
Второй закон электролиза Фарадея Второй закон в законах Фарадея электролиза гласит: «Масса вещества, которое откладывается, когда такое же количество заряда (электричества), проходящего через раствор электролита, прямо пропорционально их химическому эквивалентному весу ».
Математически этот закон может быть представлен как:
, где
- m = масса вещества
- E = эквивалентный вес вещества
Его также можно выразить как:
Эквивалентный вес или химический эквивалент вещества можно определить как соотношение его веса и валентности.
Приложения законов электролиза ФарадеяПриложения законов Фарадея электролиза включают:
- Законы Фарадея помогают в определении эквивалентных масс элементов.
- На основании законов электролиза получают неметаллы, такие как водород, фтор, хлор.
- Они также применяются в области электронной металлургии для получения металлов, таких как натрий, калий.
- Процесс гальваники включает электролиз.
- Электролизное рафинирование металлов осуществляется методом электролиза.
- Электролиз — это ответ на возобновляемые источники энергии.
Рис. 4 — Установка электролизного рафинирования меди
4 — Установка электролизного рафинирования меди
Преимущества включают:
- Промышленные химикаты легко производятся с помощью процесса электролиза.
- Процесс эффективен и рентабелен.
Недостатки:
- Требуемая энергия высока.
- Отрасли, основанные на электролизе, производят большое количество сточных вод в виде отходов.
- Отходы этих предприятий способствуют загрязнению окружающей среды.
Также читают: Законы Де Моргана - Первый и Второй закон, проверка и приложения Электрическое поле - закон Гаусса и Кулона, линии электрического поля, приложения Закон Ома - соотношение напряжения, тока и сопротивления, когда не применимо Законы Кирхгофа для тока и напряжения - применение, преимущества, ограничения
Лакшми — Б. E (Электроника и связь) и имеет опыт работы в RelQ Software в качестве инженера-испытателя и HP в качестве руководителя службы технической поддержки. Она — автор, редактор и партнер Electricalfundablog.
E (Электроника и связь) и имеет опыт работы в RelQ Software в качестве инженера-испытателя и HP в качестве руководителя службы технической поддержки. Она — автор, редактор и партнер Electricalfundablog.
Стехиометрия электролиза | Введение в химию
Цель обучения
- Предсказать, сколько кулонов потребуется для данной электрохимической реакции.
Ключевые моменты
- С точки зрения источника напряжения и цепи вне электродов, поток электронов обычно описывается в терминах электрического тока с использованием кулонов и ампер в единицах СИ.
- Требуется 96 485 кулонов, чтобы составить моль электронов, единицу, известную как фарадей (F).
- Эквивалентный вес вещества определяется как молярная масса, деленная на количество электронов, необходимых для окисления или восстановления каждой единицы вещества.
Условия
- Фарадей Количество электричества, необходимое для депонирования или высвобождения 1 грамма эквивалентного веса вещества во время электролиза; приблизительно 96 487 кулонов.

- кулонов В Международной системе единиц — производная единица электрического заряда; количество электрического заряда, переносимого током в 1 ампер, протекающим в течение 1 секунды. Символ: C.
Стехиометрия электролитической ячейки
Степень химического изменения, происходящего в электролитической ячейке, стехиометрически зависит от количества молей электронов, проходящих через ячейку. С точки зрения источника напряжения и цепи за пределами электродов, поток электронов обычно описывается в терминах электрического тока с использованием единиц СИ в кулонах и амперах.Для образования моля электронов требуется 96 485 кулонов — единица, известная как фарадей (F).
Это соотношение было впервые сформулировано Майклом Фарадеем в 1832 году в форме двух законов электролиза:
- Вес веществ, образующихся на электроде во время электролиза, прямо пропорционален количеству электричества, которое проходит через электролит.
- Вес различных веществ, образованных при прохождении одного и того же количества электричества, пропорционален эквивалентному весу каждого вещества.
 — \ rightarrow V [/ latex]).
— \ rightarrow V [/ latex]).Большинство стехиометрических задач, связанных с электролизом, могут быть решены без явного использования законов Фарадея. «Химия» в этих задачах обычно очень элементарна; основные трудности обычно возникают из-за незнания основных электрических устройств:
- ток (в амперах) — это скорость переноса заряда: 1 ампер = 1 [латекс] \ frac {Coulombs} {second} [/ latex]. Мощность
- (в ваттах) — это скорость производства или потребления энергии: 1 Вт = 1 [латекс] \ frac {Джоуль} {секунда} [/ латекс].-} = 1184 \ Coulombs [/ latex]
1,5 часа эквивалентно 5400 секундам:
[латекс] \ frac {1184 \ Coulombs} {5400 \ секунды} = 0,22 \ ампер [/ латекс]
Показать источникиBoundless проверяет и курирует высококачественный контент с открытой лицензией из Интернета. Этот конкретный ресурс использовал следующие источники:
законов Фарадея
с общим потенциалом –1,23 вольт. Обладая отрицательным потенциалом, он требует внешнего электрического тока для разложения воды указанной реакцией.
 На рисунке 1 показаны два платиновых электрода в воде, содержащей небольшое количество соли или кислоты, так что раствор может проводить электричество.
На рисунке 1 показаны два платиновых электрода в воде, содержащей небольшое количество соли или кислоты, так что раствор может проводить электричество.Рисунок 1. Электролиз воды.
Восстановление на катоде дает газ H 2 , а окисление на аноде дает газ O 2 . Обратите внимание, что на рисунке показано, что объем водорода в два раза больше объема кислорода — посмотрите на пузырьки. Молярные коэффициенты в реакции разложения подразумевают 2 объема газа H 2 на каждый 1 объем газа O 2 .
Электролиз используется для разложения многих соединений на составляющие их элементы. Вы видели этот процесс с водой. Другой пример — электролиз расплавленного хлорида натрия с получением расплавленного металлического натрия и газообразного хлора:
Химики девятнадцатого века открыли новые элементы в результате электролитического разложения многих соединений.
Количественные законы электрохимии были открыты Майклом Фарадеем из Англии.
 В его статье 1834 года по электролизу были введены многие термины, которые вы видели в этой книге, включая ион, катион, анион, электрод, катод, анод, и электролит .Он обнаружил, что масса вещества, образующегося в результате окислительно-восстановительной реакции на электроде, пропорциональна количеству электрического заряда, прошедшего через электрохимическую ячейку. Для элементов с разной степенью окисления одно и то же количество электричества производит меньше молей элемента с более высокой степенью окисления.
В его статье 1834 года по электролизу были введены многие термины, которые вы видели в этой книге, включая ион, катион, анион, электрод, катод, анод, и электролит .Он обнаружил, что масса вещества, образующегося в результате окислительно-восстановительной реакции на электроде, пропорциональна количеству электрического заряда, прошедшего через электрохимическую ячейку. Для элементов с разной степенью окисления одно и то же количество электричества производит меньше молей элемента с более высокой степенью окисления.Базовая единица электрического заряда, используемая химиками, соответственно называется фарадея , который определяется как заряд одного моля электронов (6 × 10 23 электрон).Кстати, обратите внимание, что химики расширили первоначальное определение моля как единицы массы до соответствующего числа (числа Авогадро) частиц. Используйте электролиз расплавленного хлорида натрия, чтобы увидеть взаимосвязь между фарадеями электричества и молями продуктов разложения.

Полуреакция восстановления —
., поэтому для производства 1 моля металлического натрия требуется 1 моль электронов, поэтому 1 фарадей заряда должен пройти через элемент.
Полуреакция окисления
, а для производства 1 моля газообразного хлора через устройство должно пройти 2 фарада электрического заряда.Обратите внимание, как количество электронов в окислительно-восстановительных реакциях определяет количество электричества, необходимое для реакции.
Сумма этих полуреакций с общей реакцией в электролитической ячейке:
Прохождение заряда в 2 фарада дает 2 моля металлического натрия и 1 моль газообразного хлора.
Первый из законов Фарадея гласит, что масса производимого вещества пропорциональна количеству электричества. Применение этого закона к примеру с NaCl, где 1 моль Cl 2 был произведен за 2 фарада, означает, что для производства 10 моль Cl 2 требуется прохождение через устройство 20 фарадеев.

Второй из законов Фарадея гласит, что данное количество электричества производит меньше молей веществ с более высокими степенями окисления. Сравните уменьшение ионов натрия и кальция:
Для производства 1 моля металлического кальция требуется вдвое больше электроэнергии, чем для производства 1 моля металлического натрия.
Электролитическое разложение хлорида натрия и оксида кальция выглядит одинаково:
, но для разложения NaCl требуется перенос только половины электронов, чем для разложения CaO.Для электролиза NaCl ранее было рассчитано, что прохождение 20 фарадей электрического заряда дает 20 моль металлического натрия и 10 моль газообразного хлора. Такое же количество электрического заряда, проходящего через ячейку CaO, дает только 10 моль металлического кальция и 5 моль газообразного кислорода.
Полуреакция восстановления со сбалансированными коэффициентами:
Полуреакция окисления со сбалансированными коэффициентами:
- Металлический алюминий получают электролизом расплавленного криолита, Na 3 AlF 6 .

- Металлический алюминий получают электролизом расплавленного криолита, Na 3 AlF 6 .
