Закон Фарадея для электромагнитной индукции и для электролиза
Для описания процессов в физике и химии есть целый ряд законов и соотношений, полученных экспериментальным и расчетным путем. Ни единого исследования нельзя провести без предварительной оценки процессов по теоретическим соотношениям. Законы Фарадея применяются и в физике, и в химии, а в этой статье мы постараемся кратко и понятно рассказать о всех знаменитых открытиях этого великого ученого.
История открытия
Закон Фарадея в электродинамике был открыт двумя ученными: Майклом Фарадеем и Джозефом Генри, но Фарадей опубликовал результаты своих работ раньше – в 1831 году.
В своих демонстрационных экспериментах в августе 1831 г. он использовал железный тор, на противоположные концы которого был намотан провод (по одному проводу на стороны). На концы одного первого провода он подал питание от гальванической батареи, а на выводы второго подключил гальванометр. Конструкция была похожа на современный трансформатор.
Гальванометр — это высокочувствительный прибор для измерения силы токов малой величины.
Таким образом было изображено влияние магнитного поля, образовавшегося в результате протекания тока в первом проводе, на состояние второго проводника. Это воздействие передавалось от первого ко второму через сердечник – металлический тор. В результате исследований было обнаружено и влияние постоянного магнита, который двигается в катушке, на её обмотку.
Тогда Фарадей объяснял явление электромагнитной индукции с точки зрения силовых линий. Еще одной была установка для генерирования постоянного тока: медный диск вращался вблизи магнита, а скользящий по нему провод был токосъёмником. Это изобретение так и называется — диск Фарадея.
Ученные того периода не признали идеи Фарадея, но Максвелл взял исследования для основы своей магнитной теории. В 1836 г. Майкл Фарадей установил соотношения для электрохимических процессов, которые назвали Законами электролиза Фарадея.
Электродинамика
Первые работы применяются в физике, конкретно в описании работы электрических машин и аппаратов (трансформаторов, двигателей и пр.). Закон Фарадея гласит:
Для контура индуцированная ЭДС прямо пропорциональна величине скорости магнитного потока, который перемещается через этот контур со знаком минус.
Это можно сказать простыми словами: чем быстрее магнитный поток движется через контур, тем больше на его выводах генерируется ЭДС.
Формула выглядит следующим образом:
Здесь dФ – магнитный поток, а dt – единица времени. Известно, что первая производная по времени – это скорость. Т.е скорость перемещения магнитного потока в данном конкретном случае. Кстати перемещаться может, как и источник магнитного поля (катушка с током – электромагнит, или постоянный магнит), так и контур.
Здесь же поток можно выразить по такой формуле:
B – магнитное поле, а dS – площадь поверхности.
Если рассматривать катушку с плотнонамотанными витками, при этом в количестве витков N, то закон Фарадея выглядит следующим образом:
Магнитный поток в формуле на один виток, измеряется в Веберах. Ток, протекающий в контуре, называется индукционным.
Электромагнитная индукция – явление протекания тока в замкнутом контуре под воздействием внешнего магнитного поля.
В формулах выше вы могли заметить знаки модуля, без них она имеет слегка иной вид, такой как было сказано в первой формулировке, со знаком минус.
Знак минус объясняет правило Ленца. Ток, возникающий в контуре, создает магнитное поле, оно направлено противоположно. Это является следствием закона сохранения энергии.
Направление индукционного тока можно определить по правилу правой руки или буравчика, мы его рассматривали на нашем сайте подробно.
Как уже было сказано, благодаря явлению электромагнитной индукции работают электрические машины трансформаторы, генераторы и двигатели.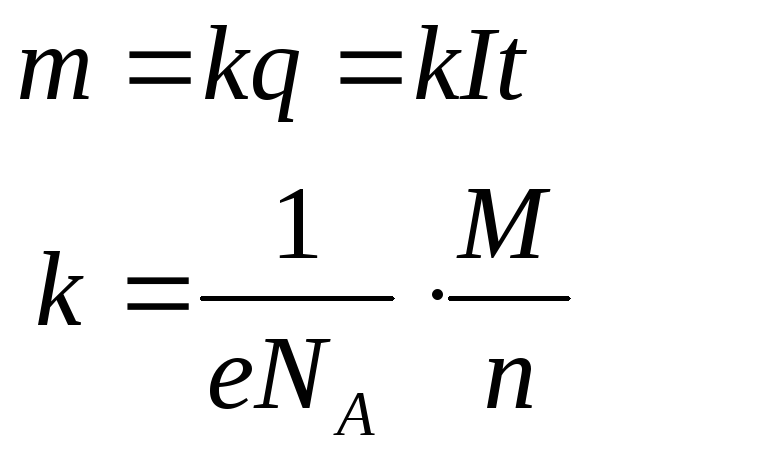 На иллюстрации показано протекание тока в обмотке якоря под воздействием магнитного поля статора. В случае с генератором, при вращении его ротора внешними силами в обмотках ротора возникает ЭДС, ток порождает магнитное поле направленное противоположно (тот самый знак минус в формуле). Чем больше ток, потребляемый нагрузкой генератора, тем больше это магнитное поле, и тем больше затрудняется его вращение.
На иллюстрации показано протекание тока в обмотке якоря под воздействием магнитного поля статора. В случае с генератором, при вращении его ротора внешними силами в обмотках ротора возникает ЭДС, ток порождает магнитное поле направленное противоположно (тот самый знак минус в формуле). Чем больше ток, потребляемый нагрузкой генератора, тем больше это магнитное поле, и тем больше затрудняется его вращение.
И наоборот — при протекании тока в роторе возникает поле, которое взаимодействует с полем статора и ротор начинает вращаться. При нагрузке на вал ток в статоре и в роторе повышается, при этом нужно обеспечить переключение обмоток, но это уже другая тема, связанная с устройством электрических машин.
В основе работы трансформатора источником движущегося магнитного потока является переменное магнитное поле, возникающее в следствие протекания в первичной обмотке переменного тока.
Если вы желаете более подробно изучить вопрос, рекомендуем просмотреть видео, на котором легко и доступно рассказывается Закон Фарадея для электромагнитной индукции:
Электролиз
Кроме исследований ЭДС и электромагнитной индукции ученный сделал большие открытия и в других дисциплинах, в том числе химии.
При протекании тока через электролит ионы (положительные и отрицательные) начинают устремляться к электродам. Отрицательные движутся к аноду, положительные к катоду. При этом на одном из электродов выделяется определенная масса вещества, которое содержится в электролите.
Фарадей проводил эксперименты, пропуская разный ток через электролит и измеряя массу вещества отложившегося на электродах, вывел закономерности.
m=k*Q
m – масса вещества, q – заряд, а k – зависит от состава электролита.
А заряд можно выразить через ток за промежуток времени:
I=q/t, тогда q = i*t
Теперь можно определить массу вещества, которое выделится, зная ток и время, которое он протекал. Это называется Первый закон электролиза Фарадея.
Это называется Первый закон электролиза Фарадея.
Второй закон:
Масса химического элемента, который осядет на электроде, прямо пропорциональна эквивалентной массе элемента (молярной массе разделенной на число, которое зависит от химической реакции, в которой участвует вещество).
С учетом вышесказанного эти законы объединяются в формулу:
m – масса вещества, которое выделилось в граммах, n – количество переносимых электронов в электродном процессе, F=986485 Кл/моль – число Фарадея, t – время в секундах, M молярная масса вещества г/моль.
В реальности же из-за разных причин, масса выделяемого вещества меньше чем расчетная (при расчетах с учетом протекающего тока). Отношение теоретической и реальной масс называют выходом по току:
Bт = 100% * mрасч/mтеор
Ну и напоследок рекомендуем просмотреть подробное объяснение закона Фарадея для электролиза:
Законы Фарадея внесли существенный вклад в развитие современной науки, благодаря его работам мы имеем электродвигатели и генераторы электроэнергии (а также работам его последователей). Работа ЭДС и явления электромагнитной индукции подарили нам большую часть современного электрооборудования, в том числе и громкоговорители и микрофоны, без которых невозможно прослушивание записей и голосовая связь. Процессы электролиза применяются в гальваническом методе покрытия материалов, что несет как декоративную ценность, так и практическую.
Похожие материалы:
Электролиз. Законы Фарадея.
Взаимное превращение электрической м химической энергии происходит в электрохимических системах, состоящих из следующих частей:
1. Проводники II рода;
2. Проводники I рода – металлические электроды. Положительный электрод называется анодом, отрицательный – катодом.
3. Проводники I рода – внешняя электрическая цепь, связывающая электроды.
Электролиз – это химическое превращение в электрической системе под действием внешнего электрического поля.
При электролизе отрицательные ионы движутся к аноду (+) – анионы. Положительно заряженные частицы – катионы – двигаются к катоду.
Вещества, которые в растворе (или расплаве) состоят полностью или частично из ионов называются электролитами.
Представим систему, в которой имеется раствор медного купороса (CuSO4 + H2O). При растворении в воде электролита происходит диссоциация на ионы
CuSO4 ⇆ Сu2+ + SO42-
При погружении в раствор электродов (катода и анода) начинается направленное движение ионов.
На катоде происходит восстановление меди по реакции:
Cu2+ + 2e → Cu0
и выделяется на нем металлическая медь.
Соотношение между (количеством) массой прореагировавших веществ и количеством постоянного электрического выражается законами Фарадея.
I закон Фарадея: Масса вещества m претерпевшего химическое превращение под действием электрического тока пропорциональна количеству протекшего электрического тока.
, где (2.1)
m – масса вещества;
J – сила тока;
τ – время электролиза
Kэ – электрохимический эквивалент.
– количество электричества.
=[кулон]
II закон Фарадея: При прохождении через различные электролиты одного и того же количества электричества массы различных веществ, участвующих в реакциях, пропорциональны их химическим эквивалентам.
Для выделения 1 г –экв. любого вещества требуется пропустить 1 Фарадей электричества.
1 Фарадей = 1F = 96500 Кл
(2.2)
Э – химический эквивалент, ;
M – мольная масса вещества;
z – число , принимающих участие в электродной реакции.
, (2.3)
тогда – электрохимический эквивалент
II закон Фарадея дает физический смысл Kэ: Кэ – это количество вещества, которое претерпевает превращение при пропускании через раствор 1 Кл электричества.
На практике часто наблюдается отклонение от законов Фарадея вследствие протекания побочных реакций; а именно:
1). в электролитах, содержащих кислоты, происходит дополнительно восстановление водорода (кислота увеличивает электропроводность)
Например: электролит ZnSO4 + H2SO4
на катоде(-):
Zn2+ + 2e → Zn0 – основная
2Н+ + 2е→H2 ↑– побочная
2). Неполное восстановление металла на катоде:
Fe3+ + 3e→ Fe0
Fe3+ + 1e→ Fe2+
3). Наличие нескольких реакций восстановления на катоде:
Au3+ + 3e→ Au0 – основная
Au1+ + 1e→ Au0 — побочная
4). Взаимодействие продуктов электролиза с электролитом:
Взаимодействие продуктов электролиза с электролитом:
H2O + NaCl
H2O ⇆ H+ + OH—
Ионы щелочных металлов не восстанавливаются, на катоде идет восстановление водорода:
(-) 2H2+ + 2e = H2↑
В прикатодном пространстве накапливаются ионы натрия, в прианодном — ионы гидроксила
На аноде идет окисление CI— ионов:
(+) 2CI− — 2e →CI2↑ выделяется газ.
Образующаяся NaOH взаимодействует с CI2:
2NaOH + CI2 = NaCI + NaCIO + H2O
Эффективность электрохимического процесса оценивается величиной выхода по току
(2.4)
В отсутствии побочных процессов ψ =1, но на самом деле ψ < 1.
Похожие статьи:
что это, формулировка, границы применимости
История открытия закона Фарадея
Майкл Фарадей – английский ученый физик, проводивший опыты с электричеством. До открытия Фарадея считалось, что между магнитным и электрическим полями нет никакой связи. Фарадей обосновал доказательство того, что магнитное поле вызывает электрический ток. Это явление получило название электромагнитной индукции, а закон стал одним из основных в электродинамике.
До открытия Фарадея считалось, что между магнитным и электрическим полями нет никакой связи. Фарадей обосновал доказательство того, что магнитное поле вызывает электрический ток. Это явление получило название электромагнитной индукции, а закон стал одним из основных в электродинамике.
Фарадей был не единственным ученым, который задумался о связи электрического и магнитного поля. Одновременно с ним над этими явлениями работал Джозеф Генри. Но Фарадей все-таки первым сформулировал и опубликовал результаты своих исследований.
Электромагнитная индукция – появление электрического тока, поля или электрической поляризации в условиях изменения во времени магнитного поля или при движении материальной среды в нем.
К своему открытию Фарадей шёл порядка десяти лет. В 1831 году ученый провел эксперимент, позволивший ему открыть элеткромагнитную индукцию. Он намотал на один железный сердечник две катушки, автономные друг от друга. Одна катушка была подключена к источнику тока, вторая к гальванометру – прибору, измеряющему силу тока. Когда по первой катушке шел электрический ток, ее магнитное поле возрастало. В это же время гальванометр, подключённый ко второй катушке, фиксировал возникновение в ней тока. Таким образом, Фарадей доказал, что в результате влияния магнитного поля, появляется ток. Такой ток стали называть индукционным. Но появлялся он только в момент подключения или отключения первой катушки от цепи. Если по первой катушке шел постоянный ток, то во второй в это время ничего не регистрировалось.
Когда по первой катушке шел электрический ток, ее магнитное поле возрастало. В это же время гальванометр, подключённый ко второй катушке, фиксировал возникновение в ней тока. Таким образом, Фарадей доказал, что в результате влияния магнитного поля, появляется ток. Такой ток стали называть индукционным. Но появлялся он только в момент подключения или отключения первой катушки от цепи. Если по первой катушке шел постоянный ток, то во второй в это время ничего не регистрировалось.
«Электрический магнетизм» проявлялся и в тот момент, когда Фарадей передвигал вторую катушку относительно первой. Сила индукционного тока увеличивалась, если движение катушки было быстрым, и наоборот.
Затем Фарадей заменил первую катушку на магнит, который вводил во вторую катушку. Явление электромагнитной индукции повторилось в точности как в опыте с двумя катушками.
Фарадей пришел к выводу, что возникновение индукционного тока зависит от количества линий магнитного поля, которые проходят сквозь контур.
Формула закона Фарадея
Проводя опыты с катушками и магнитом, Фарадей обнаружил, что величина электродвижущей силы зависит от скорости перемещения катушек или магнита. Это позволило ему выявить закономерность и сформулировать закон электромагнитной индукции.
Закон электромагнитной индукции: электродвижущая сила пропорциональна скорости изменения магнитного потока, проходящего через контур.
Формулировка закона выглядит следующим образом: Ε=-ΔΦ/Δt
ПримечаниеE в этой формуле – электродвижущая сила, ΔΦ – изменение магнитного потока, а Δt – время, за которое изменяется магнитный поток. Единицы измерения ЭДС – вольты, магнитного потока – веберы. Δ – разница между конечным и начальным параметром.
В выражении закона Фарадея стоит минус. Он подразумевает применение к этому закону правила Ленца.
ПримечаниеЭ. Х. Ленц – российский физик, основоположник электротехники. Сформулировал правило индукционного тока в 1833 году.
Правило Ленца добавляет к закону пояснение, что ток, образовавшийся в результате индукции, всегда имеет противоположное направление образующему его магнитному потоку. Магнитное поле индукционного тока всегда препятствует магнитному потоку из внешнего источника. Суть правила очень близка закону сохранения энергии.
Применение закона Фарадея
Закон Фарадея позволил создать такие устройства и приборы как электродвигатели, трансформаторы, генераторы переменного тока, индукционные печи, дроссели, электросчетчики. Принцип действия всех этих устройств основан на электромагнитной индукции.
НапримерТрансформаторы передают энергию переменного электромагнитного поля за счет явления взаимной индукции, таким образом трансформируя величину напряжения на разных клеммах.
Примеры решения задач
1. В однородном магнитном поле, индукция которого 1 Тл, имеется плоский проводящий виток, площадь которого равна 100 см2. Виток расположен перпендикулярно линиям магнитного потока. Сопротивление витка равно 200 мОм. Какой заряд протечет через поперечное сечение витка, если не станет поля?
Виток расположен перпендикулярно линиям магнитного потока. Сопротивление витка равно 200 мОм. Какой заряд протечет через поперечное сечение витка, если не станет поля?
При исчезновении магнитного поля изменится магнитный поток через виток:
ΔФ = ΔВS cos α; ΔB = B, α = 0°, cos α = 1. Тогда ΔФ = BS.
После изменения магнитного потока в контуре появится ЭДС индукции:
2. Концы катушки из тысячи витков радиусом 5 см замкнуты накоротко. Сопротивление катушки 100 Ом. С какой скоростью должна изменяться индукция магнитного поля, перпендикулярного плоскости катушки, чтобы в ней выделялась тепловая мощность 100 мВт.
По закону электромагнитной индукции
3. Провод длиной 2 м складывают пополам и замыкают концы. После этого провод растягивают в квадрат, плоскость которого перпендикулярна силовым линиям магнитного поля с индукцией 64 мкТл. Какое количество электронов пройдет при этом через поперечное сечение провода, если его сопротивление 10 мОм? Вначале площадь контура была равна 0. При растягивании провода в квадрат его площадь стала равна S = a2, где a = L/4. Когда изменится площадь, поменяется магнитный поток через контур ΔФ = B ΔS = BL2/16.
Какое количество электронов пройдет при этом через поперечное сечение провода, если его сопротивление 10 мОм? Вначале площадь контура была равна 0. При растягивании провода в квадрат его площадь стала равна S = a2, где a = L/4. Когда изменится площадь, поменяется магнитный поток через контур ΔФ = B ΔS = BL2/16.
Законы электролиза Фарадея
Первый закон Фарадея
Как уже известно, при электролизе на электродах происходит выделение вещества. Попробуем выяснить, от чего будет зависеть масса это вещества. Масса выделившегося вещества m будет равна произведению массы одного иона m0i на число ионов Ni, которые достигли электрода за промежуток времени равный ∆t: m = m0i*Ni. Масса иона m0i будет вычисляться по следующей формуле:
где М — молярная масса вещества, а Na — постоянная Авогадро.
Число ионов, которые достигнут электрода, вычисляется по следующей формуле:
где ∆q = I*∆t — заряд, прошедший через электролит за время, равное ∆t, q0i — заряд иона.
Для того, чтобы определить заряд иона, используется следующая формула:
где n — валентность, e — элементарный заряд.
Собирая воедино все представленные формулы, получаем формулу для вычисления массы выделившегося на электроде вещества:
Теперь обозначим через k коэффициент пропорциональности между массой вещества и зарядом ∆q.
Этот коэффициент k будет зависеть от природы вещества. Тогда формулу массы вещества можно переписать в следующем виде:
Второй закон Фарадея
Масса вещества, выделившегося на электроде за время, равное ∆t, при прохождении электрического тока пропорциональна силе тока и времени. Коэффициент k называют электрохимическим эквивалентом данного вещества. Единицей измерения служит кг/Кл. Разберемся с физическим смыслом электрохимического эквивалента. (-19) Кл.
(-19) Кл.
Именно таким способом было впервые получено значение элементарного электрического заряда.
Нужна помощь в учебе?
Предыдущая тема: Электрический ток в жидкостях: ионная проводимость и электролиз
Следующая тема:   Электрический ток в газах: опыт и проводимость газа
Законы электролиза Фарадея — Энциклопедия по машиностроению XXL
По закону электролиза Фарадея, количество электричества е, прошедшего через элемент, пропорционально числу п прореагировавших молей электролита и валентности Z иона, переносящего заряд [c.180]Из объединенного закона электролиза Фарадея-. [c.231]
Электрохимическая обработка металлов основывается на законах электролиза, установленных Фарадеем, и на явлении поляризации. Закон Фарадея количественно выражается уравнением [c.59]
Второй закон Фарадея (второй закон электролиза) [c.
 97]
97]Прохождение тока через растворы электролитов сопровождается переносом вещества. Явления, имеющие место при прохождении тока, подчиняются особым законам электролиза, открытым Фарадеем. [c.16]
Еще Фарадеем были исследованы законы электролиза, причем была обнаружена сугубо линейная зависимость количества ионов, выделившихся из растворов на электродах, от величины электрического заряда, прошедшего через раствор. [c.155]
Г. Первый закон электролиза первый закон Фарадея) масса вещества, выделяющегося на электроде, прямо пропорциональна электрическому заряду д, прошедшему через электролит [c.230]
Второй закон электролиза второй закон Фарадея) электрохимические эквиваленты веществ прямо пропорциональны отношениям их атомных (молярных) масс А к валентности т [c.230]
При протекании тока через электропроводные жидкие растворы (электролиты) происходит процесс электролиза, подчиняющийся законам М. Фарадея. В зависимости от конкретных условий могут наблюдаться такие процессы, как осаждение на катоде тех или иных металлических элементов, входящих в состав электролита, образование на аноде окисных пленок, растворение металла анода и др.
[c.212]
Фарадея. В зависимости от конкретных условий могут наблюдаться такие процессы, как осаждение на катоде тех или иных металлических элементов, входящих в состав электролита, образование на аноде окисных пленок, растворение металла анода и др.
[c.212]
ФАРАДЕЯ ЗАКОНЫ электролиза, см. Электро.гиз. [c.802]
Электролитические металлические покрытия получают в растворах соответствующих солей путем электролиза. Это покрытия из меди, цинка, кадмия, никеля, хрома, золота или комбинаций металлов. Осаждение металлов протекает по закону Фарадея, который заключается в том, что количество веществ, осажденных или растворенных на электродах, прямо пропорционально их электрохимическим эквивалентам. [c.74]
Кулонометрический метод. Принцип этого электрохимического метода определения толщины, заключающийся в анодном растворении металла на известной площади с измерением электрического заряда, потребляемого в данном процессе, противоположен принципу электроосаждения. С учетом площади, на которой происходит электролиз, и электрохимического эквивалента металла по закону Фарадея делается простой расчет количество электричества в кулонах, расходуемое в процессе, переводится в толщину растворенного покрытия. Для получения точных результатов расчета необходимо, чтобы растворение происходило с известным постоянным выходом по току на аноде (желательно 100%-ным). Выбранный электролит должен устранить возможность возникновения эффектов пассивации или избыточной поляризации и, кроме того, не оказывать химического воздействия на покрытие при отсутствии электрического тока. Разумеется, важно точно определить площадь анода.
[c.144]
С учетом площади, на которой происходит электролиз, и электрохимического эквивалента металла по закону Фарадея делается простой расчет количество электричества в кулонах, расходуемое в процессе, переводится в толщину растворенного покрытия. Для получения точных результатов расчета необходимо, чтобы растворение происходило с известным постоянным выходом по току на аноде (желательно 100%-ным). Выбранный электролит должен устранить возможность возникновения эффектов пассивации или избыточной поляризации и, кроме того, не оказывать химического воздействия на покрытие при отсутствии электрического тока. Разумеется, важно точно определить площадь анода.
[c.144]
Особенности процесса электролиза определяются объединенным законом Фарадея количество вещества М, выделяющегося на электроде, пропорционально перенесенному заряду q [c.211]
Первый закон Фарадея устанавливает, что количество выделившегося при электролизе вещества прямо пропорционально количеству электричества, пропущенному через электролит (прямо пропорционально силе тока и времени его действия). [c.8]
[c.8]
Дк — катодная плотность тока, а/дм . Как уже указывалось, в период разгона катодная плотность тока меняется обычно с 3—5 а/дм до 40—50 а/дм . Расчет времени электролиза. Согласно законам Фарадея [c.65]
Как и любой электрохимический процесс, электролиз алюминия в расплавленных электролитах подчиняется закону Фарадея, согласно которому теоретически для выделения 1 моля алюминия, равного 27 3 9 г, требуется 26,8 А-ч электричества, или 1 А-ч выделяет 0,336 г алюминия. Величина 0,336 г/(А-ч) называется электрохимическим эквивалентом алюминия. [c.350]
Основные процессы и параметры ЭХО. Основным электрохимическим процессом ЭХО является процесс растворения анода. Линейная скорость растворения, характеризующая производительность ЭХО, определяется из первого закона Фарадея. После ряда преобразований, учитывающих реальный процесс электролиза, уравнение для линейной скорости растворения анода принимает следующий вид
[c. 605]
605]
Выход по току — коэффициент полезного использования тока определяется как отношение количества алюминия, практически наработанного в процессе электролиза, к количеству алюминия, которое должно было выделиться в соответствии с законами Фарадея. Обычно выход по току (Рг) выражается в процентах и характеризуется зависимостью [c.235]
Анализ процесса электрохимической обработки. Основные соотношения для скорости удаления металла в процессе электрохимической обработки могут быть выведены из законов Фарадея для электролиза. [c.319]
Если обозначить через W — массу выделившегося или растворившегося вещества, через / — ток и т — продолжительность электролиза, то закон Фарадея можно выразить следующим математическим соотношением [c.14]
Во времена Фарадея никому не пришла мысль воспользоваться открытыми им законами электролиза для выяснения природы электричества. Интерес к ним возродился в конце столетия в связи с успехами атомно-молекулярной теории. Законы электролиза легко интерпретировались, если предположить, что в растворе, например, Na l в воде с каждым атомом связан определенный заряд, причем эти заряды одинаковы и противоположны по знаку Na» и С1 . Тогда при прохождении через раствор одного и того же количества электричества, равного 96484 Кл. на электродах выделится по молю вещества, т. е. по Л а = 610 атомов.
[c.98]
Законы электролиза легко интерпретировались, если предположить, что в растворе, например, Na l в воде с каждым атомом связан определенный заряд, причем эти заряды одинаковы и противоположны по знаку Na» и С1 . Тогда при прохождении через раствор одного и того же количества электричества, равного 96484 Кл. на электродах выделится по молю вещества, т. е. по Л а = 610 атомов.
[c.98]
Механизм прохождения тока в металлах — как в твердом, так и в жидком состоянии — обусловлен движением (дрейфом) свободных электронов под воздействием электрического поля поэтому металлы называют проводниками с электронной электропроводностью или проводниками первого рода. Проводниками второго рода, или электролитами, являются растворы (в частности, водные) кислот, щелочей и солей. Прохождение тока через эти вещества связано с переносом вместе с электрическими зарядами ионов в соответствии с закона . и Фарадея, вследствие чего состав электролита постепенно изменяется, а на электродах выделяются продукты электролиза. Ионные кристаллы в расплавленном состоянии также являются проводниками второго рода. Пр1 мером. могут служить соляные закал .ч-ные ванны с злектронагревом.
[c.187]
Ионные кристаллы в расплавленном состоянии также являются проводниками второго рода. Пр1 мером. могут служить соляные закал .ч-ные ванны с злектронагревом.
[c.187]
Ф. п. применяется в электрохим. расчётах. Названа в честь М. Фарадея (М. Faraday), открывшего осн. законы электролиза. Значение F определялось на основе измерений эл.-хим. эквивалента серебра. [c.275]
При восстановлении изношенных деталей используют закономерности электрохимических процессов, относящиеся к превращению электрической энергии в химическую. К ним относятся законы электролиза, термодинамические и кинетические закономерности электрохимических процессов. Теоретическое значение массы вещества т (в фаммах), выделившегося на электроде, определяется с помощью объединенного закона М. Фарадея [c.408]
Исключительное значение для обоснования электрохимического механизма коррозии имели работы выдающихся ученых Деви и Фарадея, устан01вивших законы электролиза, швейцарского химика Де-ля-Рива, объяснившего растворение цинка в кислоте действием микро-гальваничес ких элементов, русских физико-химиков Н. Н. Бекетова, исследо1вавшего в 1865 г, явления вытеснения из растворов одних металлов другими, и Н. Н. Каяндера, пришедшего в 1881 г. к выводу, что растворенные вещества распадаются на составные части, а также шведского химика Аррениуса, сформулировавшего в 1887 г. теорию электролитической диссоциации, и немецкого физико-химика Нернста, опубликовавшего в 1888 г. теорию электродных и диффузионных потенциалов.
[c.5]
Н. Бекетова, исследо1вавшего в 1865 г, явления вытеснения из растворов одних металлов другими, и Н. Н. Каяндера, пришедшего в 1881 г. к выводу, что растворенные вещества распадаются на составные части, а также шведского химика Аррениуса, сформулировавшего в 1887 г. теорию электролитической диссоциации, и немецкого физико-химика Нернста, опубликовавшего в 1888 г. теорию электродных и диффузионных потенциалов.
[c.5]
Исключительное значение для обоснования электрохимического механизма коррозии имели работы выдающегося английского ученого М. Фарадея, установившего законы электролиза, швейцарского химика А. Де-ля-Рива, объяснившего растворение цинка в кислоте действием микрогальванических элементов, русских фи-зико-химиков Н. Н. Бекетова, исследовавшего в 1865 г. явления вытеснения из растворов одних металлов другими и И. Н. Каян-дера, пришедшего в 1881 г. к выводу, что растворенные вещества распадаются на составные части, а также шведского химика
[c. 9]
9]
Важным вкладом в развитие теории электрохимической коррозии были работы английского ученого Фарадея, установившего основные законы электролиза и выдвинувшего, для объяснении явления пассивности металлов, гипотезу о существовании тонкой невидимой пленки, и швейцарского ученого Де Ла Рива, выдвинувшего гипотезу о существовании микрогальваниче-ского элемента. [c.50]
Фарадей (Faraday) Майкл (1791-1867) — английский физик, основоположник учения об электромагнитном поле. Учился самостоятельно. Ввел основные понятия электромагнитного поля, высказал идею существования электромагнитных волн. Идею электромагнитного поля А. Эйнштейн рассматривал как самое важное открытие со времен Ньютона и в связи с этим писал Надо иметь могучий дар научного предвидения, чтобы распознать, что в описании электрических явлений не заряды и не частицы описывают суть явлений, а скорее пространство между зарядами и частицами . Открыл электромагнитную индукцию. Установил законы электролиза, названные его именем, открыл вращение плоскости поляризации света в магнитном поле (эффект Фарадея). Ввел понятие диэлектрической проницаемости, экспериментально доказал закон сохранения электрического заряда.
[c.28]
Ввел понятие диэлектрической проницаемости, экспериментально доказал закон сохранения электрического заряда.
[c.28]
Электролиз, Фарадея законы). Наиболее точные непосредственные определения Ф. ч. были выполнены при электроосаждении Ag из раствора AgNOj и выделении J электроокислением растворенного KJ. Ф. ч. F равно произведению величины заряда одновалентного иона (равного заряду электрона) на число ионов в 1 г-экв или молекул в 1 г-мол Авогадро число). В углеродной шкале атомных весов F = 96 491,4 1,1 кулон г-экв. [c.292]
Объем растворенямч) при электролизе металла (расчетный) Т согласяо первому закону М. Фарадея определяется формулой [c.5]
Второй закон М. Фарадея определяет, что массы различных-нетал выделпшиеся в результате электролиза при про хождеияя [c.5]
Электролитический метод восстановления деталей. Электролитический метод восстановления деталей оснп-ван на законах электролиза. Электролиз представляет собой процесс, протекающий в электролитах при пропускании через них электрического тока. Процесс электролитического нанесения металла подчиняется закону Фарадея и определяется по формуле
[c.209]
Электролиз представляет собой процесс, протекающий в электролитах при пропускании через них электрического тока. Процесс электролитического нанесения металла подчиняется закону Фарадея и определяется по формуле
[c.209]
Электродвижущая сила и КПД топливного элемента. Процесс в гальваническом, а следовательно, и в топливном элементе может считаться обратимьш, если протекающий в замкнутой цепи электрический ток достаточно мал, т. е. внешнее сопротивление велико (при этом джоулева теплота, пропорциональная квадрату плотности тока f, пренебрежимо мала по сравнению с полезной работой, пропорциональной / другие источники необратимости здесь не рассматриваются). В этом случае полезная внешняя работа макс (отнесенная к единице площади рабочей поверхности элемента) за время т равна произведению электродвижущей силы е на электрический заряд — /т, протекающий через элемент акс = вр . По законам электролиза = Fa MZ, где М — число ионов, переносящих заряд Z — валентность иона Fa — коэффициент пропорциональности, называемый константой Фарадея (96 540 кулон моль). Таким образом, макс = Fa MZ. Но согласно уравнению -Тиббса— Гельмгольца при Т = onst, р — onst акс = Л — /2 + + Т ( акс/ Лр.
[c.172]
Таким образом, макс = Fa MZ. Но согласно уравнению -Тиббса— Гельмгольца при Т = onst, р — onst акс = Л — /2 + + Т ( акс/ Лр.
[c.172]
Ф. п. широко применяется в электрохимических расчётах. Названа в честь М. Фарадея, открывшего основные законы электролиза. Значение F определялось на основе измерений электрохим. эквивалента серебра. ФАРАДЕЯ ЭФФЕКТ, один из эффектов магнитооптики. Заключается во вращении плоскости поляризации линейно поляризов. света, распространяющегося в в-ве вдоль пост. магн. поля, в к-ром находится это в-во. Открыт М. Фарадеем в 1845 и явился первым доказательством прямой связи оптич. и эл.-магн. явлений. [c.802]
Электроосаждение металлов происходит по законам Фарадея масса металла, образующегося при электролизе, прямо пропорциональна количеству электричества, пропускаемого через раствор, и химическому эквиваленту металла. Из этого следует, что среднюю толщину осаждаемого покрытия данного металла можно легко вычислить, зная силу тока, время нанесе-
[c. 86]
86]
Коэфициент полезного действия иногда выражается в %%-х. Фактический вес осадка определяеткя обычно взвешиванием катода до и после электролиза, а теоретический вес осадка рассчитывается по законам Фарадея. [c.18]
Количество алюминия, выделяющееся при электролизе криолито-глиноземных расплавов, в соответствии с законами Фарадея определяется зависимостью [c.235]
При электролитическом осаждении металла электрическая энергия расходуется на работу передвижения и разряда ионов на электродах. Протекающие при электролизе процессьГколиче-ственно определяются двумя общеизвестными законами Фарадея. Чтобы присутствующий в водном растворе ион мог разрядиться на электроде, потенциал последнего должен быть выше потенциала выделения ука занного иона. Потенциал разряда металла равен [c.212]
Катионы легких элементов, располагаясь между атомами металлов, стягивают коллективизированные электроны и частично перекрываются с внешними s-орбиталями соседних металлических атомов, поэтому их номинальные заряды, отвечающие числу коллективизированных электронов (В » , 0 » ), понижаются до малых эффективных реальных значений, несколько различающихся при растворении в разных металлах. Соблюдение закона Фарадея при электролизе подтверждает целочисленность зарядов металлических ионов. Исследование электропереноса и многие другие данные указывают на положительный знак зарядов на примесях внедрения, т. е. на образование в металлических растворах катионов N» , О , В . Реальные заряды на катионах легких элементов есть следствие коллективизации их валентных электронов и последующего стягивания к ним электронного газа, что ведет к поляризации многозарядных ионов, приводящей к сильному уменьшению их номинального заряда до малых реальных эффективных значений.
[c.84]
Соблюдение закона Фарадея при электролизе подтверждает целочисленность зарядов металлических ионов. Исследование электропереноса и многие другие данные указывают на положительный знак зарядов на примесях внедрения, т. е. на образование в металлических растворах катионов N» , О , В . Реальные заряды на катионах легких элементов есть следствие коллективизации их валентных электронов и последующего стягивания к ним электронного газа, что ведет к поляризации многозарядных ионов, приводящей к сильному уменьшению их номинального заряда до малых реальных эффективных значений.
[c.84]
Для многих электроизоляционных материалов характерна ионная электропроводность, связанная с переносом ионов, т.е. явлением электролиза. В ряде случаев электролизу при прохождении через диэлектрик сквозного тока утечки подвергается основное вещество дн-электрика примером может служить обычное стекло, в котором благодаря его прозрачности можно непосредственно наблюдать образование и перенос продуктов электролиза при про-кускании постоянного тока через стекло, нагретое для повышения проводимости (см. ниже), у катода образуются древовидные отложения деядриты) входящих в состав молекул стекла металлов, прежде всего натрия. Еще чаще (по крайней мере, для органических электроизоляционных материалов) встречаются такие случаи, когда молекулы основного вещества диэлектрика не обладают способностью подвергаться диссоциации, но ионная электропроводность возникает благодаря присутствию в материале практически неизбежных загрязнений— примесей воды, солей, кислот, щелочей и пр. Даже весьма малые примеси способны заметно влиять на проводимость диэлектрика поэтому в технике электрической изоляции важное значение имеет чистота исходных продуктов и чистота рабочего места. У диэлектриков с ионным характером электропроводности соблюдаются законы Фарадея количество выделившегося при электролизе вещества пропор-1 ионально количеству прошедшего через материал электричества.
[c.20]
ниже), у катода образуются древовидные отложения деядриты) входящих в состав молекул стекла металлов, прежде всего натрия. Еще чаще (по крайней мере, для органических электроизоляционных материалов) встречаются такие случаи, когда молекулы основного вещества диэлектрика не обладают способностью подвергаться диссоциации, но ионная электропроводность возникает благодаря присутствию в материале практически неизбежных загрязнений— примесей воды, солей, кислот, щелочей и пр. Даже весьма малые примеси способны заметно влиять на проводимость диэлектрика поэтому в технике электрической изоляции важное значение имеет чистота исходных продуктов и чистота рабочего места. У диэлектриков с ионным характером электропроводности соблюдаются законы Фарадея количество выделившегося при электролизе вещества пропор-1 ионально количеству прошедшего через материал электричества.
[c.20]
Методическая разработка по теме Электролиз. Законы Фарадея. 11 класс профильный уровень
Физика 11 класс профильный уровень.
Методическая разработка к уроку по физике по теме: Электролиз.
Цели урока:
Оборудование: аппарат электролизер, гальванометр, источник постоянного электрического тока, соединительные провода.
Электролиз – совокупность процессов, происходящих при прохождении электрического тока через электрохимическую систему, состоящую из двух электродов и расплава или раствора электролита.
Для осуществления электролиза к отрицательному полюсу внешнего источника тока присоединяют катод, а к положительному – анод и погружают их в электролит. При прохождении тока через электролит катионы под действием электрического поля движутся к катоду, а анионы – положительному электроду – аноду. Например, при электролизе расплава MgCl2 катионы магния, подойдя к катоду, взаимодействуют с приходящими по внешней цепи электронами, восстанавливаются:
К «-» Mg2+ + 2е— → Mg.
Анионы хлора перемещаются к положительному электроду и, отдавая избыточные электроны, окисляются. При этом первичным процессом является окисление ионов хлора:
А «+» 2Cl— – 2е— > 2Cl0 ,
а вторичным – связывание образующихся атомов хлора в молекулы 2Cl → Cl2.
Складывая уравнения электродных процессов, получим суммарное уравнение окислительно-восстановительной реакции, протекающей при электролизе расплава MgCl2:
Mg2+ + 2Cl— → Mg + Cl2.
Эта реакция не может протекать самопроизвольно, энергия необходимая для ее осуществления, поступает от внешнего источника тока. В ходе этой реакции электрическая энергия превращается в химическую.
Другими словами электролиз включает два процесса: миграцию реагирующих частиц под действием электрического поля к поверхности электрода и переход заряда с частицы на электрод или с электрода на частицу. Миграция ионов определяется их подвижностью и числами переноса. Процесс переноса нескольких электрических зарядов осуществляется, как правило, в виде последовательности одноэлектродных реакций, т.е. постадийно, с образованием промежуточных частиц (ионов или радикалов), которые некоторое время могут существовать на электроде в адсорбированном состоянии.
Миграция ионов определяется их подвижностью и числами переноса. Процесс переноса нескольких электрических зарядов осуществляется, как правило, в виде последовательности одноэлектродных реакций, т.е. постадийно, с образованием промежуточных частиц (ионов или радикалов), которые некоторое время могут существовать на электроде в адсорбированном состоянии.
Скорости электродных реакций зависят от состава и концентрации электролита, материала электродов, электродного потенциала, температуры и гидродинамических условий. Мерой скорости служит плотность тока – это количество переносимых электрических зарядов через единицу площади поверхности электрода в единицу времени.
При рассмотрении электролиза водных растворов необходимо помнить, что кроме ионов электролита во всяком водном растворе есть еще ионы Н+ и ОН— — продукты диссоциации воды. В электрическом поле ионы Н+ перемещаются к катоду, а ионы ОН— к аноду. Таким образом, у катода могут разряжаться как катионы электролита, так и катионы водорода. У анода может происходить разряд как анионов электролита, так и гидроксид ионов. Кроме того, молекулы воды также могут подвергаться электрохимическому окислению или восстановлению. Из нескольких возможных процессов будет протекать тот, осуществление которого сопряжено с минимальными затратами энергии.
Таким образом, у катода могут разряжаться как катионы электролита, так и катионы водорода. У анода может происходить разряд как анионов электролита, так и гидроксид ионов. Кроме того, молекулы воды также могут подвергаться электрохимическому окислению или восстановлению. Из нескольких возможных процессов будет протекать тот, осуществление которого сопряжено с минимальными затратами энергии.
Рассмотрим последовательность разряда ионов при электролизе водных растворов электролитов.
Рассмотрим электролиз раствора сульфата калия с графитовыми электродами:
K2SO4 → 2K+ + SO4 2-
(H2O)
«–» Катод ← К+ SO42- → Анод «+»
H2O H2O
φ0 K+ / K = -2,925В < φ0Al+ / Al , следовательно, ионы К+ относятся 1-ой группе катионов и на катоде происходит выделение водорода:
К «-» 4Н2О +4е— → 4Н0 + 4ОН— – первичный процесс;
4Н → 2Н2 – вторичный процесс.
Анод из графита окислению не подвергаются. В растворе присутствуют ионы SO42- , которые также не будут подвергаться электрохимическому окислению. Происходит выделение кислорода:
А «+» 2Н2О – 4е— → 4Н+ – 2О— – первичный процесс;
2О → О2 – вторичный процесс.
На катоде выделится водород, а на аноде – кислород, следовательно происходит электрохимическое разложение воды. Вблизи катода образуется гидроксид калия, а вблизи анода – серная кислота.
Демонстрация электролиза водного раствора хлорида меди
Ученики наблюдают выделение чистой меди и газообразного хлора на электродах при прохождении постоянного тока через раствор.
а) уравнения электролитической диссоциации (образование ионов в растворе):
CuCl2 <=> Cu2+ + 2Cl–
H2O = H+ + ОН–
б) восстановительные процессы на катоде (К–):
Cu2+ + 2e– = Cu0
в) окислительные процессы на аноде (А+):
2Сl– – 2e– = 2Cl0
г) суммарное уравнение электролиза:
CuCl2 + H2O = Сu + Cl2 + H2O
CuCl2 <=> Сu2+ + 2Cl–
Из описанного выше видно, что прохождение электрического тока через электролиты сопровождается химическими превращениями вещества и выделением газообразного хлора на аноде и чистой меди – на катоде.
3) Ученик на доске под руководством учителя химии составляет уравнение электролиза водного раствора сульфата меди.
Или:
CuSO4 <=> Cu2+ + SO2–4
H2O <=> H+ + ОН–
б) К(–): Cu2+ + 2e– = Cuo (восстановление) | 2
в) A(+): 4ОН– – 4e– = O2 + 2H2O (окисление) | 1
Суммарное уравнение электролиза:
г) 2Cu SO4 + 2H2O = 2Сu + O2 + 2H2SO4
Законы электролиза
Связь между количеством выделившегося при электролизе вещества количеством прошедшего через электролит электричества выражается законами Фарадея.
Первый закон Фарадея: массы веществ, выделившиеся на электродах при электролизе, прямо пропорциональны количеству электричества прошедшего через электролит, т. е.
е.
m = k · I · Δt,
где m – масса вещества, образовавшегося на электроде или у электрода, г.
k – электрохимический эквивалент вещества;
А – молярная масса вещества;
z – валентность;
F = 96487 Кл или F = 26,8 А/ч – постоянная Фарадея;
Δt – время проведения электролиза.
Второй закон Фарадея (закон эквивалентов для электрохимических реакций): одинаковые количества электричества выделяют на электродах при электролизе эквивалентные массы различных веществ:
,
где М – молярная масса данного вещества, образовавшегося после электролиза; I- сила тока, пропущенного через вещество или смесь веществ; Δt – время, в течении которого проводится электролиз; n –число участвующих в процессе электронов, которое при достаточно больших значениях силы тока равно абсолютной величине заряда иона, принявшего непосредственное участие в электролизе.
Отношение количества электричества (q), необходимого для выделения данной массы вещества, ко всему количеству прошедшего через электролит электричества (Q), называется выходом по току данного вещества и обычно выражается в процентах:
или
Далее предлагается рассчитать, сколько времени будет продолжаться электролиз при силе тока I = 1A, 2A, 4А.
Из 1-го закона Фарадея: m = KI = = 26 . 103 c = 7,2 час.
При I = 2A
Учитель предлагает рассчитать расход электрической энергии.
A = I U t (кВт/час)
Далее ученикам, объединенным в малые группы (4 чел), предлагается решить по выбору пять комбинированных задач:
а) Сколько времени длилось никелирование, если на изделие осел слой никеля массой 1,8 г. Сила тока 2А. Составьте химическое уравнение электролиза.
б) Последовательно с электролитической ванной, заполненной солью никеля, включена ванна, которой находится соль хрома. После размыкания цепи в первой ванне выделилось 10 г никеля. Сколько хрома выделилось во второй ванне. Напишите уравнение электролиза.
Сколько хрома выделилось во второй ванне. Напишите уравнение электролиза.
в) Аэростат объемом 250 см3 заполняют водородом при температуре 27 oС и давлении 2 атм. Какой заряд надо пропустить при электролизе через слабый раствор серной кислоты, чтобы получить нужное количество водорода? Напишите химическое уравнение электролиза.
г) Для серебрения ложек ток 1,8А пропускался через раствор соли серебра в течение 5 ч. Катодом служит 12 ложек, каждая из которых имеет площадь поверхности 50 см3. Какой толщины слой серебра отложится на ложках? Каков расход электрической энергии, если напряжение на электролитической ванне равно 0,5В?
д) При электролизе раствора серной кислоты расходуется мощность 37Вт. Определите сопротивление электролита, если за время 50 мин выделяется 0,3 г водорода. Напишите химическое уравнение электролиза.
е) При электролизе водного раствора гидроксида калия с инертными электродами на катоде выделился молекулярный водород, объем которого при нормальных условиях равен 11,2 л. Какой объем кислорода выделится при этом на аноде?
Какой объем кислорода выделится при этом на аноде?
ж) При электролизе водного раствора сульфата никеля (II) на катоде получили никель массой 177 г, выход которого составил 75%. Какой объем газа выделится при этом? Выход газа считать количественным.
ЭЛЕКТРОХИМИЧЕСКИЕ ЭКВИВАЛЕНТЫ, мг/К
Серебро 1,12
Хром 0,18
Алюминий 0,093
Никель 0,30
Кислород 0,085
Подведение итогов урока
Оценивание учащихся по решению расчетных задач.
законов электролиза Фарадея | Статья о законах электролиза Фарадея в The Free Dictionary
количественные законы электролиза, открытые М. Фарадеем в 1833–1834 гг. Законы Фарадея выражают взаимосвязь между количеством электричества, прошедшего через электролит, и массой и химической природой, в терминах химических эквивалентов, веществ, осажденных или растворенных на электродах.
Первый закон электролиза Фарадея гласит, что массы м осажденных или растворенных веществ пропорциональны количеству электричества q , прошедшего через электролит.Второй закон гласит, что массы различных веществ, отложившихся или растворенных в результате прохождения одного и того же количества электричества через электролит, пропорциональны химическим эквивалентам A этих веществ. Из второго закона следует, что одно и то же количество электричества, называемое постоянной Фарадея F , требуется для осаждения одного и того же грамм-эквивалента различных веществ. Математически законы Фарадея могут быть записаны в виде одного уравнения m = ( A / F ) q = kq , где коэффициент k = A / F называется электрохимическим эквивалентом.
Оба закона Фарадея точны, если ионы электролита переносят все электричество, прошедшее через электролит. В отдельных случаях наблюдаются отклонения от законов; такие отклонения могут быть связаны с неучтенными электрохимическими побочными реакциями — например, с выделением газообразного водорода при электроосаждении некоторых металлов — или с частичной электронной проводимостью, например, при электролизе некоторых сплавов.
СПРАВКА
Фарадей, М. Экспериментальные исследования по элеклричеслву , т. 1. [Москва] 1947. Страницы 176–226 и 265–346. (Пер. С англ.)Большая Советская Энциклопедия, 3-е издание (1970-1979). © 2010 The Gale Group, Inc. Все права защищены.
faraday & — definition — English
Примеры предложений с «faraday &», память переводов
springer Данные были получены в конфигурации Фарадея путем извлечения σ + и σ- спектров с магнитным полем в нескольких кристаллографических направлениях.WikiMatrixJensen, похоже, первым вышел из машины, но, когда Фарадей был на полпути, убийца, очевидно, выстрелил Фарадею в голову. Patents-wipo Перфорированная металлическая пленка для вращателя Фарадея в видимом спектре WikiMatrixFaraday также установил, что магнетизм может влиять на лучи света и что существует лежащая в основе взаимосвязь между двумя явлениями. WikiMatrixRegelation была обнаружена Майклом Фарадеем. WikiMatrix Таким образом, фарадеевские «трубки потока» становятся элементарными возбуждениями квантового электромагнитного поля.WikiMatrix Единицей индуктивности является генри, названный в честь Джозефа Генри, современника Фарадея. Openubtitles2 Добрый день, мистер Фарадей, патенты-wipo Проводящий слой (26) образует клетку Фарадея для электростатической защиты упакованного изделия, а антистатический слой (27) -27) предотвращает контакт проводящей пыли с упакованным изделием и неблагоприятное воздействие на него, а также защищает упакованное изделие от генерации статического электричества внутри контейнера. QEDМы называем это электростатическим экранированием, и мы даем ему имя, как ваш дом называться клеткой Фарадея.Патенты-wipoA method производит структуру на основе реконфигурируемой сборки с шаблонами на основе фарадеевских волн. WikiMatrixЭлектромагнитная индукция была независимо открыта Майклом Фарадеем и Джозефом Генри в 1831 году; однако Фарадей был первым, кто опубликовал результаты своих экспериментов. WikiMatrix В своей работе по статическому электричеству эксперимент Фарадея с ведром со льдом продемонстрировал, что заряд находится только на внешней стороне заряженного проводника, а внешний заряд не влияет на что-либо, заключенное внутри него. дирижер.WikiMatrix В 1832 году он завершил серию экспериментов, направленных на исследование фундаментальной природы электричества; Фарадей использовал «статическое электричество», батареи и «животное электричество» для создания явлений электростатического притяжения, электролиза, магнетизма и т. Д. Он пришел к выводу, что, вопреки научному мнению того времени, различия между различными «видами» электричества были иллюзорными. WikiMatrixМайкл Фарадей инициировал первую серию рождественских лекций в 1825 году. WikiMatrixHe также открыл взаимную индуктивность независимо от Майкла Фарадея, хотя Фарадей был первым, кто сделал открытие и опубликовал свои результаты.Волны WikiMatrixRadio, проходящие через ионосферу Земли, также подвержены эффекту Фарадея. Обычное ползание После этого Фарадей отправил Дэви образец своих записей, сделанных во время лекций. Ответ Дэви был незамедлительным, добрым и благоприятным. WikiMatrix Фарадей позже использовал открытые им принципы для создания электрического динамо, предка современных генераторов энергии и электродвигателя. WikiMatrix Он также встретил Майкла Фарадея и помог ему в работе с газами.OpenSubtitles2018 .v3 Ну, крыло Фарадея было разрушено, но мы думаем, что оно выровнялось перед взрывом.OpenSubtitles2018.v3 Ваш друг Фарадей сказал, что вы из будущего. Patents-wipo Сборка щита Фарадея включает в себя функции выравнивания, которые могут использоваться для обеспечения механической регистрации и / или электрического соединения сборки щита Фарадея. WikiMatrix Взаимоотношения между двумя мужчинами не могли быть описан как близкий, потому что Фарадей был на 40 лет старше Максвелла и проявлял признаки дряхлости. Академия Фарадей и Максвелл изучали электричество в то время, когда большинство людей, включая многих ученых, считали его чем-то бесперспективным и непрактичным.Показаны страницы 1. Найдено 234 предложения с фразой faraday &. Найдено за 5 мс.Накопители переводов создаются человеком, но выравниваются с помощью компьютера, что может вызвать ошибки. Найдено за 0 мс.Накопители переводов создаются человеком, но выравниваются с помощью компьютера, что может вызвать ошибки. Они поступают из многих источников и не проверяются. Имейте в виду.
Physics4Kids.com: Электричество и магнетизм: закон Фарадея
Закон индукции Фарадея — одно из важных понятий электричества. Он рассматривает то, как изменение магнитных полей может вызвать протекание тока в проводах.По сути, это формула / концепция, описывающая, как создается разность потенциалов ( разность напряжений ) и сколько создается. Очень важно понимать, что изменение магнитного поля может создавать напряжение. Майкл Фарадей был английским физиком, работавшим в начале 1800-х годов. Он работал с другим ученым по имени сэр Хамфри Дэви . Большое открытие Фарадея произошло в 1831 году, когда он обнаружил, что, когда вы меняете магнитное поле, вы можете создать электрический ток.Он проделал много другой работы с электричеством, такой как изготовление генераторов и эксперименты с электрохимией и электролизом.
Эксперименты Фарадея начались с магнитных полей, которые остались прежними. Эта установка не вызывала тока. Только когда он начал изменять магнитные поля, были индуцированы (созданы) ток и напряжение. Он обнаружил, что изменения магнитного поля и размера поля связаны с величиной создаваемого тока. Ученые также используют термин магнитный поток .Магнитный поток — это величина, которая представляет собой силу магнитного поля, умноженную на площадь поверхности устройства.
Вам придется пересмотреть свои греческие буквы, когда вы запомните настоящую формулу. Вот основы …E = дБ / dt
«E» — это значение индуцированного напряжения (старое название напряжения было «ElectroMotive Force» или EMF. Это «E» в уравнении). Изменение времени эксперимента — «dt». Время измеряется в секундах. Последний — «дБ», который означает изменение магнитного потока.Магнитный поток — это силовые линии магнитного поля. Поток равен BA, где B — напряженность магнитного поля, A — площадь. Эта формула немного сложнее, чем те, которые вы, возможно, видели раньше.
По-английски: величина создаваемого напряжения равна изменению магнитного потока, деленному на изменение во времени. Чем больше изменение магнитного поля, тем больше напряжение.
Радиоволны и электричество (видео NASA SciFiles)
Encyclopedia.com:
http://www.encyclopedia.com/topic/Faradays_law.aspx
Википедия (электромагнитная индукция):
http://en.wikipedia.org/wiki/Electromagnetic_induction
Encyclopædia Britannica (Закон индукции Фарадея):
http: // www.britannica.com/EBchecked/topic/201744/Faradays-law-of-induction
Physics4Kids Разделы
Сеть сайтов по науке и математике Рейдера
Фарадея и
Электромагнитная индукция (и эксперименты Фарадея) (хинди) | Физика | Khan Academy
Электромагнитная индукция (и эксперименты Фарадея) (хинди) | Физика | Хан Академия
Электромагнитная индукция (и эксперименты Фарадея) (хинди) | Физика | Хан Академия
Давайте узнаем, как производить электрический ток без батареек.Готовы изучить следующую тему? https://www.khanacademy.org/science/science-hindi/in-in-class-10-physics-india-hindi/mintage-effects-of-electric-current-hindi/electrome-induction-hindi/v/ правая-генератор-правило-хинди? модальный = 1 Класс 10 по физике в Академии Хана: давайте исследуем тайны света и электричества. От того, как отражается свет, до исправления дефектов наших глаз. От понимания обвинений до освещения городов. Все от призмы Ньютона до генератора Фарадея. Итак, пройдя этот курс, мы освоим темы (но не ограничиваясь) 10-го класса по физике NCERT.Об Академии Хана: Академия Хана — это некоммерческая организация, миссией которой является предоставление бесплатного образования мирового уровня для всех и в любом месте. Мы предлагаем викторины, вопросы, обучающие видео и статьи по целому ряду академических предметов, включая математику, биологию, химию, физику, историю, экономику, финансы, грамматику, дошкольное обучение и многое другое. Мы предоставляем учителям инструменты и данные, чтобы они могли помочь своим ученикам развить навыки, привычки и образ мышления для достижения успеха в школе и за ее пределами.Khan Academy была переведена на десятки языков, и 15 миллионов человек по всему миру обучаются в Khan Academy каждый месяц. Как некоммерческая организация 501 (c) (3), мы будем рады вашей помощи! Бесплатно. Для каждого. Навсегда. #YouCanLearnAnything Подпишитесь на KhanAcademyIndia: https://www.youtube.com/channel/UCU0kWLAbhVGxXarmE3b8rHg Сделайте пожертвование или станьте волонтером сегодня! Сделайте пожертвование здесь: https://www.khanacademy.org/donate?utm_source=youtube&utm_medium=desc Станьте волонтером здесь: https://www.khanacademy.org/contribute?utm_source=youtube&utm_medium=descЭлектролиз по закону Фарадея
Электролиз по закону Фарадея
Майкл Фарадей (1834) сформулировал два закона на основе своих исследований по электролизу:
1.Первый закон Фарадея
Согласно этому закону, «Количество вещества, выделяемого на электроде, прямо пропорционально количеству пропущенного электричества».
или,
Где W или M = количество высвободившегося вещества в граммах.
Q = количество переданной электроэнергии в кулонах.
Так как Q = I.t
Где I = ток в амперах
и t = время в секундах
Отсюда
, где Z = константа пропорциональности, называется электрохимический эквивалент .
Если I = 1 ампер и t = 1 секунда, то Z = W Следовательно, электрохимический эквивалент может быть определен как, «Масса вещества (в граммах), выделяющегося на электроде при пропускании тока 1 ампер в течение 1 секунды или при пропускании 1 кулон электричества называется электрохимическим эквивалентом вещества ».
1F = 9500 столбцов
Итак, 1 Фарадей [96500 кулонов] электричества произведет на катоде 1 грамм-эквивалента Ag, Cu и Al.
2. Второй закон Фарадея: Согласно этому закону, «если одно и то же количество электричества проходит через разные электролиты, то количество веществ, высвобождаемых на соответствующих электродах, находится в соотношении их эквивалентных масс».
