Cинтез 4-метоксифенилхлорацетата и 4-хлорфенилхлорацетата и его реакции с диэтилдитиокарбамат натрия и дифенилтиокарбазонами
АННОТАЦИЯ
Изучены синтез 4-метоксифенилхлорацетаты и 4-хлорфенилхлор-ацетаты и реакции с диэтилдитиокарбамата натрия и дифенилтиокарбазоном в присутствии диметилформамида. Строение полученных веществ установлено методами ИК- и УФ-спектроскопии.
ABSTRACT
Astudyofthe synthesis 4-methoxyphenylchloroacetate and 4-chlorophenylchloroacetat and it‘softhe reactions odiumsalt of diethylditiokarbamate and diphenyltiokarbazone in presence of dimethylformamide. The structure of the obtained materials are installed by means of IR- and UF-spectroscopy.
Химический дизайн биологически активных веществ, в том числе фенолов, осуществляется путем комбинации в молекуле нескольких фармакофорных фрагментов, что довольно часто приводит не только к усилению основного терапевтического эффекта, но и к возникновению новых, порой неожиданных видов активности [1, с.
В статье рассмотрены некоторые методы введения в структуру физиологически активного 4-метоксифенола заместителя, содержащего гидразиногруппу и атомы галогенов, поскольку многие гидразиносоединения обладают высокой антибактериальной, инсектицидной, ростстимулирующей и другими видами биологической активности [3, с. 185]. Введение галогенов повышает липофильность лекарственных веществ и облегчает их прохождение через биомембраны. Одновременное присутствие галоген- и гидразиногруппы в ароматическом ядре, как, например, в производных фенилсалициланилидов, обладают высокой антигельминтной активностью и проявляют мощный разобщающий эффект [4, с. 179].
В связи с этим мы составили следующую схему превращений. Синтезированные по известным методикам хлорацетилхлорид, 4-метоксифенол и 4-хлорфенол, выгодно отличающейся от приведенной схемы получения в методике, ацилировали хлорангидридом хлоруксусной кислоты по схеме 1.
Ацилирование проходит в довольно мягких условиях — при кипячении в течение 12-15 ч в хлороформе.
Проведены реакции натриевой соли диэтилдитиокарбаминовой кислоты и дифенилтиокарбазонами с 4-метоксифенилхлорацетатом в диметилформамиде (ДМФА). Опыты проводились путём кипячения реакционной смеси с различной продолжительностью. Самый высокий выход продукта реакции составил 40%. В этих условиях в реакциях дифенилтиокарбазона выход продукта составил соответственно 57%.
Таблица
Зависимость выхода продукта реакции 4-метоксифенилхлорацетаты с иэтилдитиокарбамата натрия и дифенилтиокарбазонами в растворе ДМФА от продолжительности (мольные соотношения реагентов соответственно —3:1:5)
|
Продолжительность реакции, час |
Выход 4-метоксифенил-карбоксиметил-диэтилдитиокарбамата% |
Выход 4-метоксифенил-карбоксиметил-дифенилтиокарбазона % |
| 1 |
33 |
37 |
|
2 |
37 |
41 |
|
3 |
43 |
47 |
|
4 |
45 |
55 |
|
5 |
40 |
57 |
Из данных таблицы видно, что в опытах с участием диэтилдитиокарбамата натрия выходы продуктов заметно выше по сравнению с реакциями дифенилтиокарбазона.
Проведены реакции натриевой соли диэтилдитиокарбаминовой кислоты и дифенилтиокарбазонами с 4-хлорфенилхлорацетатом в диметилформамиде (ДМФА). Результаты опытов приведены в таблице 2.
Таблица 2
Влияние продолжительности реакции 4-хлорфенилхлорацетаты с диэтилдитиокарбамата натрия и дифенилтиокарбазонами в растворе ДМФА на выход продуктов (мольные соотношения реагентов соответственно —3
:1:5)|
Продолжительность реакции, час |
Выход 4-хлорфенил-карбоксиметил-диэтилдитиокарбамата% |
Выход 4-хлорфенил-карбоксиметил-дифенилтиокарбазона % |
|
1 |
40 |
43 |
|
2 |
45 |
47 |
|
3 |
53 |
|
|
4 |
60 |
60 |
|
5 |
60 |
62 |
Как известно, биполярные апротонные растворители (ДМСО, ДМФА, ТГФ, ацетон, диоксан) облегчают реакцию бимолекулярного нуклеофильного замещения в алкилгалогенидах за счёт сольватации катиона солей карбоновых кислот этими растворителями.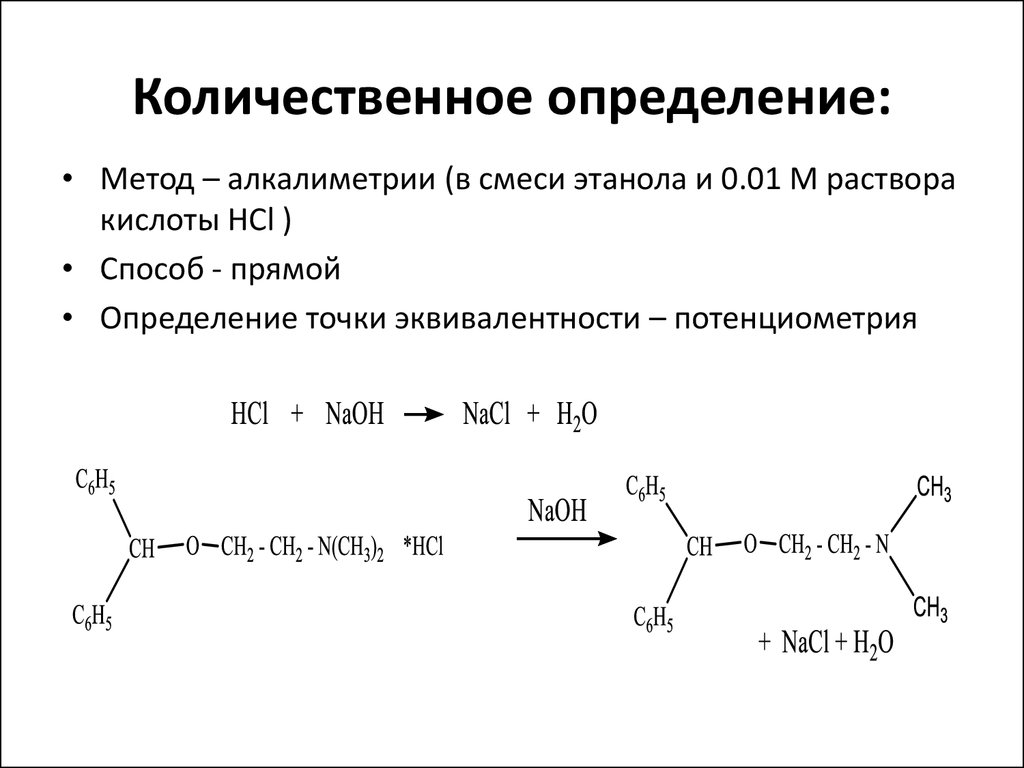
В связи с этим уравнение и механизм реакции 4-хлорфенилхлорацетата и 4-метоксифенилхлорацетата с диэтилдитиокарбамат натрия и дифенилтиокарбазонами в присутствии диметилформамида можно представить следующим образом:
Сольватация катиона натрия дает возможность проникновения (С2Н5)2NCSS— иона в органический слой и облегчает реакцию.
Синтез 4-метоксифенилхлорацетата. К раствору 12,4 г (0,1 моль) 4-метоксифенола в 10 мл хлороформа при перемешивании на магнитной мешалке прибавляли по каплям при комнатной температуре 11,3 г (0,1 моль) хлорангидрида хлоруксусной кислоты. После прибавления смесь нагревали при постоянном перемешивании и температуре 55-60°С в течение 16 ч и оставляли на ночь. Затем раствор выливали в стакан со смесью 50 г воды и 50 г льда, выпавший белый осадок отфильтровывали, промывали водой, сушили при 50°С, получили 18,8 г (94 ℅) с т. пл. 56°С (пропанол-2). В ИК-спектр (KBr, ν, см-1): 2901, 2880 (С-Н), 1740 (C=O), 1362, 1240 (С-О-С) 1506, 1540 (Ar), 1170, 1155, 976, 833 (C-CI).
Синтез 4-хлорфенилхлорацетата. Выход 19,8 г (97℅) с т. пл. 48°С (пропанол-2). В ИК-спектр (KBr, ν, см-1): 2960, 2875 (С-Н), 1743 (C=O), 1370, 1320, 1260 (С-О-С) 1498, 1408 (Ar), 1190, 1155, 1006, 980, 830 (C-CI). УФ-спектр (EtOH, λmax, нм) (lgε): 250 (5.7), 340 (5.6).
Синтез 4-хлорфенилкарбоксиметилдиэтилдитиокарбамата. К суспензии 6,15 г (0,03 моль) 4-хлорфенилхлорацетата в 10 мл абсолютного диметилформамида добавили 1,71 г (0,01 моль) диэтилдитиокарбамат натрия. Нагревали при перемешивании с обратным холодильником 3 ч, отфильтровывали горячим от осадка хлорида натрия, промывали несколько раз горячим этилацетатом. Из объединенных маточных растворов отгоняли растворитель, получили 2,25 г (71℅) бесцветной маслянистой жидкости с т. кип. 340о С. ВИК-спектр (KBr, ν, см -1): 3100-3000 (CHAr), 3000-2800 (CHAlk), 1760 (C=O), 1600-1360 (Ar), 1300-1000 (C-O), 880-620 (CHAr). УФ-спектр (EtOH, λmax, нм) (lg ε): 254 (5.5), 353 (5.5).
УФ-спектр (EtOH, λmax, нм) (lg ε): 254 (5.5), 353 (5.5).
Синтез 4-хлорфенилдифенилтиокарбазона. Ксуспензии 6,15 г (0,03 моль) 4-хлорфенилхлорацетата в 10 мл абсолютного диметилсульфоксида добавили 0,69 г (0,005 моль) поташа и 2,56 г (0,01 моль) дифенилтиокарбазона. Нагревали при перемешивании с обратным холодильником 3 ч, отфильтровывали горячим от осадка хлорида калия, промывали несколько раз горячим этилацетатом. Из объединенных маточных растворов отгоняли растворитель, получили 2,41 г (62℅) светло-желтой маслянистой жидкости с т. кип. 318о С. ВИК-спектр (KBr, ν, см-1): 3200 (N-H), 1750 (C=O), 1675-1665 (N=N), 1498, 1408 (Ar), 1300-1000 (C-O), 880-620 (CHAr). УФ-спектр (EtOH, λ
Синтез 4-метоксифенилдифенилтиокарбазона. К суспензии 6 г (0,03 моль) 4-метоксифенилхлорацетата в 10 мл абсолютного диметилсульфоксида добавили 0,69 г (0,005 моль) поташа и 2,56 г (0,01 моль) дифенилтиокарбазона. Нагревали при перемешивании с обратным холодильником 3 ч, отфильтровывали горячим от осадка хлорида калия, промывали несколько раз горячим этилацетатом. Из объединенных маточных растворов отгоняли растворитель, получили 2,47 г (59 ℅) светло-желтой маслянистой жидкости с т. кип. 305о С. ВИК-спектр (KBr, ν, см-1): 3200 (N-H), 1770 (C=O), 1650-1635 (N=N), 1500, 1399 (Ar), 1290-1021 (C-O), 883-617 (CHAr). УФ-спектр (EtOH, λmax, нм) (lgε): 252 (5.5), 353 (5.4).
Нагревали при перемешивании с обратным холодильником 3 ч, отфильтровывали горячим от осадка хлорида калия, промывали несколько раз горячим этилацетатом. Из объединенных маточных растворов отгоняли растворитель, получили 2,47 г (59 ℅) светло-желтой маслянистой жидкости с т. кип. 305о С. ВИК-спектр (KBr, ν, см-1): 3200 (N-H), 1770 (C=O), 1650-1635 (N=N), 1500, 1399 (Ar), 1290-1021 (C-O), 883-617 (CHAr). УФ-спектр (EtOH, λmax, нм) (lgε): 252 (5.5), 353 (5.4).
Состав и строение полученных соединений подтверждают данные элементного анализа, ИК- и УФ-спектроскопии. ТСХ-анализ выполнили на пластинках Sorbfil, проявление — парами йода.
Список литературы:
1. Беликов В. Г. Фармацевтическая химия. — М.: Высшая школа, 1985. — 552 с.
2. Ингольд К. К. Механизм реакций и строение органических соединений. — М.: Мир, 1959. — 340 с.
3. Солдатенков А. Т., Колядина Н. М., Шендрик И. В. Основы органической химии лекарственных веществ // Химия. — Москва, 2001. — 192 с.
— Москва, 2001. — 192 с.
4. Титце Л., Айхер Т. Препаративная органическая химия. — М.: Мир, 1999. — С. 179.
5. Холиков Т. С., Бобоназарова С. Х., Таджимухамедов Х. С. Получение бензилбензоата из бензоата натрия и хлористого бензила в присутствии малых количеств диметилформамида// ДАН РУз. — Ташкент, 2005. — № 1. — С. 34-36.
Рациональность и допустимость использования в качестве реагента потенциометрического типа диэтилдитиокарбамата натрия Группа компаний ИНФРА-М — Эдиторум
В современном понимании дитиокарбаматы представляют собой разнообразные соединения, молекулы которых включают в себя обязательное наличие карбодитиовой – CS-SH группы (серные атомы замещают кислородные атомы) и азотной аминогруппы, связанные с ней за счет атома. Дитиокарбамат (аммонийная соль этилдитиокарбамидовой кислоты) открыл немецкий учёный В. Цейс в XIX в. А в начале XX в., в трудах М. Делепина зафиксировано его применение для количественного определения, а также разделения катионов, которые имеют металлы в области аналитической химии. Эксперименты, проводимые позднее, а также новейшие и актуальные исследования позволяют наблюдать расширение экспериментальной базы, которая открывает новые сферы и рамки практического применения. На данный момент отмечается сосредоточенность использования дитиокарбаматов в секторе металлургии и медицины, аналитической химии, химической технологии и сельскохозяйственной сфере [3, с. 47–49]. В этом классе веществ наиболее распространенным, часто используемым и доступным выступает диэтилдитиокарбамат натрия (ДЭДТКNa).
Эксперименты, проводимые позднее, а также новейшие и актуальные исследования позволяют наблюдать расширение экспериментальной базы, которая открывает новые сферы и рамки практического применения. На данный момент отмечается сосредоточенность использования дитиокарбаматов в секторе металлургии и медицины, аналитической химии, химической технологии и сельскохозяйственной сфере [3, с. 47–49]. В этом классе веществ наиболее распространенным, часто используемым и доступным выступает диэтилдитиокарбамат натрия (ДЭДТКNa).
Строение заместителей при аминогруппе помимо наличия карбодитиовой группы определяют ряд химических свойств дитиокарбаматов [1, с. 9–11]. В основном взаимодействие аммиака с сероуглеродом или первичных или вторичных аминов позволяют диэтилдитиокарбаматам синтезироваться [4, с. 594].
Формула диэтилдитиокарбамата выглядит следующим образом: (C2H5)2NCS-SNa, в то время как вещество, по сути, является солью диэтилзамещенной дитиокарбамовой кислоты. Говоря об аналитической области применения ДЭДТКNa, как одного из наиболее популярных представителей этой группы, можно отметить, что причиной этому является его набор химических и физических качеств.
Говоря об аналитической области применения ДЭДТКNa, как одного из наиболее популярных представителей этой группы, можно отметить, что причиной этому является его набор химических и физических качеств.
Признание препаратов ДЭДТКNa кристаллогидратами позволяет рассматриваемому веществу быть отнесенным к ряду хорошо растворимых в воде (35,06 г/100 мл), но снижение данной способности наблюдается в основном в растворителях органического вида, включая неполярные инертные [8, с. 52]. При аналитике важно обращать внимание на неустойчивость дитиокарбаматов. Препараты ДЭДТКNa, при хранении в сухом виде, разлагаются медленно из-за влияния кислорода. Также этому процессу способствует кристаллизационная вода. Кислородное, кислотное, световое или тепловое воздействие способствуют растворам дитиокарбаматов разлагаться быстрее. Введение пирофосфата, аммиака или стабилизаторов основной природы, таких как Na2CO3 позволяет существенно увеличить срок устойчивости и хранения разбавленных растворов ДЭДТКNa от трех дней до нескольких недель. При этом темная посуда, не позволяющая пропускать лучи солнечного света, является наиболее подходящей ёмкостью для хранения рабочих растворов. При нагревании растворов ДЭДТКNa можно наблюдать их разложение до производных элементов сероводорода или тиомочевины.
При этом темная посуда, не позволяющая пропускать лучи солнечного света, является наиболее подходящей ёмкостью для хранения рабочих растворов. При нагревании растворов ДЭДТКNa можно наблюдать их разложение до производных элементов сероводорода или тиомочевины.
Стабильность рабочих растворов дитиокарбаматов регулярно подвержена воздействию степени кислотности сферы, что является важной особенностью для аналитической практики [2, с. 48]. В холодной среде минеральные кислоты, вступая в реакцию взаимодействия с щелочными солями дитиокарбаматов, образуют в воде малорастворимые осадки. Разложение до амина и сероуглерода происходит вследствие слабовыраженной устойчивости кислых и слабокислых растворов дитиокарбаматов, что неизбежно приводит к отсутствию воспроизводимости результатов. Наибольшая часть исследователей произвела ряд выдающихся открытий относительно кинетики распада различного рода дитиокарбаматов [7, с. 34]. При этом концентрация дитиокарбамата наравне с концентрацией ионов водорода определяют скорость распада. Можно считать реакцию распада дитиокарбаматов совместно с буферными растворами мономолекулярной и отнести к псевдопервому порядку. Более устойчивыми в щелочных растворах являются диалкилдитиокарбаматы, к которым относятся ДЭДТКNa. Здесь отмечена природа металла, входящего в состав дитиокарбаматного соединения, который уменьшается в ряде Na-Zn-Fe-Cu, определяющий скорость распада. При разложении ДЭДТКNa, за счет C-N проистекает разрыв, образуя тем самым диэтиламин и сероуглерод:
Можно считать реакцию распада дитиокарбаматов совместно с буферными растворами мономолекулярной и отнести к псевдопервому порядку. Более устойчивыми в щелочных растворах являются диалкилдитиокарбаматы, к которым относятся ДЭДТКNa. Здесь отмечена природа металла, входящего в состав дитиокарбаматного соединения, который уменьшается в ряде Na-Zn-Fe-Cu, определяющий скорость распада. При разложении ДЭДТКNa, за счет C-N проистекает разрыв, образуя тем самым диэтиламин и сероуглерод:
- Мгновенное протонирование аниона соли: (C2H5)2 NCS–S—+H+⇆(C2H5)2NS-SH. Прослеживается образование ионов биполярного типа и нейтральных кислотных молекул. Отмечается взаимосвязь, обеспечивающаяся за счет pH раствора, а также равноценности элементов.
- Замедленное молекулярное разложение диэтилдитиокарбамавой кислоты: (C2H5)2 CS–SH+H++⇆[(C2H5)2NH2]+CS2.
 В анализируемой реакции мы наблюдаем внутримолекулярную связь, которая зарождается благодаря связи атома азота и тиольного серного атома. Именно с первого атома происходит последующее смещение к мостиковому протону электронной плотности. Близкое расположение частиц с положительным зарядом способствует разрыву C-N связи, что обуславливается электронным эффектом на карботиольном углеродном атоме и в определенной мере является на атоме азота основной причиной отрыва от положительного заряда.
В анализируемой реакции мы наблюдаем внутримолекулярную связь, которая зарождается благодаря связи атома азота и тиольного серного атома. Именно с первого атома происходит последующее смещение к мостиковому протону электронной плотности. Близкое расположение частиц с положительным зарядом способствует разрыву C-N связи, что обуславливается электронным эффектом на карботиольном углеродном атоме и в определенной мере является на атоме азота основной причиной отрыва от положительного заряда.
Необходимо отметить, что диэлектрическая проницаемость раствора оказывает значительное влияние на скорость распада. Протонированные молекулы ДЭДТК обладают меньшей устойчивостью при ее уменьшении в растворах водно-метанольного типа. Помимо написанного выше, можно проследить, что уменьшению скорости разложения в некоторой мере способствует введение ионов, отличающихся увеличенной поляризующей способностью, например K+ и прогрессирование ионной силы раствора.
Наличие упомянутой далее схемы является сопровождающим элементом процесса окисления до тетраэтилтиурамдисульфида воздуха кислородом, что представляется одним из немаловажных аспектов при снижении концентрации ДЭДТКNa.
Такие признаки тиурамдисульфидов как устойчивость к воздействию кислот и водная малорастворимость не дает им перейти обратно в состояние диэтилдитиокарбамата.
Однако прослеживается образование прочных π – связи ковалентного и донорно-акцепторного типа, которое обеспечивается присутствием электродонорных серных тионных и тиольных атомов. Здесь можно говорить и об образовании таких внутрикомплексных соединений, которые имеют четырехчленные циклы. В основном схожесть с серой наблюдается у тех ионов, которые образуют соединения с ДЭДТКNa. Однако некоторые катионные соединения все же образуют малорастворимые сульфиды (тантал, цирконий, нептуний, торий, лантан, титан). Существуют ограничения в использовании вышеперечисленных металлов, что обуславливается специальными условиями по их образованию и созданию.
Присутствие в ДЭДТКNе гидрофобных фрагментов этилового происхождения говорит о низкой растворимости его компонентов, однако это допускает их использование с целью осуществления осаждения или экстракции различных катионов тяжелых металлов.
На сегодняшний день есть самый востребованный способ по определению допустимых значений pH, за счет формирования крепких внутрикомплексных соединений элементов с ДЭДТКNa, а также скорости процесса. Процесс заключается в наблюдении и определении за разложением диэтилдитиокарбамата, из-за чего видно её снижение к отношению, в водных растворах, скорости возникновения хелатов. Важно отметить, что скорость распада реагента влияет на выбор pH раствора ДЭДТКNa.
Те элементы, которые возникают в результате вычисления из растворимости веществ принято называть произведениями растворимости (далее – ПР), а также брать во внимание при оценивании растворимости возможных образующихся осадков. Достоверность результатов при этом может быть получена вследствие применения описанной величины для неорганических соединений, потому что эти элементы диссоциативны в воде. ПР в органических солях приводит к ошибкам и неточностям. Это происходит из-за недиссоциированных форм металлов, присутствующих в растворе: Hg (II), Au (I), Pb (II). В таких случаях используются ионные произведения (далее – ИП), определяющиеся потенциометрическим способом [9, c. 84].
В таких случаях используются ионные произведения (далее – ИП), определяющиеся потенциометрическим способом [9, c. 84].
Диэтилдитиокарбамат применяется для обнаружения, в концентрировании, при количественном анализе, для разделения и при маскировке.
Самым распространенным является потенциометрический титриметрический метод. Благодаря ему можно качественно и быстро анализировать 2-х и многокомпонентные конгломераты без разделения и маскирования. Также рассчитывать мутные или окрашенные растворы, свойственные при осаждении диэтилдитиокарбаматов.
Применение ДЭДТКNa в качестве титранта Pb(II), Cu(II), Zn(II), Ag(I), Cd(II), Tl(I), In(III), Ni(II), Hg2+, Hg22+, Bi(III), Se(IV), Te(IV) для последующего определения описано многими научными источниками. Отмечается, что неточность определений колеблется в районе 1–3% для катионов индивидуального типа [10, с. 110]. Однако, образующих прочные нерастворимые соединения с ДЭДТКNa ионов гораздо больше. Их определение можно выявить благодаря проведению расчётов, например, благодаря проведению опытов, которые требуют наибольших затрат, качественного и достаточного материала и определенного количества времени или прогнозированию в таких методах анализа как титриметрические. По завершению описываемой стадии возможно дальнейшее внесение корректировок и апробация. Результаты, полученные в табл. 1, представляют собой использование констант устойчивости образующих соединений и такого критерия прогнозирования как «степень протекания реакции в точке эквивалентности» (далее – СП).
Их определение можно выявить благодаря проведению расчётов, например, благодаря проведению опытов, которые требуют наибольших затрат, качественного и достаточного материала и определенного количества времени или прогнозированию в таких методах анализа как титриметрические. По завершению описываемой стадии возможно дальнейшее внесение корректировок и апробация. Результаты, полученные в табл. 1, представляют собой использование констант устойчивости образующих соединений и такого критерия прогнозирования как «степень протекания реакции в точке эквивалентности» (далее – СП).
Таблица 1
Различные степени протекания реакций осаждения катионов ДЭДТКNa, c ДЭДТКNa = 0,1000 моль/л, cM = 0,1000 моль/л
|
Ион |
СП, 100% |
pK |
Ион |
СП, 100% |
pK |
|
Sb3+ |
100,0* |
35,6 |
Zn2+ |
16,2 |
99,99 |
|
Au+ |
100,0 |
29,8 |
Ga3+ |
24,3 |
100,0 |
|
Hg2+ |
100,0 |
40,8 |
Sn2+ |
17,3 |
99,99 |
|
Bi3+ |
100,0 |
37,2 |
Tl+ |
9,2 |
99,95 |
|
Ag+ |
100,0 |
19,8 |
In3+ |
26,7 |
100,0 |
|
Se4+ |
100,0 |
54,6 |
Ni2+ |
19 |
100,0 |
|
Tl3+ |
100,0 |
44,5 |
Co2+ |
19,3 |
100,0 |
|
MoO22+ |
100,0 |
27,9 |
Cd2+ |
19,6 |
100,0 |
|
Cu2+ |
100,0 |
27,9 |
Pb2+ |
21,8 |
100,0 |
|
Pd2+ |
100,0 |
38,4 |
Te4+ |
43 |
100,0 |
(*100,0 > 99,99)
Самой потенциальной возможностью анализа считается последовательное титрование или маскирование из соединений ионов, не изменяя pH раствор. Также существуют иные способы по определению катионов Ag(I), Zn(II), Pb(II), Cu(II) [6, с. 62].
Также существуют иные способы по определению катионов Ag(I), Zn(II), Pb(II), Cu(II) [6, с. 62].
Таким образом, за счет протекания реакции на момент ее начала касаемо второго определяемого компонента (далее – СП’), константы устойчивости соединений, в качестве итога можно получить выявленные анализируемые с двумя скачками ионные пары [5, с. 1158]. Значения СП’ для разных пар определяемых катионов представлены в табл. 2.
То, что анализ не может быть продолжен, подтверждают отмеченные жирным шрифтом в табл. значения, которые свидетельствуют о том, что при предельном значении 99,20% показателе СП’ – ниже его. Это означает, что полученные нами показатели позволяют в утвердительном ключе говорить о наличии теоретической возможности анализа 168 различных ионных парных позиций металлов благодаря процедуре последовательного титрования. Но даже это не является ограничителем всех возможностей диэтилдитиокарбамата, так как он подвергает анализу смеси, состоящие из 3-х и более составляющих.
Далее мы провели титрование смеси, включающей Cu(II)–Pb(II)–Tl(I). Определяя индивидуальные ионы, ошибки варьировались от 3-х до 5%. Полученные результаты представлены в табл. 3. За счет компьютерной программы «GhoseSeq», нами были получены данные, свидетельствующие о том, что теоретически могут определяться до 18 143 смесей, которые имеют нужное число скачков, содержащих до 9 компонентов. Но наличие соосаждений и адсорбции, также других, приводящих к росту погрешностей, при проведении анализа возможных составляющих зафиксировано не было.
Таблица 3
Процесс титрования трехкомпонентной смеси Cu(NO3)2 – Pb(NO3)2 – TlNO30,8748 ммоль /л раствором ДЭДТКNa
|
Ион |
Введено, мг |
Величина скачка потенциала ∆E, мВ |
Относительная ошибка,% |
Найдено, мг |
|
Tl+ |
0,0870 |
15 |
5,7 |
0,0920 |
|
Cu2+ |
0,1166 |
120 |
5,0 |
0,1224 |
|
Pb2+ |
0,03831 |
110 |
3,3 |
0,03958 |
Таким образом, макроколичества и полумикроколичества металлов в некоторых растворах в роли потенциометрического реагента являются важными возможностями ДЭДТКNa, учитывая способность образования прочного комплекса с разносторонними катионами. При отсутствии разделения в количественном определении сразу нескольких катионов могут сократиться временные затраты на выявление неточности определений. Это затрудняет хранение полученных растворов, а также за счет неустойчивости реагента осуществляется индикационный процесс по соотношению равнозначных форм «диэтилдитиокарбамат-тетраэтилтиурамдисульфид».
При отсутствии разделения в количественном определении сразу нескольких катионов могут сократиться временные затраты на выявление неточности определений. Это затрудняет хранение полученных растворов, а также за счет неустойчивости реагента осуществляется индикационный процесс по соотношению равнозначных форм «диэтилдитиокарбамат-тетраэтилтиурамдисульфид».
НАТРИЯ ДИЭТИЛДИТИОКАРБАМАТ | CAMEO Chemicals
Добавить в MyChemicals Страница для печати
Химический паспорт
Химические идентификаторы | Опасности | Рекомендации по ответу | Физические свойства | Нормативная информация | Альтернативные химические названия
Химические идентификаторы
Что это за информация?
Поля химического идентификатора
включают общие идентификационные номера,
алмаз NFPA
Знаки опасности Министерства транспорта США и общий
описание хим. Информация в CAMEO Chemicals поступает
из множества
источники данных.
| Номер CAS | Номер ООН/НА | Знак опасности DOT | Береговая охрана США КРИС Код |
|---|---|---|---|
| никто | данные недоступны | никто |
| Карманный справочник NIOSH | Международная карта химической безопасности | ||
| никто |
| ||
NFPA 704
данные недоступны
Общее описание
ФИЗИЧЕСКОЕ ОПИСАНИЕ: Белые, слегка коричневые или слегка розовые кристаллы без запаха. (NTP, 1992)
(NTP, 1992)
Опасности
Что это за информация?
Опасные поля включать специальные предупреждения об опасности воздух и вода реакции, пожароопасность, опасность для здоровья, профиль реактивности и подробности о задания реактивных групп и потенциально несовместимые абсорбенты. Информация в CAMEO Chemicals поступает из различных источников. источники данных.
Предупреждения о реактивности
нет
Реакции с воздухом и водой
Растворим в воде. Тио- и дитиокарбаматы медленно разлагаются в водном растворе с образованием сероуглерода и метиламина или других аминов. Такие разложения ускоряются кислотами.
Опасность возгорания
Данные о температуре вспышки для этого химического вещества отсутствуют; однако он, вероятно, горюч. (НТП, 1992)
Опасность для здоровья
СИМПТОМЫ: Симптомы воздействия этого химического вещества включают раздражение глаз. Продолжительное воздействие может вызвать легкое раздражение кожи. Пыли этого соединения едкие для слизистых оболочек. Это соединение также едко для пищеварительного тракта.
Продолжительное воздействие может вызвать легкое раздражение кожи. Пыли этого соединения едкие для слизистых оболочек. Это соединение также едко для пищеварительного тракта.
ОСТРЫЕ/ХРОНИЧЕСКИЕ ОПАСНОСТИ: Это химическое вещество может нанести вред при проглатывании или вдыхании. При нагревании до разложения выделяет очень токсичные пары оксидов азота, оксидов серы и оксида натрия. (НТП, 1992 г.)
Профиль реакционной способности
ДИЭТИЛДИТИОКАРБАМАТ НАТРИЯ не совместим с сильными окислителями. Водные растворы медленно разлагаются с образованием сероуглерода и амина. Такие разложения ускоряются кислотами. Добавление кислоты к водному раствору дает белую мутность (NTP, 1992).
Принадлежит к следующей реакционноспособной группе (группам):
- Сложные эфиры и соли тиокарбамата/ Сложные эфиры и соли дитиокарбамата
Потенциально несовместимые абсорбенты
Соблюдайте осторожность.
Известно, что он реагирует с
абсорбенты
перечислено ниже. Больше информации о абсорбентах, в том числе о ситуациях, на которые следует обратить внимание…
Больше информации о абсорбентах, в том числе о ситуациях, на которые следует обратить внимание…
- Абсорбенты на основе целлюлозы
- Абсорбенты на минеральной и глиняной основе
- Грязь/Земля
Рекомендации по ответу
Что это за информация?
Поля рекомендации ответа включают в себя расстояния изоляции и эвакуации, а также рекомендации по пожаротушение, пожарное реагирование, защитная одежда и первая помощь. информация в CAMEO Chemicals поступает из различных источники данных.
Изоляция и эвакуация
Информация отсутствует.
Пожарное дело
Пожары, связанные с этим материалом, можно тушить с помощью сухого химиката, двуокиси углерода или галонового огнетушителя. Также можно использовать распылитель воды. (НТП, 1992)
Непожарное реагирование
НЕБОЛЬШИЕ РАЗЛИВЫ И УТЕЧКИ: Если вы пролили это химическое вещество, вам следует смочить твердый разлитый материал водой, а затем переместить смоченный материал в подходящий контейнер.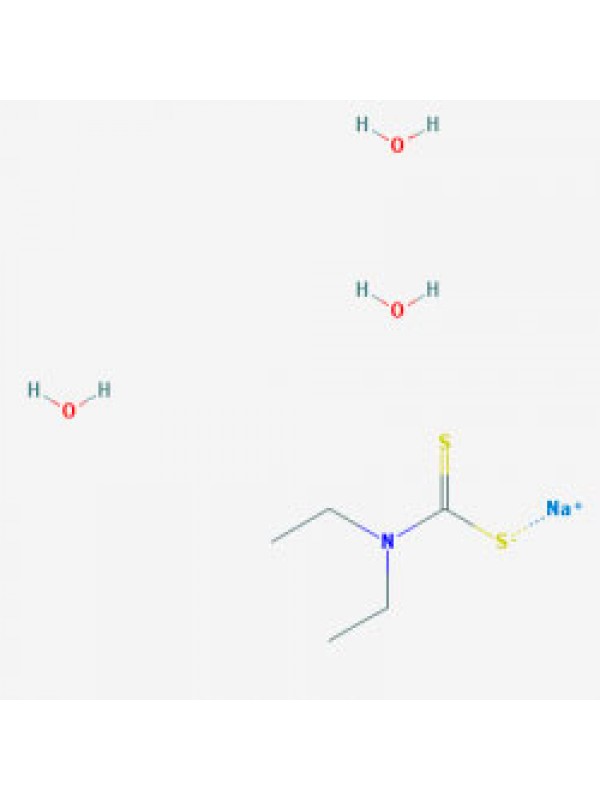 Используйте впитывающую бумагу, смоченную водой, чтобы собрать оставшийся материал. Запечатайте загрязненную одежду и впитывающую бумагу в паронепроницаемый пластиковый пакет для возможной утилизации. Вымойте все загрязненные поверхности мыльным раствором. Не возвращайтесь в загрязненную зону до тех пор, пока сотрудник службы безопасности (или другое ответственное лицо) не убедится, что зона была должным образом очищена.
Используйте впитывающую бумагу, смоченную водой, чтобы собрать оставшийся материал. Запечатайте загрязненную одежду и впитывающую бумагу в паронепроницаемый пластиковый пакет для возможной утилизации. Вымойте все загрязненные поверхности мыльным раствором. Не возвращайтесь в загрязненную зону до тех пор, пока сотрудник службы безопасности (или другое ответственное лицо) не убедится, что зона была должным образом очищена.
МЕРЫ ПРЕДОСТОРОЖНОСТИ ПРИ ХРАНЕНИИ: Этот материал следует хранить при температуре окружающей среды вдали от окисляющих материалов. (НТП, 1992 г.)
Защитная одежда
РЕКОМЕНДУЕМЫЙ РЕСПИРАТОР: При взвешивании и разбавлении неразбавленного испытуемого химического вещества наденьте полумаску, одобренную NIOSH, оснащенную картриджем с органическим паром/кислым газом (специально для органических паров, HCl, кислого газа и SO2) с пыле/туманный фильтр. (NTP, 1992)
Ткани для костюмов DuPont Tychem®
Нет доступной информации.
Первая помощь
ГЛАЗА: Сначала проверьте наличие у пострадавшего контактных линз и снимите их, если они есть. Промывать глаза пострадавшего водой или физиологическим раствором в течение 20–30 минут, одновременно звоня в больницу или токсикологический центр. Не закапывайте в глаза пострадавшему какие-либо мази, масла или лекарства без специальных указаний врача. НЕМЕДЛЕННО доставьте пострадавшего после промывания глаз в больницу, даже если симптомы (например, покраснение или раздражение) не развиваются.
Промывать глаза пострадавшего водой или физиологическим раствором в течение 20–30 минут, одновременно звоня в больницу или токсикологический центр. Не закапывайте в глаза пострадавшему какие-либо мази, масла или лекарства без специальных указаний врача. НЕМЕДЛЕННО доставьте пострадавшего после промывания глаз в больницу, даже если симптомы (например, покраснение или раздражение) не развиваются.
КОЖА: НЕМЕДЛЕННО промойте пораженные участки кожи водой, сняв и изолировав всю загрязненную одежду. Тщательно промойте все пораженные участки кожи водой с мылом. При появлении таких симптомов, как покраснение или раздражение, НЕМЕДЛЕННО вызовите врача и будьте готовы доставить пострадавшего в больницу для лечения.
ПРИ ВДЫХАНИИ: НЕМЕДЛЕННО покинуть зараженную зону; сделать глубокий вдох свежего воздуха. При появлении симптомов (таких как свистящее дыхание, кашель, одышка или жжение во рту, горле или груди) вызовите врача и будьте готовы доставить пострадавшего в больницу. Обеспечьте надлежащую защиту органов дыхания спасателям, входящим в неизвестную атмосферу.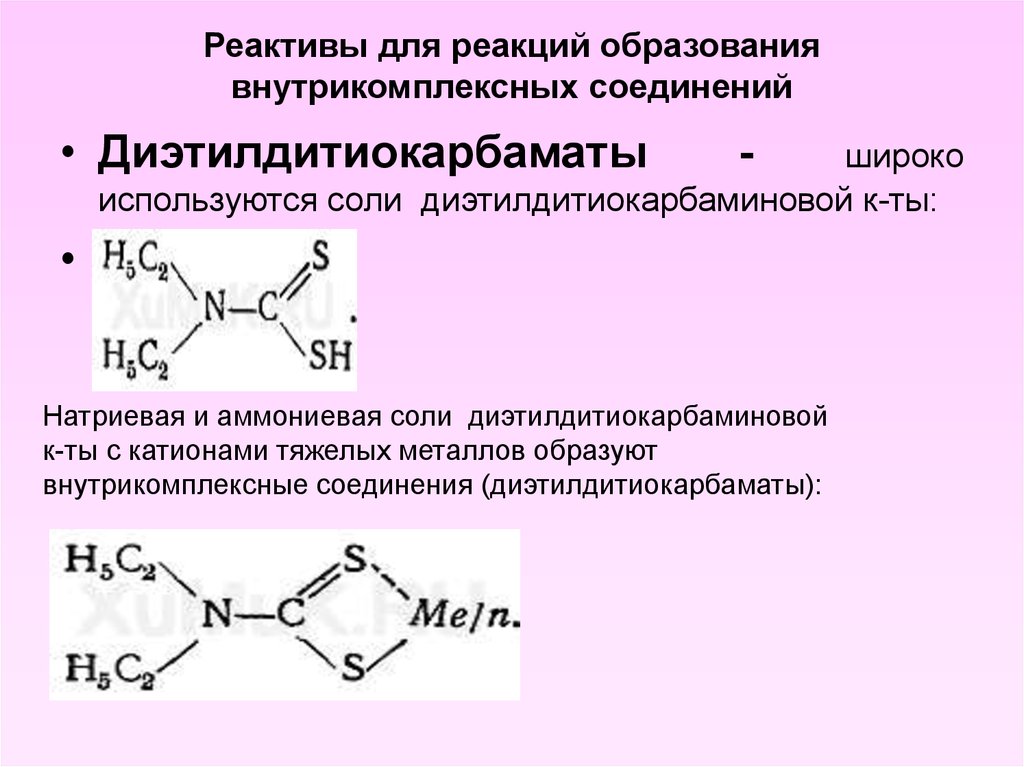 По возможности следует использовать автономный дыхательный аппарат (SCBA); если это невозможно, используйте уровень защиты выше или равный рекомендованному в разделе «Защитная одежда».
По возможности следует использовать автономный дыхательный аппарат (SCBA); если это невозможно, используйте уровень защиты выше или равный рекомендованному в разделе «Защитная одежда».
ПРОГЛАТЫВАНИЕ: НЕ ВЫЗЫВАТЬ РВОТУ. Если пострадавший в сознании и у него нет конвульсий, дайте 1-2 стакана воды для разбавления химиката и НЕМЕДЛЕННО позвоните в больницу или токсикологический центр. Будьте готовы доставить пострадавшего в больницу, если это будет рекомендовано врачом. Если пострадавший находится в судорогах или без сознания, ничего не давать ртом, убедиться, что дыхательные пути пострадавшего открыты, и уложить пострадавшего на бок так, чтобы голова была ниже туловища. НЕ ВЫЗЫВАЕТ РВОТУ. НЕМЕДЛЕННО доставьте пострадавшего в больницу. (НТП, 1992)
Физические свойства
Что это за информация?
Поля физических свойств
включают в себя такие свойства, как давление пара и
температура кипения, а также пределы взрываемости и
пороги токсического воздействия
Информация в CAMEO Chemicals поступает из различных источников. источники данных.
источники данных.
| Химическая формула: |
|
Температура вспышки: данные отсутствуют
Нижний предел взрываемости (НПВ): данные отсутствуют
Верхний предел взрываемости (ВПВ): данные отсутствуют
Температура самовоспламенения: данные отсутствуют
Температура плавления: 203°F (NTP, 1992)
Давление пара: данные недоступны
Плотность пара (относительно воздуха): 5,9 (НТП, 1992)
Удельный вес: 1.1 при 68°F (NTP, 1992)
Температура кипения: данные отсутствуют
Молекулярный вес: 171,27 (НТП, 1992)
Растворимость в воде: больше или равно 100 мг/мл при 57°F (НТП, 1992)
Энергия/потенциал ионизации: данные отсутствуют
IDLH: данные отсутствуют
AEGL (рекомендательные уровни острого воздействия)
Информация об AEGL отсутствует.ERPG (Руководство по планированию реагирования на чрезвычайные ситуации)
Информация о ERPG отсутствует.
PAC (критерии защитного действия)
| Химические вещества | ПАК-1 | ПАК-2 | ПАК-3 |
|---|---|---|---|
| Диэтилдитиокарбамат натрия; (Диэтилдитиокарбаминовая кислота, натриевая соль) (148-18-5) | 6 мг/м3 | 27 мг/м3 | 300 мг/м3 |
(DOE, 2018)
Нормативная информация
Что это за информация?
Поля нормативной информации
включить информацию из
Сводный список III Агентства по охране окружающей среды США
списки,
Химический завод Агентства кибербезопасности и безопасности инфраструктуры США
антитеррористические стандарты,
и Управление по охране труда и здоровья США
Перечень стандартов по управлению безопасностью технологического процесса при работе с особо опасными химическими веществами
(подробнее об этих
источники данных).
Сводный перечень списков EPA
Отсутствует нормативная информация.
Антитеррористические стандарты CISA Chemical Facility (CFATS)
Отсутствует нормативная информация.
Список стандартов OSHA по управлению безопасностью процессов (PSM)
Отсутствует нормативная информация.
Альтернативные химические названия
Что это за информация?
В этом разделе приводится список альтернативных названий этого химического вещества, включая торговые названия и синонимы.
- КАРБАМОВАЯ КИСЛОТА, ДИЭТИЛДИТИО-НАТРИЙНАЯ СОЛЬ
- КАРБАМОДИТИОЕВАЯ КИСЛОТА, ДЭТИЛОВАЯ, НАТРИЙНАЯ СОЛЬ
- МЕДЬ
- ДДК
- ДЭДК
- ДЭДК
- ДИТИЛ НАТРИЯ ДИТИОКАРБАМАТ
- ДИЭТИЛКАРБАМОДИТИОЕВАЯ КИСЛОТА, НАТРИЙНАЯ СОЛЬ
- ДИЭТИЛДИТИОКАРБАМАТ НАТРИЯ
- КИСЛОТА НАТРИЯ ДИЭТИЛДИТИОКАРБАНОВАЯ
- НАТРИЙНАЯ СОЛЬ ДИЭТИЛДИТИОКАРБАМОВОЙ КИСЛОТЫ
- ДИЭТИЛДИТИОКАРБАМОВАЯ КИСЛОТА, НАТРИЙНАЯ СОЛЬ
- ДИТИОКАРБ
- ДИТИОКАРБАМАТ
- ДИТОКАРБ НАТРИЯ
- ИМУТИОЛ
- КУПРАЛ
- N,N-ДИЭТИЛДИТИОКАРБАМОВАЯ КИСЛОТА, НАТРИЙНАЯ СОЛЬ
- NA-DDTC
- НКИ-C02835
- НОКСЕЛЕР SDC
- НАТРИЙ ДЭДТ
- НАТРИЯ ДИЭТИЛАМИНОКАРБОДИТИОАТ
- НАТРИЯ ДИЭТИЛАМИНОКАРБОДИТИОЛАТ
- НАТРИЯ ДИЭТИЛДИТИОКАРБАМАТ
- НАТРИЯ N,N-ДИЭТИЛДИТИОКАРБАМАТ
- НАТРИЙНАЯ СОЛЬ N,N-ДИЭТИЛДИТИОКАРБАМОВОЙ КИСЛОТЫ
- СОКСИНОЛ ESL
- ТИОКАРБ
- ВВС США ЕК-2596
Информация о веществе – ECHA
Диэтилдитиокарбамат натрия
Помощь
Ключевые наборы данных
ПОМОЩЬ
Нормативно-правовой контекст
Здесь вы можете найти все нормативы и нормативные списки, в которых фигурирует это вещество, согласно данным, доступным ECHA.
