Новые стандарты для чистых помещений: что это означает для фармацевтических производителей?
ISO 14644-4: Проектирование, сооружение и пускМеждународные эксперты внесли значительные изменения в стандарты серии ИСО 14644, связанные с чистотой воздуха по аэрозольным частицам, и теперь пришло время промышленности высказать свои комментарии по этому поводу
Начиная с 2000 года производственные предприятия, выпускающие продукцию в чистых помещениях и других контролируемых средах, использовали стандарты ИСО 14644-1 – «Часть 1: Классификация чистоты воздуха» и ИСО 14644-2 – «Часть 2: Требования к контролю и мониторингу для подтверждения постоянного соответствия ИСО 14644-1» в качестве международных стандартов для квалификации (аттестации) своих чистых помещений. В декабре прошлого года рабочая группа ИСО, разработавшая эти два основополагающих документа, выпустила пересмотренные версии стандартов в виде «Final Draft International Standards – FDIS», т. е. подготовленных к утверждению проектов новых версий вышеупомянутых стандартов. Хотя согласование и утверждение этих проектов в качестве международных стандартов еще впереди, FDIS-версии уже сейчас могут использоваться в качестве рекомендательных документов по соглашению между заказчиками и поставщиками. Таким образом, всем специалистам, которые связан с чистыми помещениями, очень важно понять не только процедурные изменения, содержащиеся в проектной версии новых стандартов, но также и причины внесения таких изменений.
е. подготовленных к утверждению проектов новых версий вышеупомянутых стандартов. Хотя согласование и утверждение этих проектов в качестве международных стандартов еще впереди, FDIS-версии уже сейчас могут использоваться в качестве рекомендательных документов по соглашению между заказчиками и поставщиками. Таким образом, всем специалистам, которые связан с чистыми помещениями, очень важно понять не только процедурные изменения, содержащиеся в проектной версии новых стандартов, но также и причины внесения таких изменений.
В новой FDIS-версии стандарта ИСО 14644-1 «Часть 1: Классификация чистоты воздуха» рабочая группа WG 1 технического комитета ISO/TC 209 (в которую входят эксперты, разработавшие исправления) представила упрощённый процесс классификации, использующий более точный метод, имеющий статистическую основу. Новая методика требует б?льшего количества точек отбора проб и предполагает случайный выбор их размещения, принимая во внимание различные уровни концентрации частиц в разных зонах чистого помещения. Такой подход позволяет обеспечить 95%-ную доверительную вероятность того, что не менее 90% площади чистого помещения соответствует требованиям по предельной концентрации частиц.
Такой подход позволяет обеспечить 95%-ную доверительную вероятность того, что не менее 90% площади чистого помещения соответствует требованиям по предельной концентрации частиц.
Как и в действующей редакции стандарта 1999 года, новая FDIS-версия ИСО 14644-1 определяет 9 классов чистоты, в каждом из которых задана максимально допустимая концентрация в зависимости от размера частиц для каждого класса (см. Таблицу 1 FDIS-версии ИСО 14644-1). Гордон Фаркварсон, ответственный за созыв рабочей группы WG 1 комитета ISO/TC 209 подчеркивает, что комитет намеренно избегал любых кардинальных изменений принципов, лежащих в основе определения классов чистоты. Так же, как и в действующем стандарте ИСО 14644-1:1999, новый стандарт ISO/FDIS 14644-1 устанавливает количество точек отбора проб для проведения классификации и критерии приёмки данных (см. Таблицу А.1 FDIS-версии ИСО 14644-1). Пользователи могут заметить критическую разницу между содержанием последней таблицы для выбора количества точек пробоотбора по сравнению с руководством, представленным в стандарте 1999 года.
Что же касается другого, сопутствующего документа, то разница между ИСО 14644-2:2000 и новой версией ISO/FDIS 14644-2 – «Часть 2: Требования к контролю и мониторингу для подтверждения постоянного соответствия ИСО 14644-1» отражает новую методику отбора проб в FDIS-версии ИСО 14644-1.
Итак, как же отразятся эти новые версии стандартов на производителях лекарственных средств и медицинских изделий? Ответ может измениться по мере прохождения документами процесса утверждения в качестве международных стандартов, но, начиная со стадии DIS (стадии рабочего проекта), эти документы в любое время можно использовать в договорных отношениях.
FDA США (Управление по контролю за продуктами и лекарственными препаратами) ещё должно публично высказаться о новых версиях этих стандартов. Однако Департамент производства и качества продукции в составе Центра по проверке и исследованию лекарственных средств FDA опубликовал официальное заявление, которое гласит: «FDA поддерживает усилия по созданию стандартов такими организациями как ISO, особенно когда документы гармонизированы в международном масштабе. Мы в 2004 году цитировали предыдущую версию ИСО 14644-1 в нашем документе «Указания по производству стерильных лекарственных средств в асептических процессах». В настоящее время у нас нет намерений публиковать свою позицию по стандарту ISO/DIS 14644-1, но мы с интересом рассмотрим его и будем надеяться на то, что многие предприятия начнут использовать данные нормативы для достижения соответствия сGMP».
Мы в 2004 году цитировали предыдущую версию ИСО 14644-1 в нашем документе «Указания по производству стерильных лекарственных средств в асептических процессах». В настоящее время у нас нет намерений публиковать свою позицию по стандарту ISO/DIS 14644-1, но мы с интересом рассмотрим его и будем надеяться на то, что многие предприятия начнут использовать данные нормативы для достижения соответствия сGMP».
Кроме того, в качестве члена консультационной группы по техническим вопросам от США – US Technical Advisory Group (US TAG) при ISO/TC 209 – FDA предоставит на рассмотрение в ИСО свои комментарии в течение шести месяцев – периода сбора отзывов, начинающегося со 2-го мая 2011 года. Отражая сбалансированный вклад американских производителей, пользователей и организаций, имеющих интерес в данной области, а также государственных экспертов, консультационная группа US TAG разрабатывает официальную позицию США в отношении DIS-версий вышеуказанных стандартов.
Анн Мари Диксон, глава делегации US TAG в комитете ISO/TC 209, объясняет, что выработка позиции США влечёт за собой активный запрос мнений от правительственных и неправительственных заинтересованных сторон через административный орган TAG – Институт исследований окружающей среды и технологий (IEST). «Новые версии стандартов влекут за собой значительные изменения процессов сертификации и, потенциально, квалификации (аттестации)» – отмечает госпожа Диксон. «Жизненно важно, чтобы все специалисты, чья сфера деятельности тесно связана с применением стандартов серии ИСО 14644, внимательно рассмотрели новые версии документов и статистику, скрывающуюся за ними». И добавляет – «Стандарты требуют достижения согласия, как при разработке, так и на практике. Период сбора отзывов предоставляет пользователям и представителям регуляторных органов уникальную возможность сформировать окончательные версии этих стандартов, что является жизненно важным для мировой промышленности и бизнеса» .
«Новые версии стандартов влекут за собой значительные изменения процессов сертификации и, потенциально, квалификации (аттестации)» – отмечает госпожа Диксон. «Жизненно важно, чтобы все специалисты, чья сфера деятельности тесно связана с применением стандартов серии ИСО 14644, внимательно рассмотрели новые версии документов и статистику, скрывающуюся за ними». И добавляет – «Стандарты требуют достижения согласия, как при разработке, так и на практике. Период сбора отзывов предоставляет пользователям и представителям регуляторных органов уникальную возможность сформировать окончательные версии этих стандартов, что является жизненно важным для мировой промышленности и бизнеса» .
Ответственный за созыв рабочей группы WG 1 Гордон Фаркварсон соглашается, замечая, что, так как новый вариант отбора проб сильно отличается от процедуры, принятой в стандарте 1999 года – «я подозреваю, что FDIS-версии стандарта ИСО 14644-1 вызовет гораздо большее количество отзывов, чем любая другая часть серии стандартов ИСО 14644».
Свою точку зрения Г. Фаркварсон поясняет тем, что «некоторым производителям фармацевтической продукции может не понравиться положение о случайном выборе точек отбора проб. Такой выбор точек при каждом измерении концентрации частиц в чистом помещении означает вероятность получения результатов, не совпадающих с результатами, полученными ранее». Он добавляет, что внедрение нового подхода потребует от производителей проверять большее количество точек отбора проб, в связи с чем «им придётся аннулировать свои текущие планы проведения измерений и составить их заново».
Понимая, что новый подход к отбору проб, скорее всего, вызовет расхождение во мнениях, Гордон Фаркварсон и другие члены рабочей группы WG 1 подготовили материал, опубликованный в виде статьи в январе этого года как специальное «ISO-издание» («Special ISO Edition») журнала IEST. Статья под названием «План отбора проб для классификации чистых помещений по аэрозольным частицам» сравнивает подходы к отбору проб в стандарте 1999 года и новой FDIS-версии этого стандарта, а также объясняет статистические соображения, лежащие в основе изменений. Статья доступна для ознакомления на сайте IEST (www.iest.org), и авторы поддерживают её повсеместное распространение с целью повысить понимание внесенных изменений, особенно в период сбора отзывов.
Статья доступна для ознакомления на сайте IEST (www.iest.org), и авторы поддерживают её повсеместное распространение с целью повысить понимание внесенных изменений, особенно в период сбора отзывов.
Роберт Милк (Robert Mielke), секретарь ISO/TC 209 и соавтор вышеупомянутой статьи в журнале IEST, предлагает производителям лекарственных средств и медицинских изделий держать в уме общую картину происходящего. «Хотя новые FDIS-версии стандартов ИСО 14644-1 и 14644-2 и логика, стоящая за ними, весьма важны, они описывают только часть того, что относится к квалификации и мониторингу чистых помещений в фармацевтической промышленности и производстве медицинских изделий» – говорит он. «Следует проводить дополнительные измерения, которые, в зависимости от расположения производства и производимого в данном чистом помещении продукта, могут включать микробиологические испытания, сканирование фильтров на утечку, измерения скорости воздушных потоков и другие. Также необходимо следовать предписаниям контролирующих ведомств, таким как руководства, разработанные FDA и EMA (Европейское медицинское агентство).
Хэйди Парсонс, технический редактор Института исследований окружающей среды и технологий (IEST)
“Чистые помещения и технологические среды” No 2 / 2011 г.
ГОСТ Р ИСО 14644-4-2002: Чистые помещения и связанные с ними контролируемые среды. Часть 4. Проектирование, строительство и ввод в эксплуатацию
Терминология ГОСТ Р ИСО 14644-4-2002: Чистые помещения и связанные с ними контролируемые среды. Часть 4. Проектирование, строительство и ввод в эксплуатацию оригинал документа:
3.10 ввод в эксплуатацию ( start-up): Действия по подготовке и переводу в эксплуатацию чистого помещения со всеми подсистемами, включая комплект документации, наличие обученного персонала, вспомогательных служб и пр.
Определения термина из разных документов: ввод в эксплуатацию ( start-up)
3.5 загрязнение ( contaminant): Любое вещество (частицы, молекулярные и биологические структуры), которое может неблагоприятно влиять на продукт или процесс.
Определения термина из разных документов: загрязнение ( contaminant)
3.1 комната переодевания ( changing room): Помещение, в котором персонал может надеть или снять одежду для чистого помещения.
Определения термина из разных документов: комната переодевания ( changing room)
3.6 неоднонаправленный поток воздуха ( non-unidirectional airflow): Распределение воздуха, при котором поступающий в чистую зону воздух смешивается с внутренним воздухом посредством подачи струи приточного воздуха.
Определения термина из разных документов: неоднонаправленный поток воздуха ( non-unidirectional airflow)
3.11 однонаправленный поток воздуха ( unidirectional airflow): Контролируемый поток воздуха с постоянной скоростью и примерно параллельными линиями тока по всему поперечному сечению чистой зоны.
Примечание — Поток воздуха такого типа непосредственно уносит частицы из чистой зоны.
Определения термина из разных документов: однонаправленный поток воздуха ( unidirectional airflow)
3. 8 предфильтр ( pre-filter): Воздушный фильтр, установленный перед другим фильтром с целью уменьшения загрязнения этого фильтра.
8 предфильтр ( pre-filter): Воздушный фильтр, установленный перед другим фильтром с целью уменьшения загрязнения этого фильтра.
Определения термина из разных документов: предфильтр ( pre-filter)
3.4 приемка ( commissioning): Последовательность плановых испытаний и регулировок, выполняемых для ввода в эксплуатацию системы чистых помещений в соответствии с заданными требованиями.
Определения термина из разных документов: приемка ( commissioning)
3.9 технологическое ядро ( process core): Пространство, в котором выполняется технологический процесс и осуществляется связь процесса с окружающей средой.
Определения термина из разных документов: технологическое ядро ( process core)
3.2 установка очистки воздуха ( clean air device): Оборудование для подготовки и распределения чистого воздуха с целью достижения определенных параметров окружающей среды.
Определения термина из разных документов: установка очистки воздуха ( clean air device)
3. 7 частица ( particle): По ГОСТ Р ИСО 14644-1.
7 частица ( particle): По ГОСТ Р ИСО 14644-1.
Определения термина из разных документов: частица ( particle)
3.3 чистота ( cleanliness): Состояние продукта, поверхности, устройства, газа, жидкости и т.п., при котором загрязнения не превышают установленный для них уровень.
Примечание — Возможно загрязнение частицами; оно может быть биологическим, молекулярным и др.
Определения термина из разных документов: чистота ( cleanliness)
Словарь-справочник терминов нормативно-технической документации. academic.ru. 2015.
Создание чистого помещения — начните с ISO 14644-4
Если вы посвятите значительную часть своей карьеры технологиям чистых помещений, у вас будет возможность спроектировать, построить или отремонтировать чистое помещение. Прежде чем приступить к любому проектированию или проекту, ключевой задачей любого пользователя является общее использование объекта — выполняемая операция и требования. Должны быть определены вопросы продукта, процесса, регулирования и качества, и эти параметры будут определять методы контроля, а также требования к чистоте и мониторингу чистого помещения. В стандарте ISO 14644-4 подробно описаны элементы, которые потребуются для планирования и проектирования, строительства и запуска, тестирования и утверждения, а также документации проекта чистого помещения. Основное внимание в стандарте уделяется определению требований к проектированию и строительству установки в чистых помещениях; однако он не предписывает конкретных технологических или договорных средств для выполнения этих требований. Предоставляется руководство по строительству, включая требования к запуску и квалификации. Как правило, основные элементы проектирования и конструкции, необходимые для обеспечения непрерывной удовлетворительной работы, определяются путем рассмотрения соответствующих аспектов эксплуатации и технического обслуживания.
Должны быть определены вопросы продукта, процесса, регулирования и качества, и эти параметры будут определять методы контроля, а также требования к чистоте и мониторингу чистого помещения. В стандарте ISO 14644-4 подробно описаны элементы, которые потребуются для планирования и проектирования, строительства и запуска, тестирования и утверждения, а также документации проекта чистого помещения. Основное внимание в стандарте уделяется определению требований к проектированию и строительству установки в чистых помещениях; однако он не предписывает конкретных технологических или договорных средств для выполнения этих требований. Предоставляется руководство по строительству, включая требования к запуску и квалификации. Как правило, основные элементы проектирования и конструкции, необходимые для обеспечения непрерывной удовлетворительной работы, определяются путем рассмотрения соответствующих аспектов эксплуатации и технического обслуживания.
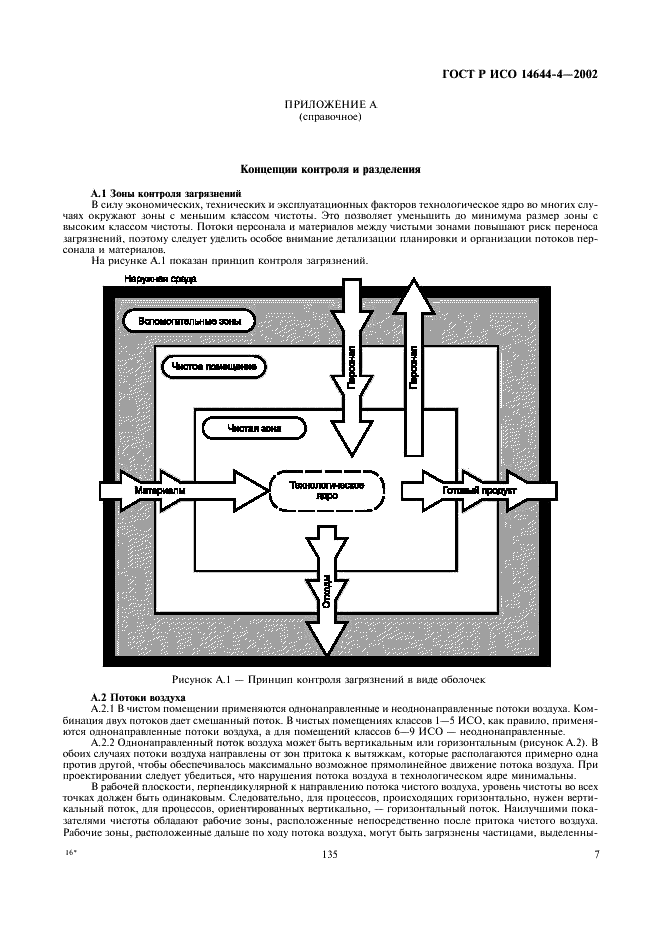
Приложение А стандарта ISO 14644-4 описывает зоны контроля загрязнения. Эти концепции изображены в виде основных эскизов, которые помогут пользователю в определении типов воздушного потока, разделения (люди и процесс) и давления. В приложении B предлагаются типы чистых помещений по отраслям и основные критерии проектирования (например, медицинские учреждения и микроэлектронные устройства).
Эти концепции изображены в виде основных эскизов, которые помогут пользователю в определении типов воздушного потока, разделения (люди и процесс) и давления. В приложении B предлагаются типы чистых помещений по отраслям и основные критерии проектирования (например, медицинские учреждения и микроэлектронные устройства).
Планировка и конфигурация любого чистого помещения должны поддерживать соответствующее оборудование, процесс, продукцию, безопасность, качество, перемещение персонала и материалов. Таким образом, проектирование представляет собой скоординированные усилия, направленные на решение всех проблем, связанных с исследованиями или производством, которые будут осуществляться в космосе. В любом процессе планирования разработка должна включать: стоимость, внешние факторы, строительство, сроки, варианты дизайна, контроль окружающей среды и другие факторы.
Приложения с B по G содержат рекомендации по этим вопросам, а также по фильтрации, вибрации и энергосбережению.
После того, как проект был квалифицирован и принят, надлежащее планирование позволит осуществлять контролируемое строительство, запуск и испытания объекта. Строительные работы по своей природе создают и генерируют твердые частицы, которые необходимо уменьшить и удалить на этом этапе. Система «чистого строительства» в этом стандарте ISO касается методов контроля риска нежелательного загрязнения во время строительства. Ввод в эксплуатацию, функциональные испытания, приемочные испытания и документация необходимы до любого пуска в эксплуатацию.
Приложение H этого стандарта представляет собой 13-страничный контрольный список элементов, которые могут повлиять на функциональность чистого помещения.
■ Требования к процессу
■ Загрязнители процесса
■ Спецификации процесса оборудования
■ Внешние факторы
■ Требования к окружающей среде
■ Безопасность
■ Избыточность системы
■ Операции и техническое обслуживание
■ Персонал, Эргономика, Эстетика
■ Будущие разработки
■ Столы
■ Столы ■ Столы ■ Столы ■ Столы ■ Столы ■ Столы ■ Столы ■ Столы ■ Столы ■ Столы ■ Столы ■ Столы ■ Столы ■ Ст. ■ Расписание■ Обзор требований, стандартов, состояния занятости и управления
Тщательное соблюдение условий руководства, изложенных в Приложении H, является обязательным для всех, кто занимается проектированием, строительством или эксплуатацией чистых помещений.
Контрольные списки, содержащиеся в стандарте, предоставляют пользователю список мелких и крупных деталей, которые могут быть забыты или упущены из виду в любом проекте чистых помещений. Думаете о новом объекте? Начните с ISO 14644-4 — небольшая инвестиция времени и средств.
ISO 14644-4 доступен на веб-сайте IEST (www.iest.org) или по телефону IEST (847) 255-1561.
Энн Мари Диксон является президентом Cleanroom Management Associates, Inc., консалтинговой фирмы, которая специализируется на конкурентном сравнительном анализе, обучении и аудите чистых и асептических операций и управления. Г-жа Диксон более 25 лет активно занимается контролем загрязнения и имеет обширный опыт в области обучения, написания технических документов, стратегического консультирования, запуска объекта, протоколов строительства и оптимизации процессов.
О IEST: Основанное в 1953 году, IEST является международным некоммерческим техническим обществом инженеров, ученых и педагогов, которое обслуживает своих членов и отрасли, которые они представляют (моделирование, тестирование, контроль и обучение окружающей среде земли и космоса). ) посредством обучения и разработки рекомендуемых практик и стандартов. IEST — организация по разработке стандартов, аккредитованная ANSI; Секретариат ISO/TC 209, Чистые помещения и связанные с ними контролируемые среды; Администратор US TAG, аккредитованного ANSI, согласно ISO/TC 209; Администратор US TAG, аккредитованного ANSI, по ISO/TC 142, Оборудование для очистки воздуха и других газов; и член-учредитель TAG США, аккредитованной ANSI, для ISO/TC 229, Нанотехнологии.
4 элемента проектирования, сертификации и обслуживания чистых помещений, часть 2
Элемент 2: воздушный поток
*Обновлено в августе 2018 г. по сравнению с исходной датой публикации 2014 г.
Одним из способов, которым AMCBP является «Построение интеллектуального будущего», является работа нашей группы по разработке решений для чистых помещений. В этой серии из 4 частей наш собственный Эмиль Борделон, сертифицированный специалист NEBB, описывает четыре основных элемента чистого помещения, которые учитываются на этапах проектирования / строительства, сертификации и технического обслуживания.
4 элемента:
- Фильтры HEPA/ULPA
- Воздушный поток
- Класс чистых помещений
- Комнатное давление
На этой неделе г-н Борделон расскажет о важности воздушного потока как части проектирования / строительства чистых помещений, сертификации и технического обслуживания.
Конструкция воздушного потока
В чистом помещении существует 3 различных типа воздушного потока:
Однонаправленный воздушный поток:
Однонаправленный воздушный поток определяется в зона с установившейся скоростью и приблизительно параллельными линиями тока». Он также указывается как ≤ 14º от перпендикуляра при выполнении параллелизма воздушного потока. В IEST RP-CC006.2 рекомендуется, чтобы чистое помещение с однонаправленным потоком воздуха имело покрытие фильтра менее 80%. Классы ISO с 1 по 5 рекомендуются для конструкций с однонаправленным воздушным потоком (см. таблицу B.2 стандарта ISO 14644-4 ниже). Ниже приведен пример чистого помещения с однонаправленным потоком воздуха:
Неоднонаправленный поток воздуха :
Однонаправленный поток воздуха определяется в ISO 14644-4 как «распределение воздуха, при котором приточный воздух, поступающий в чистую зону, смешивается с внутренним воздухом посредством всасывания». Классы ISO с 6 по 9 рекомендуются для конструкций с неоднонаправленным воздушным потоком (см. таблицу B.2 стандарта ISO 14644-4 ниже). Ниже приведен пример чистого помещения с неоднонаправленным потоком воздуха
Классы ISO с 6 по 9 рекомендуются для конструкций с неоднонаправленным воздушным потоком (см. таблицу B.2 стандарта ISO 14644-4 ниже). Ниже приведен пример чистого помещения с неоднонаправленным потоком воздуха
Смешанный поток воздуха:
Смешанный поток воздуха определяется в ISO 14644-4 как «комбинация однонаправленного и неоднонаправленного воздушных потоков». Ниже приведен пример чистого помещения со смешанным потоком воздуха:
Тестирование воздушного потока:
Существует два метода измерения воздушного потока в зависимости от типа используемого воздушного потока.
Однонаправленный воздушный поток:
Метод скорости воздушного потока используется в чистых помещениях с однонаправленным воздушным потоком. Тестовый прибор используется для измерения скорости воздуха на выходе из HEPA/ULPA-фильтра. Должна быть равномерная скорость воздушного потока ± 15 %. В некоторых случаях требуется более жесткая спецификация. Скорость измеряется в футах в минуту или метрах в секунду. В таблице B.2 стандарта ISO 14644-4 указан диапазон скорости воздушного потока в помещении для каждого класса ISO с 1 по 5. Это скорость воздушного потока в помещении, а не фильтр HEPA/ULPA. Они могут быть разными в зависимости от покрытия фильтра и высоты потолка.
Скорость измеряется в футах в минуту или метрах в секунду. В таблице B.2 стандарта ISO 14644-4 указан диапазон скорости воздушного потока в помещении для каждого класса ISO с 1 по 5. Это скорость воздушного потока в помещении, а не фильтр HEPA/ULPA. Они могут быть разными в зависимости от покрытия фильтра и высоты потолка.
Неоднонаправленный и смешанный воздушный поток:
Метод объемного воздушного потока используется в чистых помещениях с неоднонаправленным и смешанным воздушным потоком. Вытяжной колпак используется для измерения объема воздуха, выходящего из HEPA/ULPA-фильтра. Результаты испытаний сообщаются в кубических футах в минуту или литрах в секунду. Общий расход воздуха в помещении делится на объем помещения для расчета скорости воздухообмена в помещении в час. В таблице B.2 стандарта ISO 14644-4 указан диапазон воздухообмена в час для каждого класса ISO с 6 по 9..
Визуализация воздушного потока:
Существует два метода измерения визуализации воздушного потока.
Параллелизм:
Параллелизм воздушного потока используется в чистых помещениях с однонаправленным воздушным потоком для визуализации воздушного потока. Использование отвеса и нелиняющей нити с высоким отношением площади поверхности к весу (а именно потоком) для измерения угла отклонения воздушного потока от перпендикуляра. Ниже приведен пример стенда для проверки параллелизма.
Тест направленного воздушного потока:
Тест направленного воздушного потока используется в чистых помещениях с неоднонаправленным воздушным потоком. Этот тест включает использование видимого пара для визуализации направления воздушного потока и влияния технологического оборудования на воздушный поток. По этой причине фармацевтическая промышленность использует этот метод для чистых помещений как с однонаправленным, так и с неоднонаправленным потоком воздуха. Ниже приведен пример испытательного стенда направленного воздушного потока.
Дизайн чистого помещения:
Используя ISO 14644-4 Таблица B. 2 скоростей воздухообмена и скоростей в помещении, можно разработать базовую схему воздушного потока для чистого помещения. Ниже приведены два примера чистых помещений: однонаправленное и неоднонаправленное.
2 скоростей воздухообмена и скоростей в помещении, можно разработать базовую схему воздушного потока для чистого помещения. Ниже приведены два примера чистых помещений: однонаправленное и неоднонаправленное.
Неоднонаправленная конструкция:
Этот пример представляет собой чистую комнату класса ISO 6 размером 20 на 20 футов с потолками высотой 10 футов. Объем помещения составляет 4000 кубических футов. Рекомендуемый диапазон скорости воздухообмена по ISO 14644-4 для класса 6 составляет от 70 до 160 в час. При выборе среднего диапазона 115 воздухообменов в час общий требуемый объем в час составляет 460 000 кубических футов в час (4 000 x 115). Разделив общий объем в час на 60, мы получим 7667 кубических футов в минуту. Используя указанные 720 кубических футов в минуту на фильтр делим 7667 на 720 получаем 10,6 округляем до 11 фильтров. Это будет равно 1,98 смен в минуту или 118 смен в час. Эта комната будет иметь покрытие фильтра 22%.
Однонаправленная конструкция:
Этот пример представляет собой чистое помещение класса 4 ISO размером 20 на 20 футов с потолками высотой 10 футов. Объем помещения составляет 4000 кубических футов. Рекомендуемая комнатная скорость согласно ISO 14644-4 для класса 4 составляет 0,3–0,5 метра в секунду (от 59 до 98 футов в минуту). При выборе среднего диапазона 75 футов в минуту общий требуемый объем составляет 30 000 кубических футов в минуту (4000 x 75). Используя указанные 720 кубических футов в минуту на фильтр делим 30000 на 720 получаем 41,6 округляем до 42 фильтров. Это будет равняться 75,6 футов в минуту. Эта комната будет иметь покрытие фильтра 84%.
Объем помещения составляет 4000 кубических футов. Рекомендуемая комнатная скорость согласно ISO 14644-4 для класса 4 составляет 0,3–0,5 метра в секунду (от 59 до 98 футов в минуту). При выборе среднего диапазона 75 футов в минуту общий требуемый объем составляет 30 000 кубических футов в минуту (4000 x 75). Используя указанные 720 кубических футов в минуту на фильтр делим 30000 на 720 получаем 41,6 округляем до 42 фильтров. Это будет равняться 75,6 футов в минуту. Эта комната будет иметь покрытие фильтра 84%.
Используя ISO 14644-4, Таблица B.2, можно создать очень простую конструкцию воздушного потока, но перед тем, как будет сделан окончательный проект чистого помещения, необходимо учитывать другие факторы. Некоторые из этих факторов; отработанный воздух, подпиточный воздух, производственный процесс, тип используемых фильтров и т. д., но при понимании принципа построения воздушного потока этот выбор должен быть проще.
Как это использовать:
Более двадцати лет наша команда по разработке решений для чистых помещений предоставляет услуги по тестированию чистых помещений, сертификации, составлению отчетов, строительству и консультациям на различных рынках, таких как полупроводники, медико-биологические науки, технологии и исследования.