Что такое электролиз? Анод и катод. Физико-химический процесс
Образование 26 июля 2015Долгое время людям не удавалось получать многие чистые вещества в свободном виде. Такие, например, как:
- металлы;
- щелочи;
- хлор;
- водород;
- перекись водорода;
- хлорорганика и прочие.
Их получали либо с большим содержанием примесей, от которых невозможно было избавиться, либо не синтезировали вовсе. А ведь соединения очень важные для использования в промышленности и быту. Но с открытием такого процесса, как электролиз, задача огромного масштаба была решена. Сегодня он применяется не только для синтеза, но и для многих других процессов.
Что такое электролиз? Как он происходит, из каких этапов складывается, в чем заключается основное преимущество данного метода, попробуем разобраться в ходе статьи.
Что такое электролиз?
Чтобы ответить на данный вопрос, следует сначала обратиться к терминологии и уяснить некоторые основные физико-химические понятия.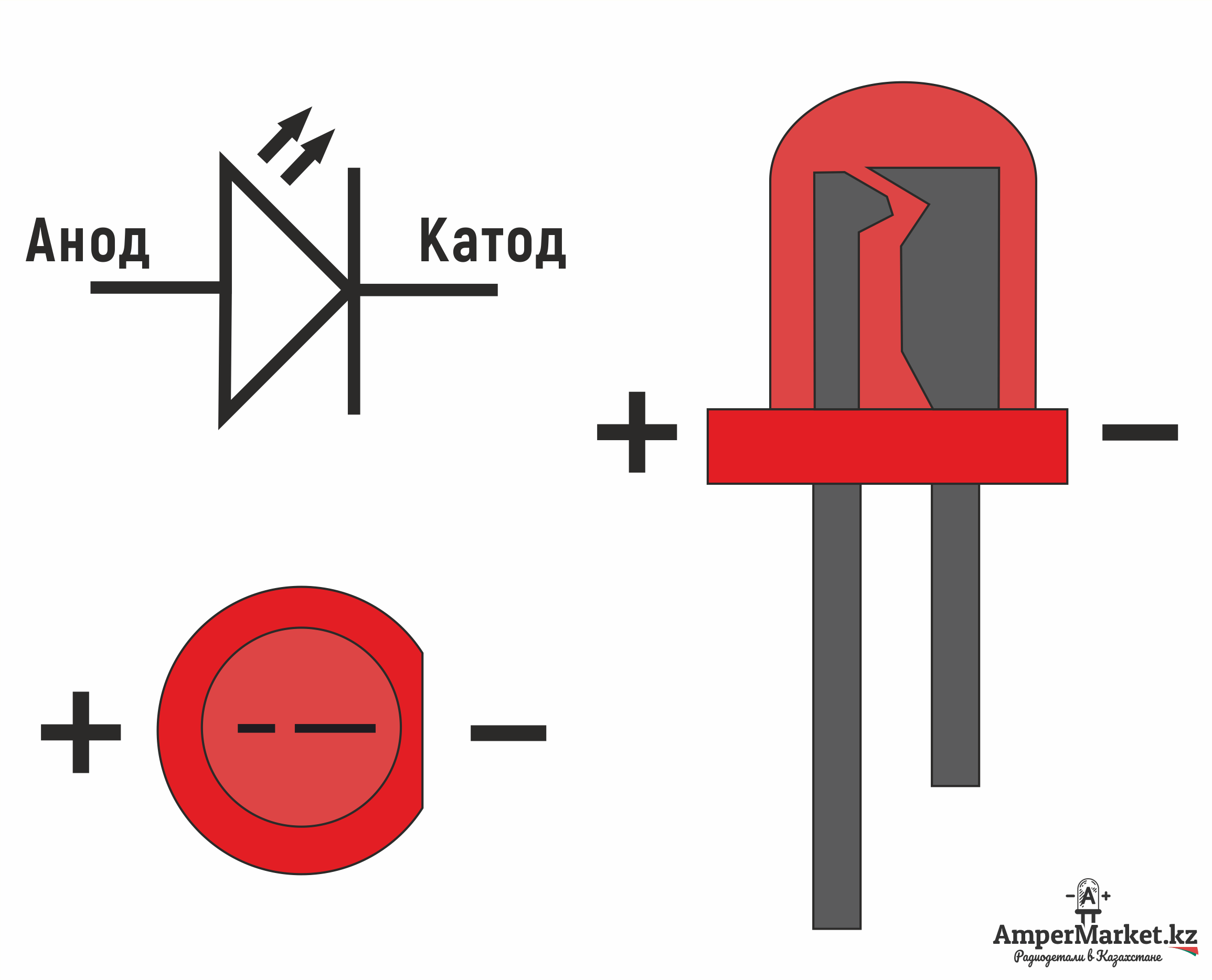
- Постоянный ток — это направленный поток электронов, исходящий от любого источника электричества.
- Электролит — вещество, раствор которого способен проводить электрический ток.
- Электроды — пластинки из определенных материалов, соединенные между собой, которые пропускают электричество через себя (анод и катод).
- Окислительно-восстановительная реакция — это процесс, при котором происходит изменение степеней окисления участников. То есть одни ионы окисляются и повышают значение степени окисления, другие, напротив, восстанавливаются, понижая ее.
Уяснив все эти термины, можно ответить на вопрос о том, что такое электролиз. Это окислительно-восстановительный процесс, заключающийся в пропускании постоянного тока через раствор электролита и завершающийся выделением разных продуктов на электродах.
Простейшая установка, которую можно назвать электролизером, включает в себя всего несколько компонентов:
- два стакана с электролитом;
- источник тока;
- два электрода, соединенных между собой.

В промышленности использует гораздо более сложные автоматизированные конструкции, позволяющие получать большие массы продуктов — электролизные ванны.
Процесс электролиза достаточно сложный, подчиняется нескольким теоретическим законам и протекает по установленным порядкам и правилам. Чтобы правильно предсказать его исход, необходимо четко усвоить все закономерности и возможные варианты прохождения.
Теоретические основы процесса
Самые главные основополагающие каноны, на которых держится электролиз, — законы Майкла Фарадея — знаменитого ученого-физика, известного своими работами в области изучения электрического тока и всех сопровождающих его процессов.
Всего таких правил два, каждое из которых описывает суть происходящих при электролизе процессов.
Первый закон
Первый закон Фарадея, формула которого записывается как m=kI*Δt, звучит следующим образом.
Масса вещества, выделяющегося на электроде, прямо пропорциональна тому электричеству, которое прошло через электролит.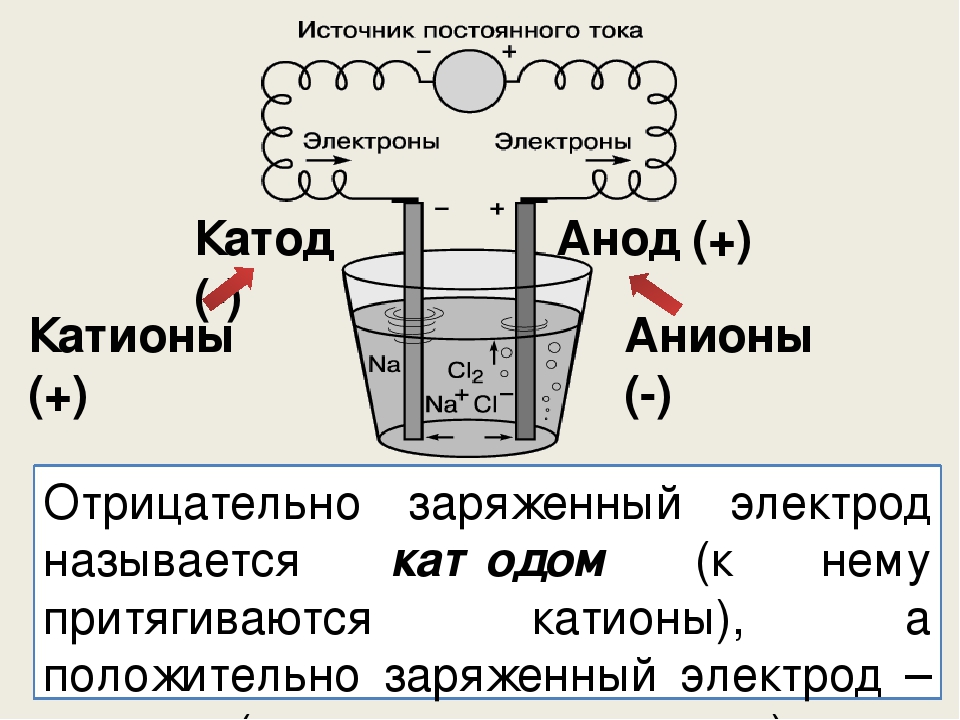
Из формулы видно, что m — это масса вещества, I — сила тока, Δt — время, в течение которого он пропускался. Также имеется значение k, которое называется электрохимическим эквивалентом соединения. Эта величина зависит от природы самого соединения. Численно k равно массе вещества, которое выделяется на электроде при пропускании через электролит одной единицы электрического заряда.
Второе правило электролиза
Второй закон Фарадея, формула которого — m=M*I*Δt/n*F, звучит следующим образом. Электрохимический эквивалент соединения (k) прямо пропорционален его молярной массе и обратно пропорционален валентности вещества.
Приведенная формула является результатом вывода из всех объединенных. Она отражает суть второго закона электролиза. М — молярная масса соединения, I — сила тока, пропущенного за весь процесс, Δt — время всего электролиза, F — постоянная Фарадея, n — электроны, которые участвовали в процессе. Их число равно заряду иона, принимавшего участие в процессе.
Законы Фарадея помогают понять, что такое электролиз, а также рассчитать возможный выход продукта по массе, спрогнозировать необходимый результат и повлиять на ход процесса. Они и составляют теоретическую основу рассматриваемых преобразований.
Понятие об аноде и его типы
Очень важное значение в электролизе имеют электроды. Весь процесс зависит от материала, из которого они изготовлены, от их специфических свойств и характера. Поэтому рассмотрим более подробно каждый из них.
Анод — плюс, или положительный электрод. То есть такой, который присоединяется к «+» полюсу источника питания. Соответственно, к нему из раствора электролита будут двигаться отрицательные ионы или анионы. Они будут окисляться здесь, приобретая более высокую степень окисления.
Поэтому можно изобразить небольшую схему, которая поможет запомнить анодные процессы: анод «плюс» — анионы — окисление. При этом существует два основных типа данного электрода, в зависимости от которых, будет получаться тот или иной продукт.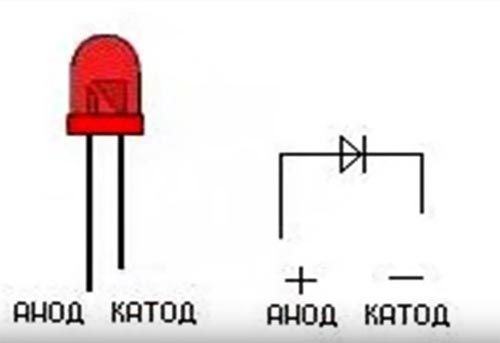
- Нерастворимый, или инертный анод. К такому типу относят электрод, который служит лишь для передачи электронов и процессов окисления, однако сам он при этом не расходуется и не растворяется. Таковыми анодами являются изготовленные из графита, иридия, платины, угля и так далее. Используя такие электроды, можно получать металлы в чистом виде, газы (кислород, водород, хлор и так далее).
- Растворимый анод. При окислительных процессах он сам растворяется и влияет на исход всего электролиза. Основные материалы, из которых изготавливаются подобного типа электроды: никель, медь, кадмий, свинец, олово, цинк и прочие. Использование таких анодов необходимо для процессов электрорафинирования металлов, гальванопластике, нанесения защитных покрытий от коррозии и так далее.
Суть всех происходящих процессов на положительном электроде сводится к тому, чтобы разрядились наиболее электроотрицательные по значению потенциала ионы. ИВот почему это делают анионы бескислородных кислот и гидроксид-ион, а потом вода, если речь идет о растворе. Кислородсодержащие анионы в водном растворе электролита вообще на аноде не разряжаются, так как вода делает это быстрее, высвобождая кислород.
Кислородсодержащие анионы в водном растворе электролита вообще на аноде не разряжаются, так как вода делает это быстрее, высвобождая кислород.
Катод и его характеристика
Катод — это отрицательно заряженный электрод (за счет скопления на нем электронов при пропускании электрического тока). Именно поэтому к нему движутся положительно заряженные ионы — катионы, которые претерпевают восстановление, то есть понижают степень окисления.
Здесь для запоминания также уместна схема: катод «минус» — катион — восстановление. В качестве материала для катода могут служить:
- нержавейка;
- медь;
- углерод;
- латунь;
- железо;
- алюминий и прочие.
Именно на этом электроде происходит восстановление металлов до чистых веществ, что является одним из основных способов получения их в промышленности. Также возможен переход электронов от анода к катоду, а если первый — растворимый, то его ионы восстанавливаются на отрицательном электроде.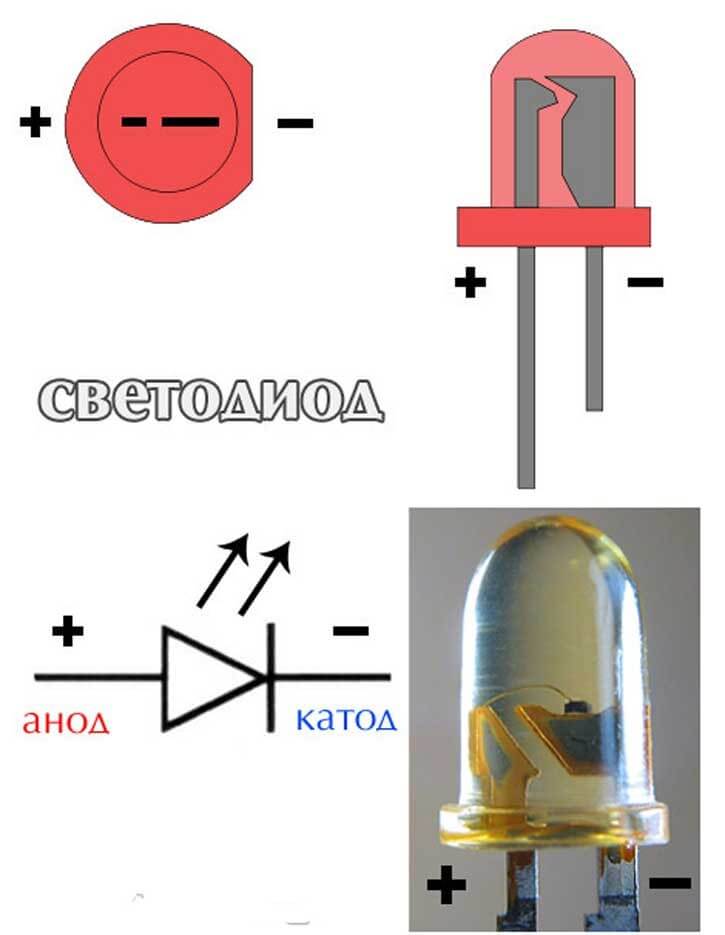 Здесь же происходит восстановление катионов водорода до газа Н2. Поэтому катод — это одна из самых важных частей в общей схеме процесса электролиза веществ.
Здесь же происходит восстановление катионов водорода до газа Н2. Поэтому катод — это одна из самых важных частей в общей схеме процесса электролиза веществ.
Электролиз расплавов
С точки зрения химии рассматриваемый процесс имеет свое уравнение. При помощи него можно изобразить всю схему на бумаге и предугадать результат. Самое главное, на что следует обращать внимание, — наличие или отсутствие водной среды и тип анода (растворимый или нет).
Если необходимо получение следующих продуктов: щелочных и щелочноземельных металлов, щелочей, алюминия, бериллия, газы из кислородсодержащих анионов, тогда не может идти речь об электролизе раствора электролита. Только расплав, потому что иначе требуемых соединений не получится. Именно поэтому часто в промышленности синтезируют перечисленные вещества, используя их безводные сухие соли и гидроксиды.
В целом уравнение электролиза расплава выглядит достаточно просто и стандартно. Например, если рассмотреть и записать его для йодида калия, то вид будет следующий:
KI = K+ + I—
Катод (К) «-«: К+ + 1е = К0
Анод (А) «+»: 2I— — 2e = I20
Итог процесса: KI = K + I2.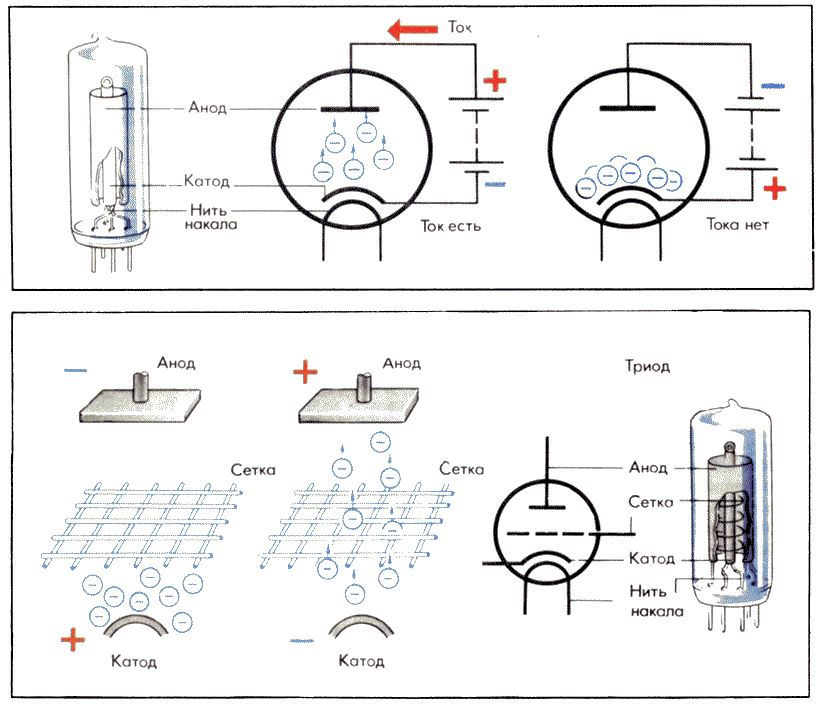
Точно так же будет записываться электролиз любого металла, независимо от значения его электродного потенциала.
Электролиз водного раствора
Если речь идет о растворах электролитов, то исход процесса будет совсем другой. Ведь вода становится активным участником. Она способна также диссоциировать на ионы и разряжаться у электродов. Поэтому в подобных случаях важное значение имеет электродный потенциал ионов. Чем его отрицательное значение ниже, тем больше вероятность более быстрого окисления или восстановления.
Электролиз водного раствора подчиняется нескольким правилам, которые следует запомнить.
- Анодные процессы: разряжаются только анионы бескислородных кислот (кроме фтороводородной). Если ион кислородсодержащий или фторид-ион, то окисляться будет вода с высвобождением кислорода.
- Катодные процессы: металлы в электрохимическом ряду напряжений (до алюминия включительно) на катоде не восстанавливаются вследствие высокой химической активности.
 Это делает вода с высвобождением водорода. Металлы от алюминия до водорода восстанавливаются одновременно с водой до простых веществ. Те же, что стоят после водорода в ряду напряжений (малоактивные), легко подвергаются восстановлению до простых веществ.
Это делает вода с высвобождением водорода. Металлы от алюминия до водорода восстанавливаются одновременно с водой до простых веществ. Те же, что стоят после водорода в ряду напряжений (малоактивные), легко подвергаются восстановлению до простых веществ.
Если следовать этим правилам, то можно изобразить любой электролиз и просчитать выход продукта. В случае с растворимым анодом схема меняется и становится гораздо более сложной.
Электролиз солей
Данные процессы используют для получения чистых металлов и газов, так как это технологически просто и экономически выгодно. К тому же продукты выходят с большой долей чистоты, что немаловажно.
Например, электролиз меди позволяет быстро получать ее в чистом виде из раствора любой соли. Чаще всего используется медный купорос или сульфат меди (II) — CuSO4.
Как из расплава, так и из раствора данной соли можно извлечь чистый металл, который так необходим практически во всех отраслях электротехники и металлостроительстве.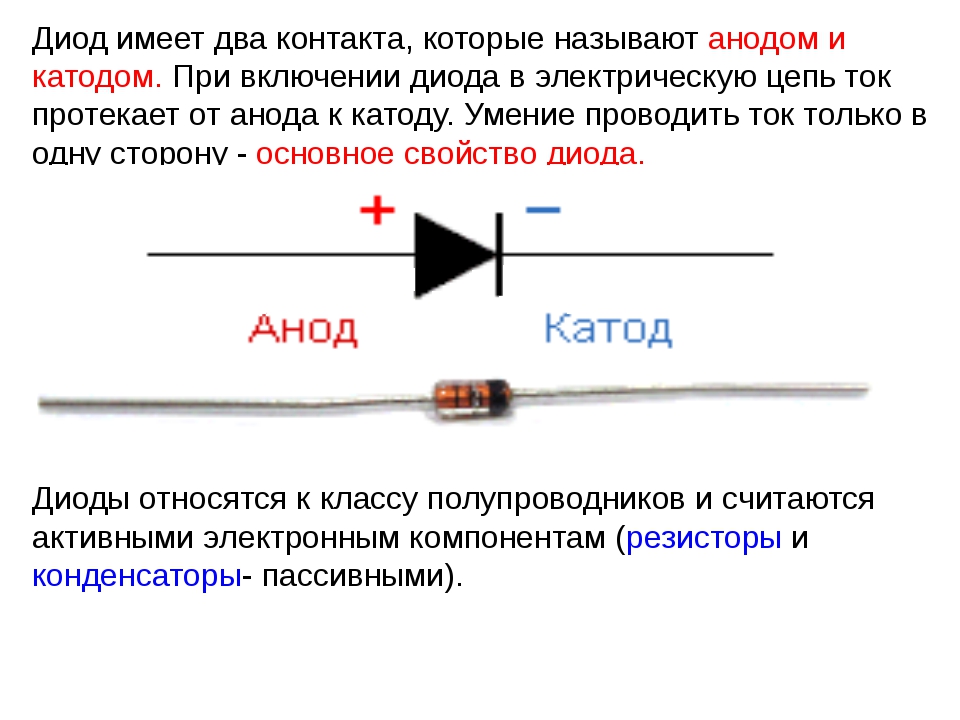
Значение и применение процесса
Электролиз — очень важный процесс. На его основе базируются такие необходимые технические операции, как:
- Рафинирование металлов.
- Электроэкстракция.
- Гальванотехника.
- Электросинтез.
- Нанесение антикоррозионных покрытий и другие.
Анод — Википедия. Что такое Анод
Ано́д (др.-греч. ἄνοδος — движение вверх) — электрод некоторого прибора, присоединённый к положительному полюсу источника питания. Электрический потенциал анода положителен по отношению к потенциалу катода (кроме гальванических элементов).[источник не указан 1317 дней]
Анод в электрохимии
При процессах электролиза (получение элементов из солевых растворов и расплавов под действием постоянного электрического тока), анод — электрически положительный полюс, на нём происходят окислительно-восстановительные реакции (окисление), результатом которых, в определённых условиях, может быть разрушение (растворение) анода, что используется, к примеру, при электрорафинировании металлов.
Аноды — множественное число слова «анод»; эта форма применяется преимущественно в металлургии, где применяются аноды для гальваники, используемые для нанесения на поверхность изделия слоя металла электрохимическим способом, либо для электрорафинирования, где металл с примесями растворяется на аноде и осаждается в очищенном виде на катоде. Основное распространение получили аноды из цинка (бывают сферические, литые и катаные, чаще используются последние), никеля, меди (среди которых отдельно выделяют медно-фосфористые, марки АМФ), кадмия (применение которых сокращается из-за экологической вредности), бронзы, олова (применяются при производстве печатных плат в радиоэлектронной промышленности), сплава свинца и сурьмы, серебра, золота и платины. Аноды из недрагоценных металлов применяются для повышения коррозионной стойкости, повышения эстетических свойств предметов и др. целей. Аноды из драгоценных металлов применяются гальваническим производством для повышения электропроводности изделий и др.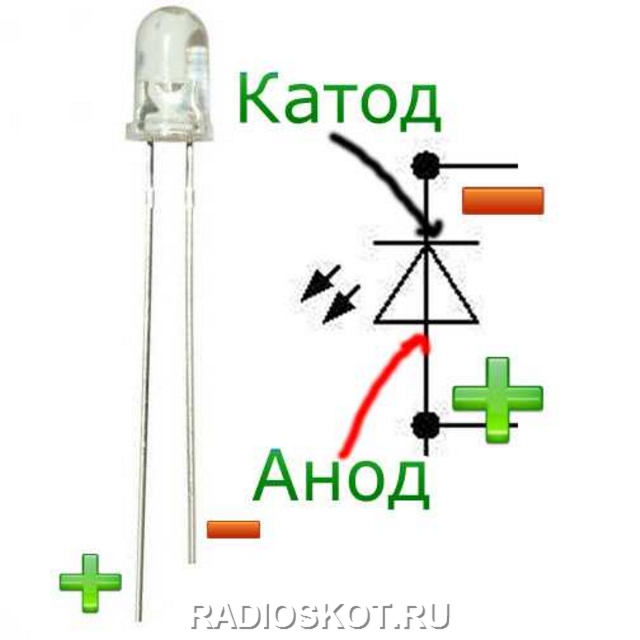
Кроме принудительной организации полезных электрохимических процессов, аноды применяются и для защиты от последствий нежелательных, побочных электрохимических процессов.
Анод в вакуумных электронных приборах
В вакуумных электронных приборах анод — электрод, который притягивает к себе летящие электроны, испущенные катодом. В электронных лампах и рентгеновских трубках конструкция анода такова, что он полностью поглощает электроны. А в электронно-лучевых приборах анод является элементом электронной пушки. Он поглощает лишь часть летящих электронов, формируя после себя электронный луч.
Анод у полупроводниковых приборов
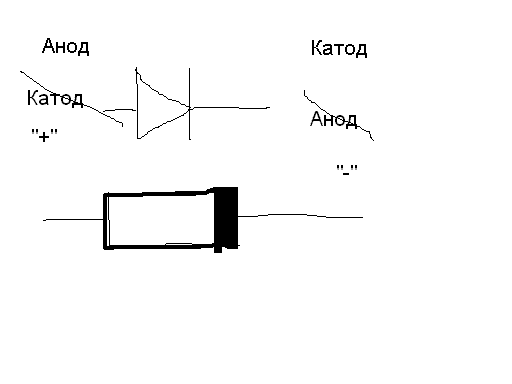
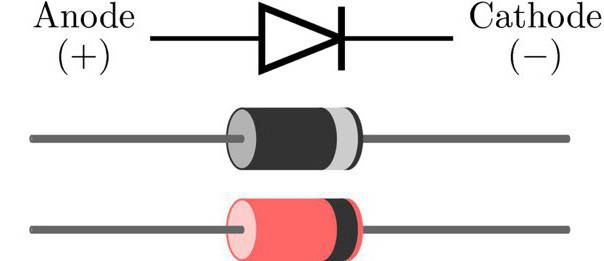
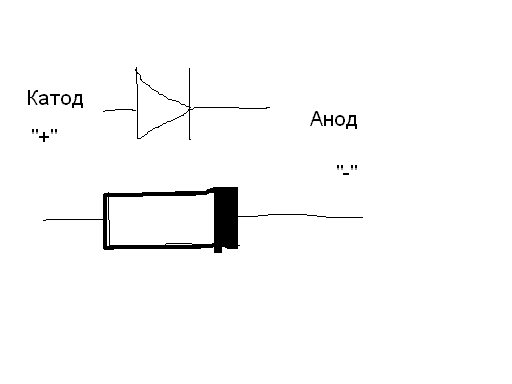
Электрод полупроводникового прибора (диода, тиристора), подключённый к положительному полюсу источника тока, когда прибор открыт (то есть имеет маленькое сопротивление), называют анодом, подключённый к отрицательному полюсу — катодом.
Знак анода и катода
В литературе встречается различное обозначение знака анода — «+» или «−», что определяется, в частности, особенностями рассматриваемых процессов.
В электрохимии принято считать, что катод — электрод, на котором происходит процесс восстановления, а анод — тот, где протекает окисление[1]. При работе электролизера (например, при рафинировании меди) внешний источник тока обеспечивает на одном из электродов избыток электронов (отрицательный заряд), здесь происходит восстановление металла, это катод. На другом электроде обеспечивается недостаток электронов и окисление металла, это анод.
В то же время при работе гальванического элемента (к примеру, медно-цинкового), избыток электронов (и отрицательный заряд) на одном из электродов обеспечивается не внешним источником тока, а собственно реакцией окисления металла (растворения цинка), то есть здесь отрицательным, если следовать приведённому определению, будет уже анод. Электроны, проходя через внешнюю цепь, расходуются на протекание реакции восстановления (меди), то есть катодом будет являться положительный электрод.
В соответствии с таким толкованием, для аккумулятора анод и катод меняются местами в зависимости от направления тока внутри аккумулятора[2][3].
В электротехнике анод — положительный электрод, ток течёт от анода к катоду, электроны, соответственно, наоборот.
См. также
Литература
- ↑ Антропов Л. И. Теоретическая электрохимия : Учеб. для хим.-технолог. спец. вузов. — 4-е изд., перераб. и доп. — М. : Высш. шк., 1984. — С. 13.
- ↑ Левин А. И. Теоретические основы электрохимии. — М.: Металлургиздат, 1963. — С. 131.
- ↑ Справочник по электрохимии / Под ред. А. М. Сухотина. — Л. : Химия, 1981. — С. 405.
Ссылки
по маркировке, внешнему виду и мультиметром
Для устройства точечного освещения мастера часто используют светодиоды. Эти маленькие лампочки при минимальном потреблении электроэнергии способны выдавать хорошую производительность. К тому же служат гораздо дольше обычных ламп накаливания. Но при монтаже цепи освещения важно учитывать полярность светодиода. Иначе он просто не сработает на подаваемый ток или быстро выйдет из строя.
Подробно о полярностях светодиодных ламп
Несоблюдение полярности и неправильное включение может привести к поломке светодиодаРаботают такие маленькие точки освещения по принципу протекания через них тока только в прямом направлении. От этого возникает оптическое излучение лампочки. Если полярности не соблюсти при подключении, ток не сможет проложить себе прямой путь по цепи. Соответственно, прибор освещения не заработает.
Таким образом, перед установкой светодиода мастер должен узнать расположение его катода и анода («+» и «—»). Сделать это не сложно, зная определенные принципы визуальной оценки лампочки или работы электроприборов в сочетании с ЛЕД-элементом.
Способы выявления полярности
Определение полярности светодиода по внешнему видуВыделяют несколько основных методов, по которым можно выяснить, где плюс у светодиода, а где минус. Самый простой способ — визуальный осмотр элемента и определение полярностей по внешнему виду.
Для новых LED-элементов характерной чертой является длина ножек. Анод (плюс) всегда будет длиннее катода (минуса). Как памятка мастеру — первая литера «К» от слова «катод» означает «короткий». Можно оценить визуально и колбу лампочки. Если она хорошо просматривается, мастер увидит так называемую «чашечку». В ней расположен кристаллик. Это и есть катод.
Анод (плюс) всегда будет длиннее катода (минуса). Как памятка мастеру — первая литера «К» от слова «катод» означает «короткий». Можно оценить визуально и колбу лампочки. Если она хорошо просматривается, мастер увидит так называемую «чашечку». В ней расположен кристаллик. Это и есть катод.
Нелишне обратить внимание и на ободок LED-детали. Многие производители предпочитают проставлять специальную маркировку-обозначение напротив катода. Она может выглядеть как засечка (риска), маленький срез или точка. Не увидеть их сложно.
Новый вариант маркировки светодиодов — значки «+» и «-» на цоколе. Таким образом производитель облегчает мастеру работу, помогает определять полярности. Иногда возможна маркировка зеленой линией напротив плюса.
Использование мультиметра
Определение полярности светодиода при помощи мультиметраЕсли определить светодиод – анод/катод – визуально не получается, можно использовать специальное оборудование. Таковым является мультиметр.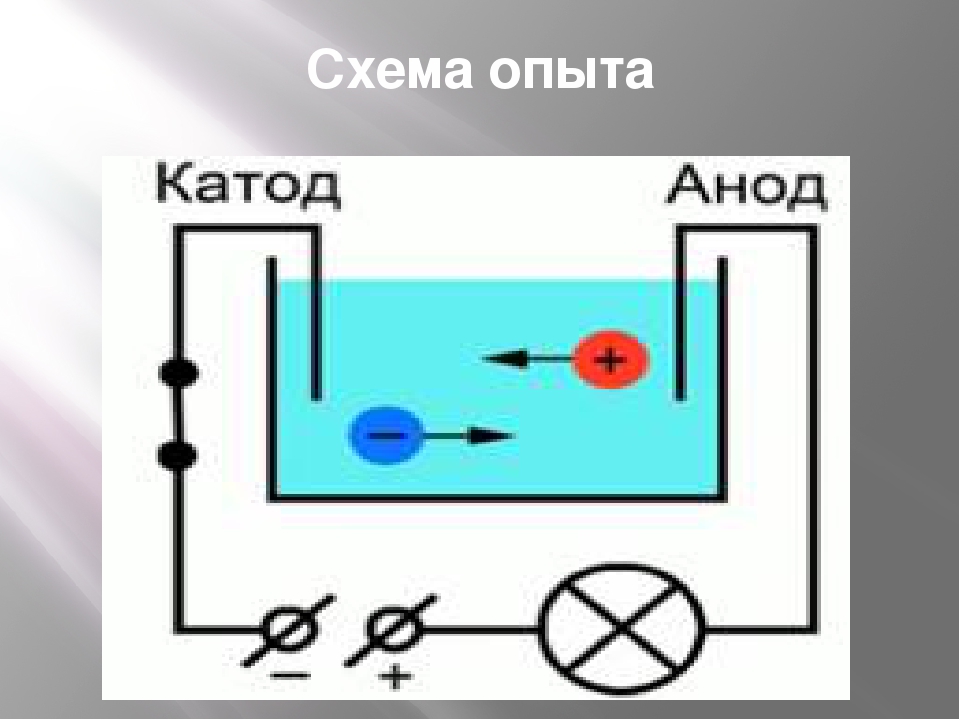 Вся процедура проверки займет не более минуты. Действуют таким образом:
Вся процедура проверки займет не более минуты. Действуют таким образом:
- На аппарате устанавливают режим измерения сопротивления.
- Щупы мультиметра аккуратно соединяют с ножками LED-лампочки. Предположительный плюс ставят к красному проводку. Минус — к черному. При этом касание делают кратковременным.
- Если контакты установлены правильно, аппарат покажет сопротивление, близкое к 1,7 кОм. При неправильном подключении ничего не произойдет.
Мультиметр можно эксплуатировать и в режиме проверки диодов. Здесь при правильном соблюдении полярностей лампочка даст свет. Особенно хорошо такая рекомендация работает с диодами зеленого и красного цветов. Белые и синие требуют напряжения более 3В, поэтому даже при правильном подключении могут не засветиться.
Чтобы проверить элементы этих колеров через мультиметр, можно применить режим определения характеристик транзистора. Он есть на всех современных моделях приборов. Здесь действуют так:
- Выставляют нужный режим.

- Лампочку ножками вставляют в специальные пазы С (коллектор) и Е (эмиттер). Они предназначены для транзистора в нижней части устройства.
Если минус светодиода подключен к коллектору, лампочка даст свет.
Метод подачи напряжения
Определение полярности светодиода методом подачи напряженияЧтобы определить полярности светодиода, можно использовать для этого источники напряжения (аккумуляторная батарейка). Но лучше всего применить лабораторный блок питания с наличием плавной регулировки напряжения, а также вольтметр постоянного тока.
Действуют таким образом:
- ЛЕД-лампочку подключают к источнику питания и медленно поднимают напряжение.
- Если полярности элемента соблюдены правильно, светодиод даст колер.
- Если при достижении 3-4 В лампочка так и не засветится, плюс и минус подключены неверно.
При срабатывании лампочки не нужно продолжать увеличивать напряжение. Элемент от таких экспериментов просто сгорит.
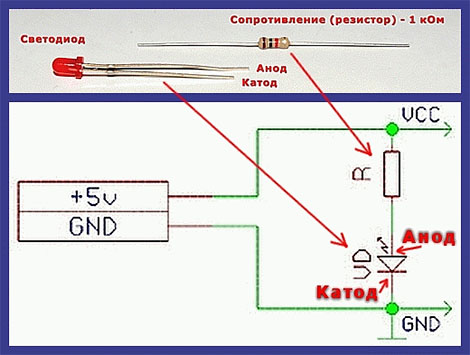
Если у мастера нет блока питания или батареи на 5-12 В, можно последовательно соединить между собой несколько элементов по 1,5 В. Пригодятся здесь аккумулятор от мобильного телефона или авто. Но стоит помнить: при подключении LED-элементов к мощным устройствам рекомендуется параллельно применять токоограничивающий резистор.
Определение полярности с помощью техдокументации
Если светодиод только что купленный, к нему прилагается техническая документация от производителя. Здесь указаны основные данные о лампочках:
- масса;
- цоколевка светодиодов;
- габариты;
- электрические параметры:
- иногда распиновка (схема подключения).
При покупке элементов в розницу можно попросить продавца дать ознакомиться с информацией, чтобы не мучиться дома и не искать, где у светодиодов плюс и минус. По бумагам делается соответствующий вывод.
Когда требуется определение полярностей LED-лампочек
Применение светодиодов в декорировании улицыМаленькие светодиоды широко применяются в различных областях, связанных с освещением и индикацией:
- уличное освещение: рекламные вывески, парковые подсветки;
- бытовые элементы искусственного света: освещение рабочих панелей, периметра подвесного потолка, встроенной мебели и др.
 ;
; - индикация электроприборов режимов вкл./выкл.: самодельные умные розетки и т.д.;
- детские игрушки;
- пульты ДУ и многое другое.
При выходе из строя лампочки мастер прибегает к её замене. При этом требуется определить анод и катод светодиода. В противном случае элемент просто не выдаст освещения.
На различных форумах есть информация о том, что нет смысла искать, где светодиод «прячет» плюс и минус. Нередки суждения, что лампочку можно подключать без соблюдения полярностей. Здесь есть нюансы. Даже если мастеру повезет и элемент даст свет, в конечном счете это приведет к таким последствиям:
- Ресурс работы неправильно подключенной лампочки, заявленный производителем, сократится в разы. К примеру, при гарантированном режиме 45000 часов светодиод отработает в два раза меньше.
- Производительность (интенсивность, яркость света) снизится в разы от той, которая должна быть. В общей цепи это будет видно невооруженным глазом.
Подобные игры с полярностями и вероятность работы диодного элемента напрямую зависят от характеристик конкретного полупроводника и напряжения пробоя.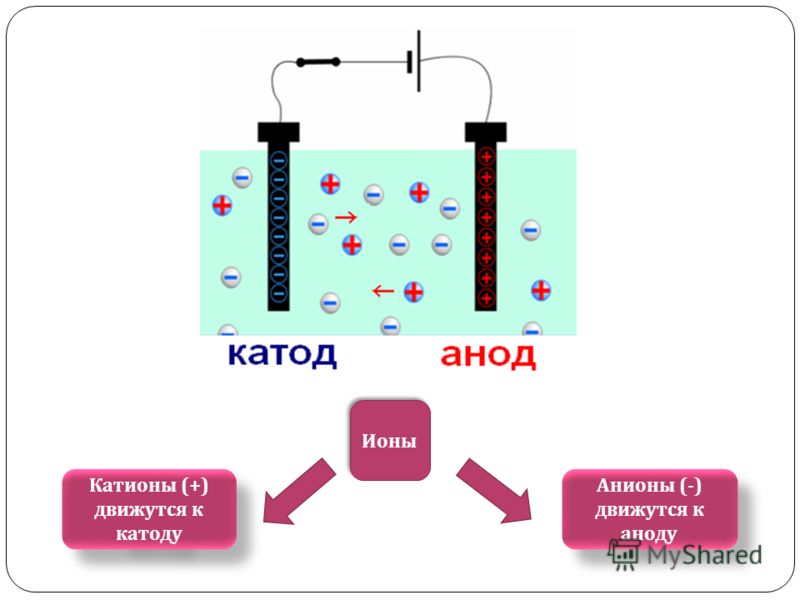
Средняя продолжительность LED-лампочек составляет 10 лет. При их влагозащите IP67 и более элементы можно смело использовать при устройстве уличного освещения. Чтобы светодиоды работали заявленный срок, стоит принципиально соблюдать полярности при их подключении и определяться с ними до проведения ремонтных работ, а не после.
- Как клеить бамбуковые обои: инструкция на видео
- Почему виниловые обои на кухне уместны
Катод — Википедия
Материал из Википедии — свободной энциклопедии
Схема гальванического элемента Даниэля-ЯкобиКатод (от греч. κάθοδος — ход вниз; нисхождение) — электрод некоторого прибора, присоединённый к отрицательному полюсу источника тока.
Катод в электрохимии и цветной металлургии
В электрохимии катод — электрод, на котором происходят реакции восстановления. Например, при электролитическом рафинировании металлов (меди, никеля и пр.) на катоде осаждается очищенный металл.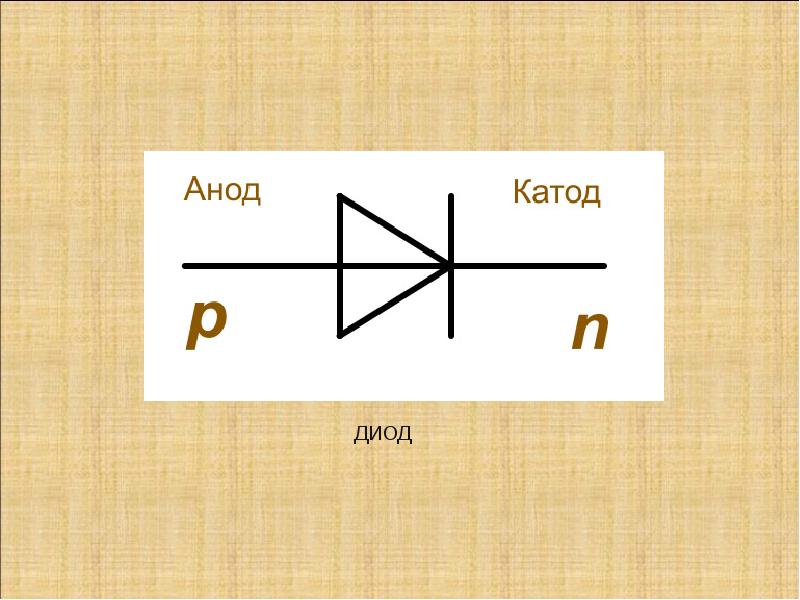 Получаемый металл также именуется катодом (катод медный[1], катод никелевый, катод цинковый и т.п.) и используется для последующего изготовления металлической продукции (проволоки, фольги, порошка, изделий и пр.). Для сдирания готового катода с постоянной катодной основы используются катодосдирочные машины.
Получаемый металл также именуется катодом (катод медный[1], катод никелевый, катод цинковый и т.п.) и используется для последующего изготовления металлической продукции (проволоки, фольги, порошка, изделий и пр.). Для сдирания готового катода с постоянной катодной основы используются катодосдирочные машины.
Катод в вакуумных электронных приборах
В вакуумных электронных приборах катод — электрод, который является источником свободных электронов, обычно вследствие термоэлектронной эмиссии. В электронно-лучевых приборах катод входит в состав электронной пушки. Для облегчения электронной эмиссии как правило, делается с нанесением металлов с малой работой выхода электрона и дополнительно подогревается. Различают катоды прямого накала, где нить накала непосредственно является источником электронов, и косвенного, где катод подогревается через керамический изолятор.
Катод у полупроводниковых приборов
Электрод полупроводникового прибора (диода, тиристора), подключенный к отрицательному полюсу источника тока, когда прибор открыт (то есть имеет маленькое сопротивление), называют катодом, подключённый к положительному полюсу — анодом.
Знак анода и катода
В литературе встречается различное обозначение знака катода — «-» или «+», что определяется, в частности, особенностями рассматриваемых процессов. В электрохимии принято считать, что «-» катод — электрод, на котором происходит процесс восстановления, а «+» анод — тот, где протекает процесс окисления[2][3]. При работе электролизера (например, при рафинировании меди) внешний источник тока обеспечивает на одном из электродов избыток электронов (отрицательный заряд), здесь происходит восстановление металла, это катод. На другом электроде обеспечивается недостаток электронов и окисление металла, это анод. В то же время при работе гальванического элемента (к примеру, медно-цинкового), избыток электронов (и отрицательный заряд) на одном из электродов обеспечивается не внешним источником тока, а собственно реакцией окисления металла (растворения цинка), то есть здесь отрицательным, если следовать приведённому определению, будет анод.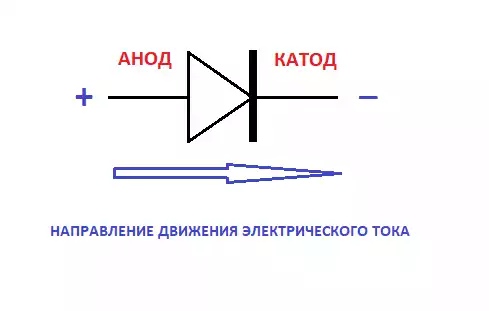 Электроны, проходя через внешнюю цепь, расходуются на протекание реакции восстановления (меди), то есть катодом будет являться положительный электрод. Так, на приведённой иллюстрации изображён обозначенный знаком «-» катод гальванического элемента, на котором происходит восстановление меди. В соответствии с таким толкованием, для аккумулятора знак анода и катода меняется в зависимости от направления протекания тока.[3][4][5].
Электроны, проходя через внешнюю цепь, расходуются на протекание реакции восстановления (меди), то есть катодом будет являться положительный электрод. Так, на приведённой иллюстрации изображён обозначенный знаком «-» катод гальванического элемента, на котором происходит восстановление меди. В соответствии с таким толкованием, для аккумулятора знак анода и катода меняется в зависимости от направления протекания тока.[3][4][5].
В электротехнике за направление тока принято считать направление движения положительных зарядов, отрицательный электрод «−» (Zn) — катод, положительный «+» (Cu) — анод, ток течёт от анода к катоду, электроны, соответственно, наоборот, от «−» (Zn) к «+» (Cu).
См. также
Литература
- ↑ ГОСТ 546-2001 Катоды медные. Технические условия
- ↑ Антропов Л. И. Теоретическая электрохимия : Учеб. для хим.-технолог. спец. вузов. — 4-е изд., перераб. и доп. — М. : Высш. шк., 1984. — С. 13.
- ↑ 1 2 Лукомский Ю.
 Я., Гамбург Ю. Д. Физико-химические основы электрохимии: Учебник. — Долгопрудный : Издательский Дом «Интеллект», 2008. — С. 19 — ISBN 978-5-91559-007-5
Я., Гамбург Ю. Д. Физико-химические основы электрохимии: Учебник. — Долгопрудный : Издательский Дом «Интеллект», 2008. — С. 19 — ISBN 978-5-91559-007-5 - ↑ Левин А. И. Теоретические основы электрохимии. — М.: Металлургиздат, 1963. — С. 131.
- ↑ Справочник по электрохимии / Под ред. А. М. Сухотина. — Л. : Химия, 1981. — С. 405.
Ссылки
Анод — Википедия. Что такое Анод
Ано́д (др.-греч. ἄνοδος — движение вверх) — электрод некоторого прибора, присоединённый к положительному полюсу источника питания. Электрический потенциал анода положителен по отношению к потенциалу катода (кроме гальванических элементов).[источник не указан 1317 дней]
Анод в электрохимии
При процессах электролиза (получение элементов из солевых растворов и расплавов под действием постоянного электрического тока), анод — электрически положительный полюс, на нём происходят окислительно-восстановительные реакции (окисление), результатом которых, в определённых условиях, может быть разрушение (растворение) анода, что используется, к примеру, при электрорафинировании металлов.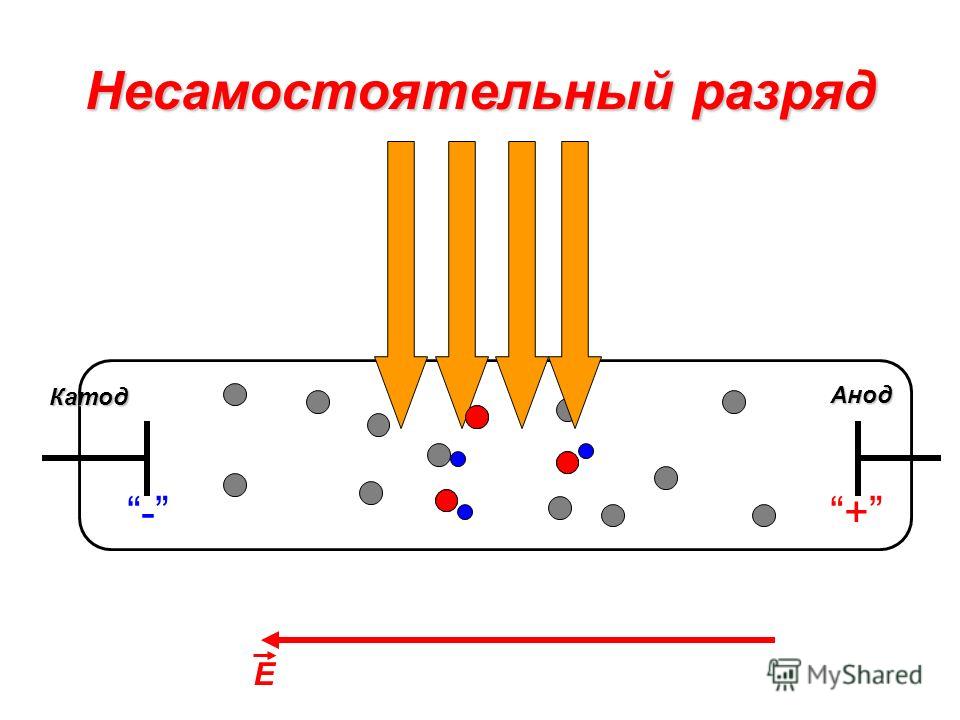
Аноды — множественное число слова «анод»; эта форма применяется преимущественно в металлургии, где применяются аноды для гальваники, используемые для нанесения на поверхность изделия слоя металла электрохимическим способом, либо для электрорафинирования, где металл с примесями растворяется на аноде и осаждается в очищенном виде на катоде. Основное распространение получили аноды из цинка (бывают сферические, литые и катаные, чаще используются последние), никеля, меди (среди которых отдельно выделяют медно-фосфористые, марки АМФ), кадмия (применение которых сокращается из-за экологической вредности), бронзы, олова (применяются при производстве печатных плат в радиоэлектронной промышленности), сплава свинца и сурьмы, серебра, золота и платины. Аноды из недрагоценных металлов применяются для повышения коррозионной стойкости, повышения эстетических свойств предметов и др. целей. Аноды из драгоценных металлов применяются гальваническим производством для повышения электропроводности изделий и др.
Кроме принудительной организации полезных электрохимических процессов, аноды применяются и для защиты от последствий нежелательных, побочных электрохимических процессов.
Анод в вакуумных электронных приборах
В вакуумных электронных приборах анод — электрод, который притягивает к себе летящие электроны, испущенные катодом. В электронных лампах и рентгеновских трубках конструкция анода такова, что он полностью поглощает электроны. А в электронно-лучевых приборах анод является элементом электронной пушки. Он поглощает лишь часть летящих электронов, формируя после себя электронный луч.
Анод у полупроводниковых приборов
Электрод полупроводникового прибора (диода, тиристора), подключённый к положительному полюсу источника тока, когда прибор открыт (то есть имеет маленькое сопротивление), называют анодом, подключённый к отрицательному полюсу — катодом.
Знак анода и катода
В литературе встречается различное обозначение знака анода — «+» или «−», что определяется, в частности, особенностями рассматриваемых процессов.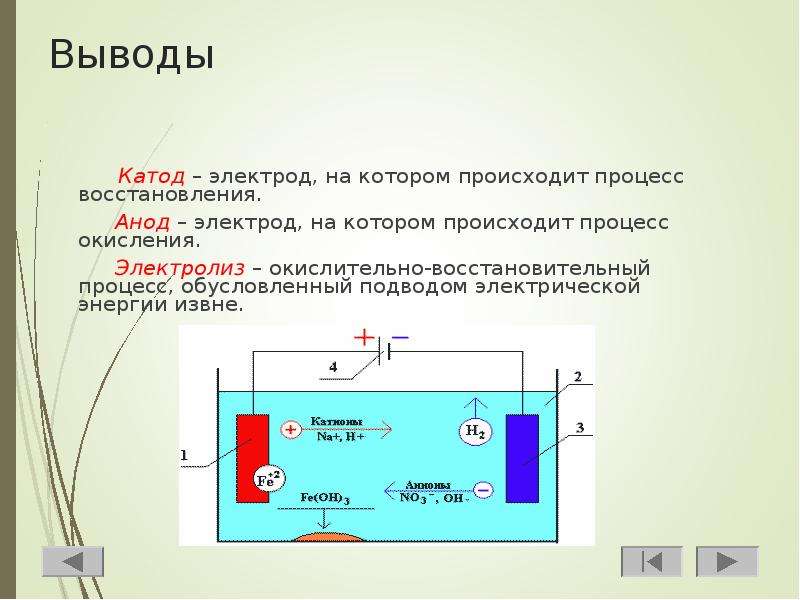
В электрохимии принято считать, что катод — электрод, на котором происходит процесс восстановления, а анод — тот, где протекает окисление[1]. При работе электролизера (например, при рафинировании меди) внешний источник тока обеспечивает на одном из электродов избыток электронов (отрицательный заряд), здесь происходит восстановление металла, это катод. На другом электроде обеспечивается недостаток электронов и окисление металла, это анод.
В то же время при работе гальванического элемента (к примеру, медно-цинкового), избыток электронов (и отрицательный заряд) на одном из электродов обеспечивается не внешним источником тока, а собственно реакцией окисления металла (растворения цинка), то есть здесь отрицательным, если следовать приведённому определению, будет уже анод. Электроны, проходя через внешнюю цепь, расходуются на протекание реакции восстановления (меди), то есть катодом будет являться положительный электрод.
В соответствии с таким толкованием, для аккумулятора анод и катод меняются местами в зависимости от направления тока внутри аккумулятора[2][3].
В электротехнике анод — положительный электрод, ток течёт от анода к катоду, электроны, соответственно, наоборот.
См. также
Литература
- ↑ Антропов Л. И. Теоретическая электрохимия : Учеб. для хим.-технолог. спец. вузов. — 4-е изд., перераб. и доп. — М. : Высш. шк., 1984. — С. 13.
- ↑ Левин А. И. Теоретические основы электрохимии. — М.: Металлургиздат, 1963. — С. 131.
- ↑ Справочник по электрохимии / Под ред. А. М. Сухотина. — Л. : Химия, 1981. — С. 405.
Ссылки
Анод и катод. Физико-химический процесс электролиза
Анод и катод. Физико-химический процесс электролиза li { font-size:1.06rem; } }.sidebar .widget { padding-left: 20px; padding-right: 20px; padding-top: 20px; }::selection { background-color: #4f4f4f; } ::-moz-selection { background-color: #4f4f4f; }a,.themeform label .required,#flexslider-featured .flex-direction-nav .flex-next:hover,#flexslider-featured .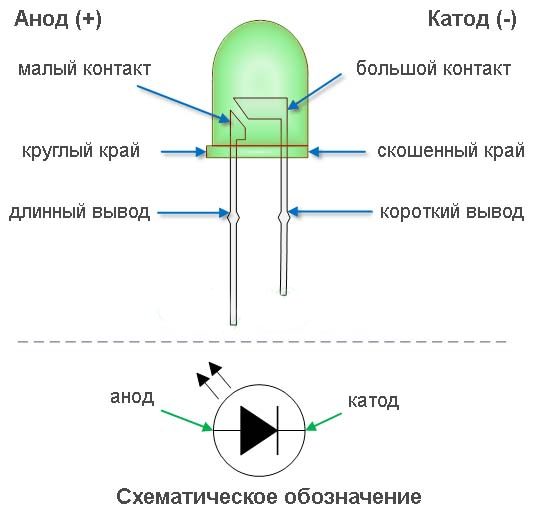 flex-direction-nav .flex-prev:hover,.post-hover:hover .post-title a,.post-title a:hover,.sidebar.s1 .post-nav li a:hover i,.content .post-nav li a:hover i,.post-related a:hover,.sidebar.s1 .widget_rss ul li a,#footer .widget_rss ul li a,.sidebar.s1 .widget_calendar a,#footer .widget_calendar a,.sidebar.s1 .alx-tab .tab-item-category a,.sidebar.s1 .alx-posts .post-item-category a,.sidebar.s1 .alx-tab li:hover .tab-item-title a,.sidebar.s1 .alx-tab li:hover .tab-item-comment a,.sidebar.s1 .alx-posts li:hover .post-item-title a,#footer .alx-tab .tab-item-category a,#footer .alx-posts .post-item-category a,#footer .alx-tab li:hover .tab-item-title a,#footer .alx-tab li:hover .tab-item-comment a,#footer .alx-posts li:hover .post-item-title a,.comment-tabs li.active a,.comment-awaiting-moderation,.child-menu a:hover,.child-menu .current_page_item > a,.wp-pagenavi a,.entry.woocommerce div.product .woocommerce-tabs ul.tabs li.active a{ color: #4f4f4f; }.themeform input[type=»submit»],.themeform button[type=»submit»],.
flex-direction-nav .flex-prev:hover,.post-hover:hover .post-title a,.post-title a:hover,.sidebar.s1 .post-nav li a:hover i,.content .post-nav li a:hover i,.post-related a:hover,.sidebar.s1 .widget_rss ul li a,#footer .widget_rss ul li a,.sidebar.s1 .widget_calendar a,#footer .widget_calendar a,.sidebar.s1 .alx-tab .tab-item-category a,.sidebar.s1 .alx-posts .post-item-category a,.sidebar.s1 .alx-tab li:hover .tab-item-title a,.sidebar.s1 .alx-tab li:hover .tab-item-comment a,.sidebar.s1 .alx-posts li:hover .post-item-title a,#footer .alx-tab .tab-item-category a,#footer .alx-posts .post-item-category a,#footer .alx-tab li:hover .tab-item-title a,#footer .alx-tab li:hover .tab-item-comment a,#footer .alx-posts li:hover .post-item-title a,.comment-tabs li.active a,.comment-awaiting-moderation,.child-menu a:hover,.child-menu .current_page_item > a,.wp-pagenavi a,.entry.woocommerce div.product .woocommerce-tabs ul.tabs li.active a{ color: #4f4f4f; }.themeform input[type=»submit»],.themeform button[type=»submit»],.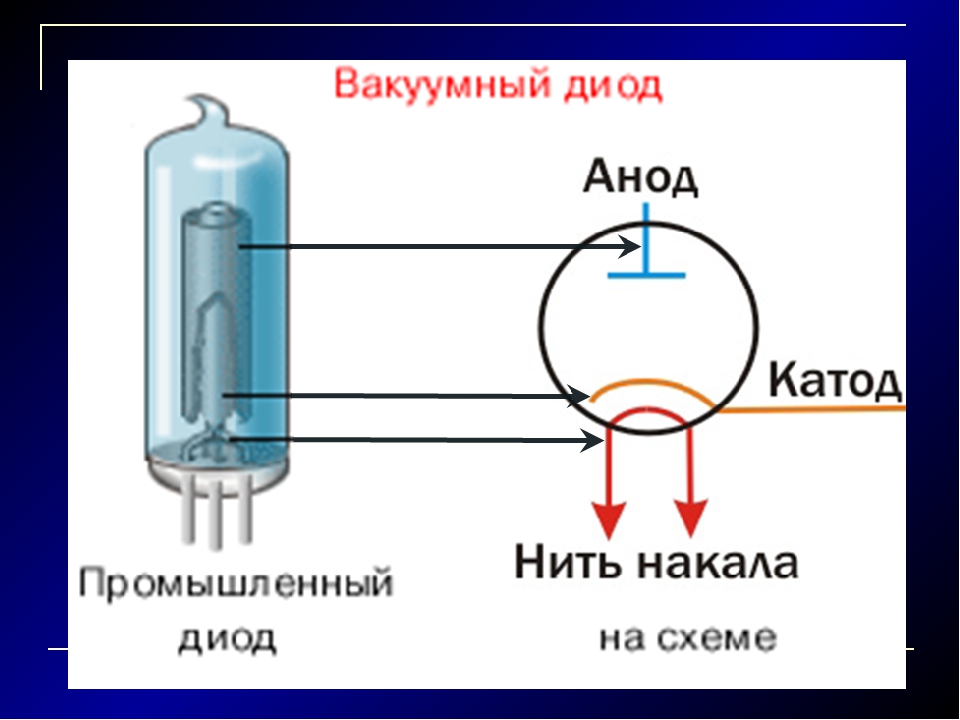 sidebar.s1 .sidebar-top,.sidebar.s1 .sidebar-toggle,#flexslider-featured .flex-control-nav li a.flex-active,.post-tags a:hover,.sidebar.s1 .widget_calendar caption,#footer .widget_calendar caption,.author-bio .bio-avatar:after,.commentlist li.bypostauthor > .comment-body:after,.commentlist li.comment-author-admin > .comment-body:after,.themeform .woocommerce #respond input#submit.alt,.themeform .woocommerce a.button.alt,.themeform .woocommerce button.button.alt,.themeform .woocommerce input.button.alt{ background-color: #4f4f4f; }.post-format .format-container { border-color: #4f4f4f; }.sidebar.s1 .alx-tabs-nav li.active a,#footer .alx-tabs-nav li.active a,.comment-tabs li.active a,.wp-pagenavi a:hover,.wp-pagenavi a:active,.wp-pagenavi span.current,.entry.woocommerce div.product .woocommerce-tabs ul.tabs li.active a{ border-bottom-color: #4f4f4f!important; } .search-expand,
#nav-topbar.nav-container { background-color: #282828}@media only screen and (min-width: 720px) {
#nav-topbar .
sidebar.s1 .sidebar-top,.sidebar.s1 .sidebar-toggle,#flexslider-featured .flex-control-nav li a.flex-active,.post-tags a:hover,.sidebar.s1 .widget_calendar caption,#footer .widget_calendar caption,.author-bio .bio-avatar:after,.commentlist li.bypostauthor > .comment-body:after,.commentlist li.comment-author-admin > .comment-body:after,.themeform .woocommerce #respond input#submit.alt,.themeform .woocommerce a.button.alt,.themeform .woocommerce button.button.alt,.themeform .woocommerce input.button.alt{ background-color: #4f4f4f; }.post-format .format-container { border-color: #4f4f4f; }.sidebar.s1 .alx-tabs-nav li.active a,#footer .alx-tabs-nav li.active a,.comment-tabs li.active a,.wp-pagenavi a:hover,.wp-pagenavi a:active,.wp-pagenavi span.current,.entry.woocommerce div.product .woocommerce-tabs ul.tabs li.active a{ border-bottom-color: #4f4f4f!important; } .search-expand,
#nav-topbar.nav-container { background-color: #282828}@media only screen and (min-width: 720px) {
#nav-topbar .Анод и катод | определение анода и катода в Медицинском словаре
электрод
[e-lek´trōd] любой из двух выводов электропроводящей системы или ячейки; в частности, неизолированная часть провода, которая находится в прямом контакте с телом.каломельный электрод способный как собирать, так и отдавать хлорид-ионы в нейтральной или кислой водной среде, состоящий из ртути в контакте с хлоридом ртути; используется в качестве электрода сравнения при измерениях pH.
деполяризующий электрод электрод, сопротивление которого больше, чем сопротивление части тела, заключенной в цепь.
водородный электрод электрод, изготовленный путем нанесения платиновой черни на платину с последующим поглощением газообразного водорода до насыщения; используется для определения концентрации ионов водорода.
индифферентный электрод на один больше терапевтического электрода, рассеивающий электрическую стимуляцию на большей площади.
точечный электрод электрод, имеющий на одном конце металлический острие; используется при подаче тока.
терапевтический электрод на один меньший, чем индифферентный электрод, производящий электрическую стимуляцию в концентрированной области; также называется активным электродом.Энциклопедия и словарь Миллера-Кина по медицине, сестринскому делу и смежному здоровью, седьмое издание. © 2003 Saunders, принадлежность Elsevier, Inc. Все права защищены.
e · lec · trode
(ē-lek’trōd),1. Устройство для записи одного из двух концов электрической цепи; один из двух полюсов электрической батареи или присоединенного к ней конца проводов.
2. Электрический терминал, предназначенный для определенной электрохимической реакции.
[электро- + G. ходов, путей]
Farlex Partner Medical Dictionary © Farlex 2012
электрод
Стимуляция сердца Часть электрического проводника, через который ток входит или выходит; неизолированная проводящая часть электрокардиостимулятора или корпус имплантируемого униполярного генератора импульсов, обеспечивающий электрический контакт с тканью; электроды используются для регистрации электрической активности сокращающихся мышц; электромиографические данные собираются с помощью поверхностных электродов, тонкопроволочных и игольчатых электродов. См. Кольцевой электрод, Электрод SilverBullet ™ , Наконечник электрода.
См. Кольцевой электрод, Электрод SilverBullet ™ , Наконечник электрода.Краткий словарь современной медицины МакГроу-Хилла. © 2002 McGraw-Hill Companies, Inc.
e · lec · trode
(ĕ-lek’trōd)1. Устройство для записи одного из двух концов электрической цепи; один из двух полюсов электрической батареи или присоединенного к ней конца проводов.
2. Электрический терминал, предназначенный для определенной электрохимической реакции.
[ electro- + G. hodos, way]
Медицинский словарь для медицинских работников и медсестер © Farlex 2012
Электрод
Среда для проведения электрического тока — в данном случае платиновые провода.
Медицинская энциклопедия Гейла. Copyright 2008 The Gale Group, Inc. Все права защищены.
e · lec · trode
(ĕ-lek’trōd) Устройство для записи одного из двух концов электрической цепи; один из двух полюсов электрической батареи или присоединенного к ней конца проводов.
[ electro- + G. hodos, way]
Медицинский словарь для стоматологов © Farlex 2012
Плюс или минус — идиомы от The Free Dictionary
«Гораздо проще и гораздо вероятнее поверить, что моя смерть необходима — смерть незначительного атома — для того, чтобы выполнить общую гармонию вселенной — чтобы сделать хоть какой-то плюс или минус в В третьем квартале мы ожидаем, что выручка составит примерно 324 млн долларов США, плюс-минус 2%, что в середине представляет собой еще один квартальный рекорд и продолжающийся рост по сравнению с прошлым годом, а также дальнейшее опережение наших обслуживали рынки.Окрашивание туннеля выявило 16,4 (плюс-минус 0,6424) апоптотических клеток на поле высокой мощности в 5-секундном эксперименте криохирургии и 20,6 (плюс-минус 0,6424) в 10-секундной процедуре. Независимо от того, идет ли война с лекарствами, плюс или минус, Компания Intel Corporation (Nasdaq: INTC) объявила в четверг, что ожидает, что выручка во втором квартале составит 13,7 млрд долларов США, плюс-минус 300 млн долларов США, по сравнению с предыдущим диапазоном в 13,0 млрд долларов США, плюс-минус 500 млн долларов США. Инструктор, который выставлял по крайней мере одну оценку плюс или минус за курс каждый раз, когда он преподавался в период с 2006 по 2012 год, был классифицирован как Чейнджер для этого курса.- В среднем фракция выброса левого желудочка (ФВЛЖ) была значительно увеличена по сравнению с исходным уровнем в группе C-Cure по сравнению с контрольной группой (5,2 плюс-минус 0,6 процента по сравнению с I плюс-минус 0,7 процента, p !!!! 0,01), что означает на 18,1 плюс-минус 2,3 процента относительного увеличения систолической функции, обеспечиваемого клеточной терапией. — В среднем фракция выброса левого желудочка (ФВЛЖ) была значительно увеличена по сравнению с исходным уровнем в группе C-Cure по сравнению с контрольной группой (5,2 плюс-минус 0,6 процента). против 1 плюс-минус 0.7 процентов, p !!! 0,01), что соответствует относительному увеличению систолической функции на 18,1 плюс-минус 2,3 процента, обеспечиваемому клеточной терапией. Производитель кремниевых чипов Intel Corporation (Nasdaq: INTC) в пятницу заявила, что теперь ожидает доходов от третьего за квартал составит 9,0 млрд долларов США, плюс-минус 200 млн долларов США, по сравнению с предыдущими ожиданиями в 8,5 млрд долларов США, плюс-минус 400 млн долларов США.
Инструктор, который выставлял по крайней мере одну оценку плюс или минус за курс каждый раз, когда он преподавался в период с 2006 по 2012 год, был классифицирован как Чейнджер для этого курса.- В среднем фракция выброса левого желудочка (ФВЛЖ) была значительно увеличена по сравнению с исходным уровнем в группе C-Cure по сравнению с контрольной группой (5,2 плюс-минус 0,6 процента по сравнению с I плюс-минус 0,7 процента, p !!!! 0,01), что означает на 18,1 плюс-минус 2,3 процента относительного увеличения систолической функции, обеспечиваемого клеточной терапией. — В среднем фракция выброса левого желудочка (ФВЛЖ) была значительно увеличена по сравнению с исходным уровнем в группе C-Cure по сравнению с контрольной группой (5,2 плюс-минус 0,6 процента). против 1 плюс-минус 0.7 процентов, p !!! 0,01), что соответствует относительному увеличению систолической функции на 18,1 плюс-минус 2,3 процента, обеспечиваемому клеточной терапией. Производитель кремниевых чипов Intel Corporation (Nasdaq: INTC) в пятницу заявила, что теперь ожидает доходов от третьего за квартал составит 9,0 млрд долларов США, плюс-минус 200 млн долларов США, по сравнению с предыдущими ожиданиями в 8,5 млрд долларов США, плюс-минус 400 млн долларов США. Средний ИМТ для всех респондентов составил 25,24 плюс-минус 5,56. В случае испытания натощак среднее время до утомления составило 109 плюс-минус 12 минут.Основная антенна Хаббла, или антенны с высоким коэффициентом усиления, предназначены для поворота на угол плюс-минус 93 [градуса] в каждом из двух направлений поворота. Кех-Шью Лу прокомментировал: «Мы ожидаем выручку в первом квартале 2019 года. составляет примерно 305 миллионов долларов, плюс-минус 2,5 процента. Опрос, в котором использовались очные интервью с 1800 филиппинцами, имел погрешность плюс-минус 2 процентных пункта.
Средний ИМТ для всех респондентов составил 25,24 плюс-минус 5,56. В случае испытания натощак среднее время до утомления составило 109 плюс-минус 12 минут.Основная антенна Хаббла, или антенны с высоким коэффициентом усиления, предназначены для поворота на угол плюс-минус 93 [градуса] в каждом из двух направлений поворота. Кех-Шью Лу прокомментировал: «Мы ожидаем выручку в первом квартале 2019 года. составляет примерно 305 миллионов долларов, плюс-минус 2,5 процента. Опрос, в котором использовались очные интервью с 1800 филиппинцами, имел погрешность плюс-минус 2 процентных пункта.PPT — Anode PowerPoint Presentation, скачать бесплатно
Основные концепции электрохимических ячеек Электрификация! Анод Катод
ХИМИЧЕСКИЕ ИЗМЕНЕНИЯ —> ЭЛЕКТРИЧЕСКИЙ ТОК Со временем медные пластинки на металлической полосе Zn, и полоса Zn «исчезает.”• Zn окисляется и является восстановителем Zn (s) —> Zn2 + (водн. ) + 2e- • Cu2 + восстанавливается и является окислителем Cu2 + (водн.) + 2e- —> Cu (s)
) + 2e- • Cu2 + восстанавливается и является окислителем Cu2 + (водн.) + 2e- —> Cu (s)
Электроны переходят от Zn к Cu2 +, но полезный электрический ток отсутствует. ХИМИЧЕСКИЕ ИЗМЕНЕНИЯ —> ЭЛЕКТРИЧЕСКИЙ ТОК Окисление: Zn (s) —> Zn2 + (водн.) + 2e- Восстановление: Cu2 + (водн.) + 2e- —> Cu (s) ——— ———————————————— Cu2 + ( aq) + Zn (s) —> Zn2 + (aq) + Cu (s)
ХИМИЧЕСКОЕ ИЗМЕНЕНИЕ —> ЭЛЕКТРИЧЕСКИЙ ТОК • Чтобы получить полезный ток, мы разделяем окислитель и восстановитель таким образом, чтобы перенос электронов происходит через внешний провод.Это выполняется в ГАЛЬВАНИЧЕСКОЙ или НАПРЯЖЕННОЙ ячейке. Группа таких ячеек называется аккумулятором.
Zn -> Zn2 + + 2e- Cu2 + + 2e- -> Окисляющий анод отрицательный восстановительный катод положительный • Электроны проходят через внешний провод. • Солевой мостик позволяет анионам и катионам перемещаться между отсеками электродов. <- Анионы Катионы ->
Ячейка Cu | Cu2 + и Ag | Ag + Электроны движутся от анода к катоду в проводе. Анионы и катионы перемещаются через солевой мостик.
Анод, место окисления, отрицательный Катод, место восстановления, положительный
1,10 В 1,0 M 1,0 M ПОТЕНЦИАЛ ЯЧЕЙКИ, E • Электроны «перемещаются» от анода к катоду под действием электродвижущей силы или ЭДС. • Для ячейки Zn / Cu это указывается напряжением 1,10 В при 25 ˚C и когда [Zn2 +] и [Cu2 +] = 1,0 М. Zn и Zn2 +, анод Cu и Cu2 +, катод
ПОТЕНЦИАЛ ЯЧЕЙКИ , E • Для ячейки Zn / Cu потенциал равен +1.10 В при 25 ˚C и когда [Zn2 +] и [Cu2 +] = 1,0 М. • Это СТАНДАРТНЫЙ ПОТЕНЦИАЛ ЯЧЕЙКИ, Eo • — количественная мера тенденции реагентов переходить в продукты, когда все они находятся в своих стандартных состояниях при 25 ˚C. • Имеются в виду чистые твердые вещества или раствор с концентрацией 1M !!!!
Расчет напряжения ячейки • Сбалансированные полуреакции можно сложить вместе, чтобы получить общее сбалансированное уравнение. Zn (s) —> Zn2 + (водн.) + 2e- Cu2 + (aq) + 2e- —> Cu (s) ——————— ———————— Cu2 + (водн.) + Zn (s) —> Zn2 + (водн.) + Cu (s) • Если мы знаем Eo для каждой полуреакции, мы можем получить Eo для чистой реакции.• Давайте вернемся к моему хайку!
Zn (s) —> Zn2 + (водн.) + 2e- Cu2 + (aq) + 2e- —> Cu (s) ——————— ———————— Cu2 + (водн.) + Zn (s) —> Zn2 + (водн.) + Cu (s) • Если мы знаем Eo для каждой полуреакции, мы можем получить Eo для чистой реакции.• Давайте вернемся к моему хайку!
Окисление Haiku! • Потеряли электрон • Но теперь чувствую себя позитивно • Окисленный — это круто! • Что это? Хотите сокращение Haiku?
Уменьшение Haiku !!! • Получил несколько электронов • Поднял настроение! • Теперь я могу сказать Гер! • Спасибо … Наслаждайтесь буфетом … Не ешьте детскую химикат или мебель!
КЛЕТОЧНЫЙ ПОТЕНЦИАЛ, Eo Невозможно напрямую измерить 1/2 реакции Eo.Поэтому измеряйте его относительно СТАНДАРТНОЙ ВОДОРОДНОЙ ЯЧЕЙКИ, SHE. 2 H + (вод., 1 M) + 2e- <----> h3 (g, 1 атм) Eo = 0,0 В
Отрицательный электрод Положительный электрод Zn / Zn2 + полуэлемент, прикрепленный к SHE. Eo для ячейки = +0,76 В Поставщик электронов Приемник электронов Zn -> Zn2 + + 2e- Окислительный анод 2 H + + 2e- -> h3 Восстановительный катод
Eo для ячейки = +0,76 В Поставщик электронов Приемник электронов Zn -> Zn2 + + 2e- Окислительный анод 2 H + + 2e- -> h3 Восстановительный катод
Восстановление H + Zn Рисунок 20.10
Общая реакция — восстановление H + металлическим Zn. Zn (s) + 2 H + (aq) -> Zn2 + + h3 (g) Eo = +0,76 В Следовательно, Eo для Zn —> Zn2 + (aq) + 2e- равно +0,76 В Zn является (лучше ) (более бедный) восстановитель, чем h3.
Cu / Cu2 + и h3 / H + Ячейка Eo = +0,34 В Положительный Отрицательный Акцептор электронов Поставщик электронов Cu2 + + 2e- -> Восстановительный катод Cu h3 -> 2 H + + 2e- Окисляющий анод
Ячейка Cu / Cu2 + и h3 / H + Общая реакция — восстановление Cu2 + газом h3. Cu2 + (водн.) + H3 (g) —> Cu (s) + 2 H + (водн.) Измеренное Eo = +0.34 В Следовательно, Eo для Cu2 + + 2e- —> Cu равно +0,34 В
+ Zn / Cu Электрохимическая ячейка Zn (s) —> Zn2 + (водн. ) + 2e- Eo = +0,76 V Cu2 + (водн.) + 2e- —> Cu (s) Eo = +0,34 В —————————— ———————————- Cu2 + (водн.) + Zn (s) —> Zn2 + (водн. ) + Cu (s) Eo (рассчитано) = +1,10 В Анод, отрицательный, источник электронов Катод, положительный, сток для электронов
) + 2e- Eo = +0,76 V Cu2 + (водн.) + 2e- —> Cu (s) Eo = +0,34 В —————————— ———————————- Cu2 + (водн.) + Zn (s) —> Zn2 + (водн. ) + Cu (s) Eo (рассчитано) = +1,10 В Анод, отрицательный, источник электронов Катод, положительный, сток для электронов
Да. Наконец-то настало время для ДЕМО !! • Вы хотите преодолеть эту соль?
окислительная o способность иона E (V) 2+ Cu + 2e- Cu +0.34 + 2 H + 2e- H 0,00 2+ Zn + 2e- Zn -0,76 восстанавливающая способность элемента ТАБЛИЦА СТАНДАРТНЫХ ПОТЕНЦИАЛОВ СНИЖЕНИЯ 2
Потенциальная лестница для полуреакций восстановления Рисунок 20.11
Таблица 21.1 Страница 970
2+ Cu + 2e- Cu +0,34 + 2 H + 2e- H 0,00 2 2+ Zn + 2e- Zn -0,76 Стандартный окислительно-восстановительный потенциал, Eo Любое вещество справа восстанавливает любое вещество выше, чем слева. Правило северо-запада-юго-востока: реакции в пользу продукта происходят между восстановителем в юго-восточном углу (анод) и окислителем в северо-западном углу (катод).
Правило северо-запада-юго-востока: реакции в пользу продукта происходят между восстановителем в юго-восточном углу (анод) и окислителем в северо-западном углу (катод).
Стандартные окислительно-восстановительные потенциалы, Eo Любое вещество справа восстанавливает любое вещество выше, чем оно слева. • Zn может восстанавливать H + и Cu2 +. • h3 может восстанавливать Cu2 +, но не Zn2 + • Cu не может восстанавливать H + или Zn2 +.
Использование стандартных потенциалов, EoTable 20.1 • В каком направлении идут следующие реакции? • Cu (s) + 2 Ag + (водный раствор) —> Cu2 + (водный раствор) + 2 Ag (s) • 2 Fe2 + (водный раствор) + Sn2 + (водный раствор) —> 2 Fe3 + (водный раствор) + Sn (s) • Что такое Eonet для общей реакции?
Стандартные окислительно-восстановительные потенциалы, Eo E˚net = «расстояние» от «верхней» полуреакции (катод) до «нижней» полуреакции (анод) E˚net = E˚cathode — E˚anode Eonet для реакции Cu / Ag + = +0. 46 В
Eo для гальванического элемента Cd -> Cd2 + + 2e- или Cd2 + + 2e- -> Cd Fe -> Fe2 + + 2e- или Fe2 + + 2e- -> Fe Все ингредиенты являются подарок. В каком направлении идет реакция?
Eo для гальванического элемента Из таблицы видно: • Fe — лучший восстановитель, чем Cd • Cd2 + — лучший окислитель, чем Fe2 + Общая реакция Fe + Cd2 + —> Cd + Fe2 + Eo = E ˚катод — E˚анод = (-0,40 В) — (-0,44 В) = +0.04 В
Подробнее о расчете напряжения элемента 2 h3O + 2e- —> h3 + 2 OH- Катод 2 I —-> I2 + 2e- Анод ———- ————————————— 2 I- + 2 h3O -> I2 + 2 OH- + h3 Предположим, ион I- может восстанавливать воду. Предполагая, что реакция происходит, как написано, E˚net = E˚cathode — E˚anode = (-0,828 В) — (+0,535 В) = -1,363 В Минус E˚ означает rxn. происходит в обратном направлении
Если вы зашли так далеко, вам нужна пауза!
Вычитание положительных и отрицательных чисел
Вычесть положительные числа, такие как 4–2, несложно.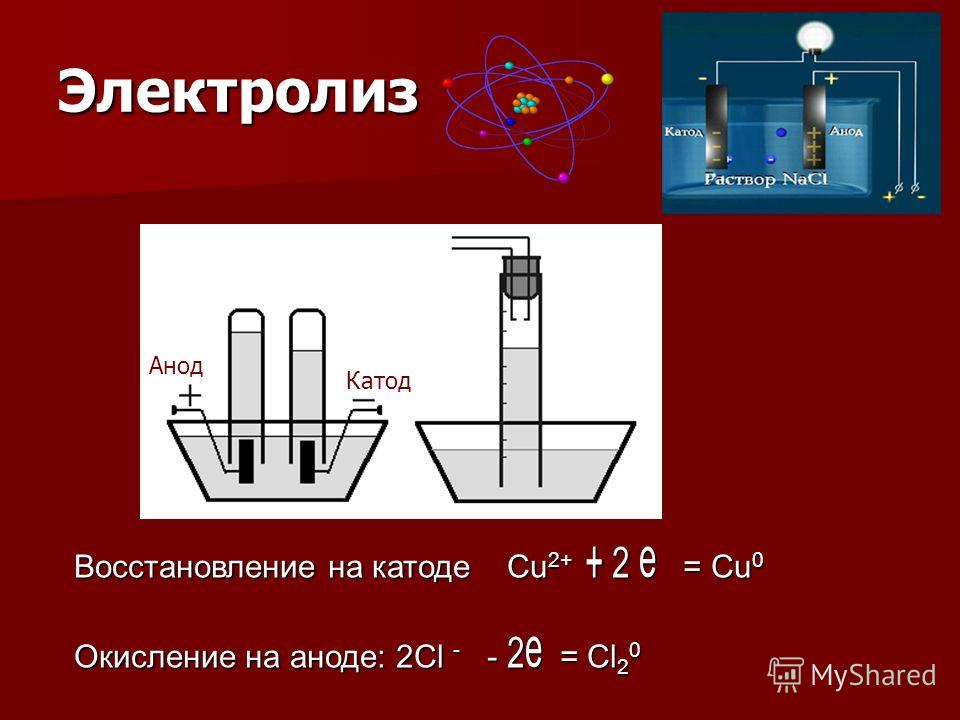 Когда мы вычитаем отрицательные числа или вычитаем отрицательные числа из положительных, все становится сложнее.
Когда мы вычитаем отрицательные числа или вычитаем отрицательные числа из положительных, все становится сложнее.
Вот несколько простых правил, которым нужно следовать при вычитании отрицательных чисел.
Правило 1. Вычитание положительного числа из положительного — это обычное вычитание.
Например: это то, что вы узнали раньше. 6-3 — два положительных числа. Решите это уравнение, как всегда: 6 — 3 = 3.
Правило 2: Вычитание положительного числа из отрицательного числа — начните с отрицательного числа и считайте в обратном порядке.
Например: Допустим, у нас есть задача -2 — 3. Используя числовую линию, давайте начнем с -2.
Теперь сосчитайте назад на 3 единицы. Так что продолжайте отсчитывать три пробела от -2 в числовой строке.
Ответ: -2 — 3 = -5.
Правило 3: вычитание отрицательного числа из отрицательного числа — знак минус, за которым следует отрицательный знак, превращает два знака в знак плюс.
Итак, вместо вычитания отрицательного числа вы добавляете положительное.Обычно — (-4) становится +4, а затем вы складываете числа.
Например, у нас есть проблема -2 — –4. Это будет читать «два отрицательных минус 4 отрицательных». Итак, мы меняем два отрицательных знака на положительные, и теперь уравнение принимает вид -2 + 4.
На числовой строке он начинается с -2.
Затем продвигаемся на 4 единицы: +4.
Ответ -2 — (-4) = 2.
Правило 4: Вычитание отрицательного числа из положительного — превратите знак вычитания, за которым следует отрицательный знак, в знак плюс.
Итак, вместо того, чтобы вычитать отрицательное, вы добавляете положительное. Таким образом, уравнение превращается в простую задачу сложения.
Например: допустим, у нас есть проблема 2 — (-3).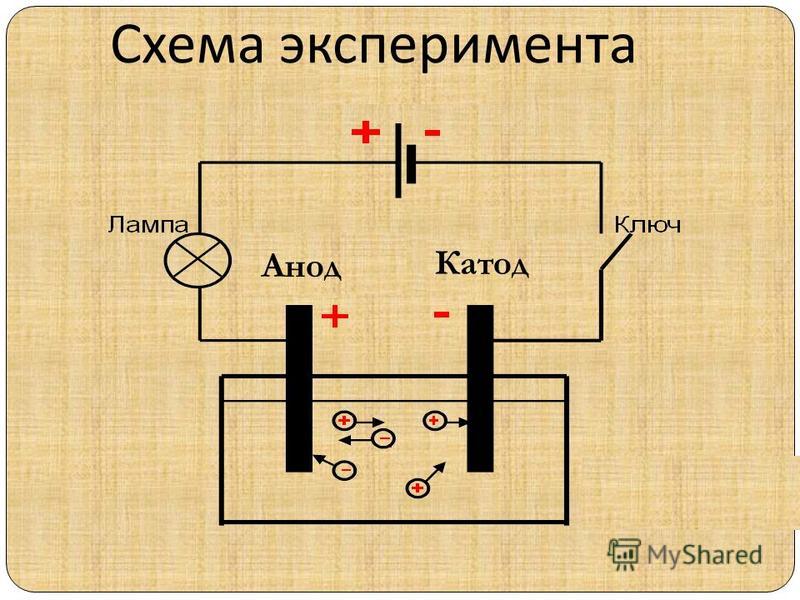 Это читается как «два минус три минус». — (-3) превращается в +3.
Это читается как «два минус три минус». — (-3) превращается в +3.
На числовой строке мы начинаем с 2.
Затем продвигаемся на три части: 2 + 3.
Ответ 2 — (-3) = 5.
Анод— Викисловарь
Английский [править]
Этимология [править]
От древнегреческого ἀνα- (ана, «вверх») и ὁδός (ходос, «путь»), образуя новогреческое соединение ἄνοδος (ánodos). Создан английским эрудитом Уильямом Уэвеллом в 1834 году для Майкла Фарадея, который представил его позже в том же году.
Произношение [править]
Существительное [править]
анод ( несколько анодов )
- (электричество) Электрод элемента или другого электрически поляризованного устройства, через который положительный электрический ток течет внутрь (и, таким образом, электроны текут наружу).
 Он может иметь как отрицательное, так и положительное напряжение.
Он может иметь как отрицательное, так и положительное напряжение. - (химия, в широком смысле) Электрод, на котором происходит химическое окисление анионов, обычно приводящее к эрозии металла с электрода.
- (электроника) Электрод, который собирает электроны, испускаемые катодом в вакуумной трубке или газонаполненной трубке.
- (электроника) Электрод полупроводникового прибора, который соединен с материалом p-типа p-n-перехода.
Условия координат [править]
Производные термины [править]
Переводы [править]
электрод электрохимической ячейки, на котором происходит окисление
электрод, через который ток течет в ячейку
- Приведенные ниже переводы необходимо проверить и вставить выше в соответствующие таблицы переводов, удалив все цифры.Числа не обязательно совпадают с числами в определениях. См. Инструкции в Викисловаре: Макет статьи § Переводы.
Проверяемые переводы
Анаграммы [править]
Этимология [править]
Заимствовано с английского анод .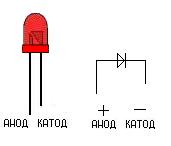
Произношение [править]
- IPA (ключ) : /ˌaːˈnoː.də/
- Расстановка переносов: ano‧de
- Рифмы: -oːdə
Существительное [править]
анод f ( множественное число анод или анод , миниатюрный анод n )
- (электричество) анод
Антонимы [править]
Этимология [править]
Заимствовано с английского анод .
Существительное [править]
анод f ( множественное число анодов )
- анод (электрод, через который ток течет в устройство или ячейку)
Дополнительная литература [редактировать]
Что такое унарный плюс / минус в R?
Переполнение стека- Около
- Продукты
- Для команд
- Переполнение стека Общественные вопросы и ответы
- Переполнение стека для команд Где разработчики и технологи делятся частными знаниями с коллегами
- Вакансии Программирование и связанные с ним технические возможности карьерного роста
- Талант Нанимайте технических специалистов и создавайте свой бренд работодателя
- Реклама Обратитесь к разработчикам и технологам со всего мира
- О компании