Катод и анод это плюс или минус
Последний раз редактировалось sashatgu Здравствуйте, помогите пожалуйста разобраться в том что такое анод и катод, где они находятся с внешней стороны пальчиковой батарейки и какие знаки имеют, а также где они находятся внутри пальчиковой батарейки и какие знаки имеют. Также где катод и анод у светодиода и какие знаки имеют? Я ничего не могу понять даже на уровне пальчиковой батарейки.
Поиск данных по Вашему запросу:
Схемы, справочники, даташиты:
Прайс-листы, цены:
Обсуждения, статьи, мануалы:
Дождитесь окончания поиска во всех базах.
По завершению появится ссылка для доступа к найденным материалам.
Содержание:
- Где у светодиода плюс и минус
- Научный форум dxdy
- Электронный анод.
Назначение диода. Определяем полярность светодиода. Где плюс и минус у LED
- Катод и анод
- Что такое анод и катод?
- Все методы определения полярности у светодиодов
- Анод и катод
- Что такое анод и катод — простое объяснение
- Анод и катод — что это и как правильно определить? Анод и катод на схеме диода
- Что такое анод и катод — простое объяснение
ПОСМОТРИТЕ ВИДЕО ПО ТЕМЕ: Катод
Где у светодиода плюс и минус
Часто возникает проблема определения, какой из электродов является катодом, а какой — анодом. Для начала нужно разобраться с терминами. В сложных веществах электроны между атомами в соединениях распределены неодинаково.
Для начала нужно разобраться с терминами. В сложных веществах электроны между атомами в соединениях распределены неодинаково.
В результате взаимодействия частицы перемещаются от атома одного вещества к атому другого. Реакция именуется окислительно-восстановительной. Потеря электронов называется окислением, элемент, отдающий электроны — восстановителем. Присоединение электронов носит название восстановление, принимающий элемент в этом процессе — окислитель. Переход электронов от восстановителя к окислителю может протекать по внешней цепи, и тогда его можно использовать в качестве источника электрической энергии.
Устройства, в которых энергия химической реакции превращается в электрическую энергию, называются гальваническими элементами.
 Электрод, на котором протекает восстановление — катодом.
Электрод, на котором протекает восстановление — катодом.Из школьных учебников химии известен пример медно-цинкового гальванического элемента, работающего за счет энергии реакции между цинком и сульфатом меди. В устройстве Якоби — Даниэля пластина из меди помещена в раствор сульфата меди медный электрод , цинковая пластина погружена в раствор сульфата цинка цинковый электрод.
Цинковый электрод отдает катионы в раствор, создавая в нем избыточный положительный заряд, а у медного электрода раствор обедняется катионами, здесь раствор заряжен отрицательно. Замыкание внешней цепи заставляет электроны перетекать от цинкового электрода к медному. Равновесные отношения на границах фаз прерываются. Идёт окислительно-восстановительная реакция. Если химическую реакцию провоцирует внешняя энергия электрического тока, идёт процесс, называемый электролизом. Процессы, протекающие при электролизе, обратны процессам, протекающим при работе гальванического элемента.
Электрод, на котором происходит восстановление, также называется катодом, но при электролизе он заряжен отрицательно, а анод — положительно.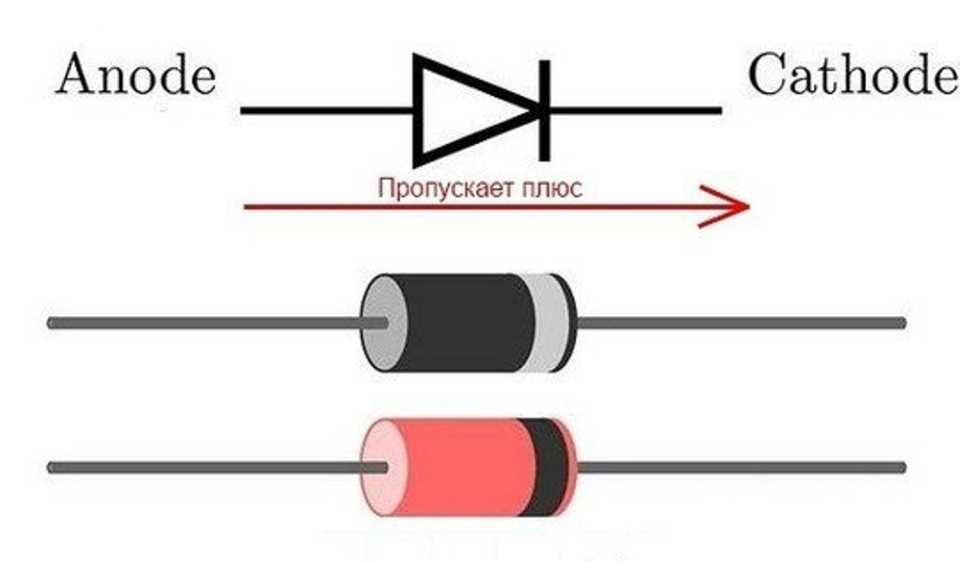 Электролизом расплавленных соединений и водных растворов получают металлы, производят очистку металлов от примесей и извлечение ценных компонентов электролитическое рафинирование. Из металла, подлежащего очистке, отливают пластины.
Электролизом расплавленных соединений и водных растворов получают металлы, производят очистку металлов от примесей и извлечение ценных компонентов электролитическое рафинирование. Из металла, подлежащего очистке, отливают пластины.
Они помещаются в качестве анодов в электролизер. Под воздействием электрического тока металл подвергается растворению. Его катионы переходят в раствор и разряжаются на катоде, образуя осадок чистого металла.
Примеси, содержащиеся в первоначальной неочищенной металлической пластине, либо остаются нерастворимыми в виде анодного шлама, либо переходят в электролите, откуда удаляются. Электролитическому рафинированию подвергают медь, никель, свинец, золото, серебро, олово. Электроэкстракция — процесс выделения металла из раствора в ходе электролиза.
Для того чтобы металл перешёл в раствор, его обрабатывают специальными реагентами. В ходе процесса на катоде происходит выделение металла, характеризующегося высокой чистотой. Так получают цинк, медь, кадмий. Чтобы избежать коррозии, придать прочность, украсить изделие поверхность одного металла покрывают слоем другого. Этот процесс называется гальваностегией. Гальванопластика — процесс получения металлических копий с объёмных предметов электроосаждением металла.
Чтобы избежать коррозии, придать прочность, украсить изделие поверхность одного металла покрывают слоем другого. Этот процесс называется гальваностегией. Гальванопластика — процесс получения металлических копий с объёмных предметов электроосаждением металла.
Принцип действия катода и анода в вакуумном приборе может продемонстрировать электронная лампа. Она выглядит как герметически запаянный сосуд с металлическими деталями внутри.
Прибор используется для выпрямления, генерирования и преобразования электрических сигналов. По числу электродов выделяют:. Диод — вакуумный прибор с двумя электродами, катодом и анодом.
Катод подключен к отрицательному полюсу источника питания, анод — к положительному. Предназначение катода — испускать электроны под действием нагрева электрическим током до определенной температуры.
Посредством испущенных электронов создается пространственный заряд между катодом и анодом. Самые быстрые электроны устремляются к аноду, преодолевая отрицательный потенциальный барьер объемного заряда.
Анод принимает эти частицы. Создается анодный ток во внешней цепи. Электронным потоком управляют с помощью дополнительных электродов, подавая на них электрический потенциал. Посредством диодов переменный ток преобразуется в постоянный. В электронике широко используется свойство диодов пропускать ток в прямом направлении и не пропускать в обратном. Работа светодиода основана на свойстве кристаллов полупроводников светиться при пропускании через p-n переход тока в прямом направлении.
Химические источники электрического тока, в которых протекают обратимые реакции, называются аккумуляторами: их перезаряжают и используют многократно.
При работе свинцового аккумулятора происходит окислительно-восстановительная реакция. Металлический свинец окисляется, отдает свои электроны, восстанавливая диоксид свинца, принимающего электроны.
Металлический свинец в аккумуляторе — анод, он заряжен отрицательно. Диоксид свинца — катод и заряжен положительно. По мере разряда аккумулятора расходуются вещества катода и анода и их электролита, серной кислоты.
В аккумуляторе вновь создаются вещества, необходимые для его работы. Проблема возникает из-за того, что определенный знак заряда не может быть прочно закреплен за анодом или катодом. Часто катодом является положительно заряженный электрод, а анодом — отрицательный. Часто, но не всегда. Все зависит от процесса, протекающего на электроде. Деталь, которую поместили в электролит, может быть и анодом и катодом. Все зависит от цели процесса: нужно нанести на нее другой слой металла или снять его.
В электрохимии анод — это электрод, на котором идут процессы окисления, катод — это электрод, где происходит восстановление. У диода отводы называются анод и катод. У нового светодиода с необрезанными контактами анод и катод определяются визуально по длине.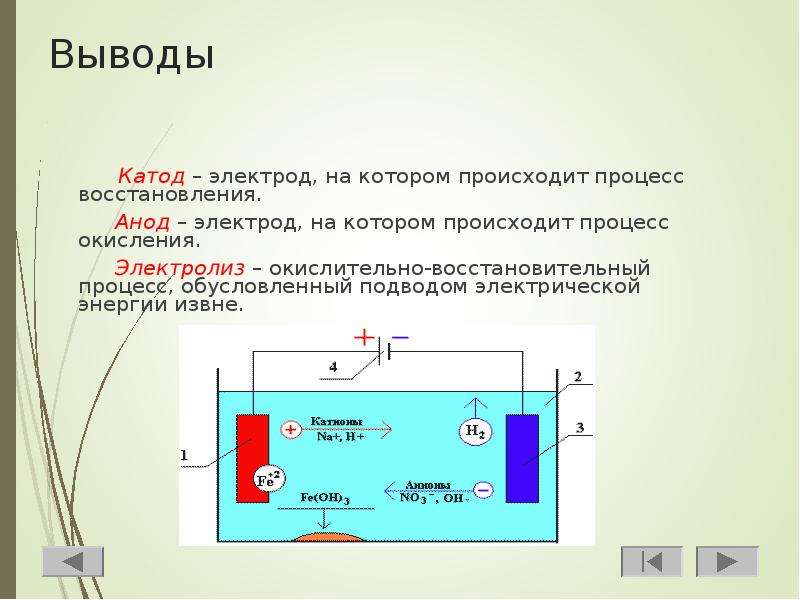
Если контакты обрезаны, поможет батарейка, приложенная к ним. Свет появится, когда полярности совпадут. В электрохимии речь правильнее вести не о знаках зарядов электродов, а о процессах, на них идущих. На катоде проходит реакция восстановления, на аноде — окисления. В электротехнике для протекания тока катод подключают к отрицательному полюсу источника тока, анод — к положительному.
Содержание 1 Понятие катода и анода — простое объяснение 2 Применение в электрохимии 2. Термометр сопротивления — датчик для измерения температуры: что это такое, описание и виды. Что такое электроконтактный манометр, назначение, принцип работы, схема подключения и обзор популярных моделей. Чем отличаются и где используются постоянный и переменный ток. Что такое активная и реактивная мощность переменного электрического тока?
Как установить и настроить спутниковую антенну самостоятельно? Для чего нужен пирометр и как измерять температуру бесконтактным методом. Что такое нихромовая проволока, её свойства и область применения.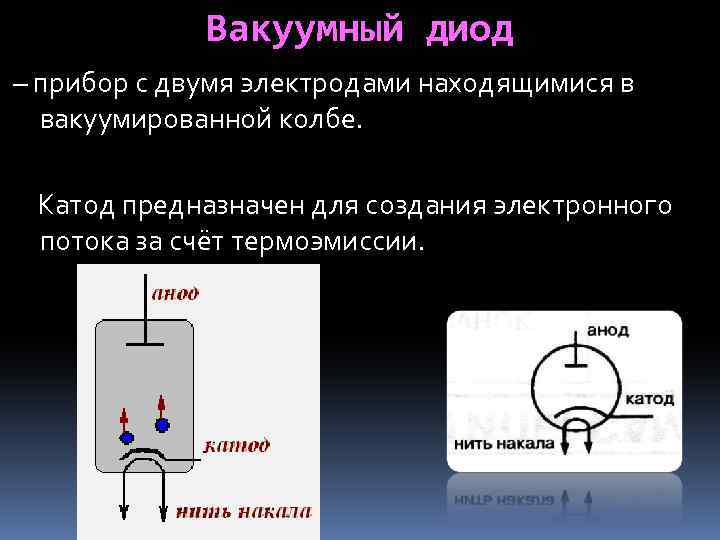
Что такое тензодатчик, типы тензометрических датчиков, схема подключения и их применение.
Научный форум dxdy
Ета такая хренатень, которая употребляется в скопе с другими такого рода хренатенями для достижения результативности в случаи скрещивания этих хренатеней с разными, но уже другими хренатенями Зубы вставь,сквозит. Ноу коментс. Анад, катод элименты ламп То что называют безграмотные меня меньше всего волнует Проблема толерантности имеет значение при пересадке органов и тканей 2 ] Способность организма переносить неблагоприятное влияние того или иного фактора среды это из википедии
Анод — это плюс (по четыре буквы в каждом слове). Катод — это минус (по пять букв в каждом слове). У анода анионы окисляются (все слова.
Электронный анод. Назначение диода. Определяем полярность светодиода. Где плюс и минус у LED
Изучение таких отраслей, как электрохимия и цветная металлургия, невозможно без понимания в полной мере терминов катод и анод. В то же время эти термины являются неотъемлемой частью вакуумных и полупроводниковых электронных приборов. Под электрохимией следует понимать раздел физической химии, изучающий химические процессы, вызываемые воздействием электрического тока, а также электрические явления, вызываемые химическими процессами. Существует два основных вида электрохимических операций:. Под процессами окисления стоит понимать процедуру, при которой частица отдает электроны. Восстановительный процесс подразумевает процедуру принятия электронов частицей. Цветная металлургия широко использует процесс электролиза для выделения металлов из добытых руд и дальнейшей очистки.
Под электрохимией следует понимать раздел физической химии, изучающий химические процессы, вызываемые воздействием электрического тока, а также электрические явления, вызываемые химическими процессами. Существует два основных вида электрохимических операций:. Под процессами окисления стоит понимать процедуру, при которой частица отдает электроны. Восстановительный процесс подразумевает процедуру принятия электронов частицей. Цветная металлургия широко использует процесс электролиза для выделения металлов из добытых руд и дальнейшей очистки.
Катод и анод
Часто возникает проблема определения, какой из электродов является катодом, а какой — анодом. Для начала нужно разобраться с терминами. В сложных веществах электроны между атомами в соединениях распределены неодинаково. В результате взаимодействия частицы перемещаются от атома одного вещества к атому другого. Реакция именуется окислительно-восстановительной.
Вспомните, как вы накачивали колесо велосипеда или автомобиля.
Что такое анод и катод?
Назначение диода — проводить электрический ток только в одном направлении. Когда-то давно применялись ламповые диоды. Но сейчас используются в основном полупроводниковые диоды. В отличие от ламповых они значительно меньше по размеру, не требуют цепей накала и их очень просто соединять различным образом. На рисунке показано условное обозначение диода на схеме.
Все методы определения полярности у светодиодов
Это возникает от того, что новое понятие не может однозначно зацепиться за уже известные факты в сознании, никак не получается построить новую связь в семантической сети фактов. Все знают, что у диода есть катод и анод. Все знают, как диод обозначается на электрической схеме. Но далеко не все могут правильно сказать, где же на схеме что. Под спойлером картинка, посмотрев на которую, вы навсегда запомните, где у диода анод, а где катод. Должен предупредить, развидеть это не получится, так что тот, кто не уверен в себе, пусть не открывает. Теперь, когда мы отпугнули слабых, продолжаем Да, вот так все просто.
Теперь, когда мы отпугнули слабых, продолжаем Да, вот так все просто.
Анод — это плюс (по четыре буквы в каждом слове). Катод — это минус (по пять букв в каждом слове). У анода анионы окисляются (все слова.
Анод и катод
Известно, что светодиод в рабочем состоянии пропускает ток только в одном направлении. Если его подключить инверсионно, то постоянный ток через цепь не пройдет, и прибор не засветится. Происходит это потому, что по своей сущности прибор является диодом, просто не каждый диод способен светиться. Получается, что существует полярность светодиода, то есть он чувствует направление движения тока и работает только при определенном его направлении.
Что такое анод и катод — простое объяснение
ВИДЕО ПО ТЕМЕ: Расчет резистора для светодиода
Анод др. Катод от греч. В технике: Электрод полупроводникового прибора диода, тиристора , подключенный к отрицательному полюсу источника тока, когда прибор открыт то есть имеет маленькое сопротивление , называют катодом, подключённый к положительному полюсу — анодом. В электрохимии: Катод — электрод, на котором происходят реакции восстановления, анод — электрод, на котором происходят окислительно-восстановительные реакции окисление. Термины и определения. Примечание — Анод — отрицательный электрод во время разряда и положительный во время заряда.
В электрохимии: Катод — электрод, на котором происходят реакции восстановления, анод — электрод, на котором происходят окислительно-восстановительные реакции окисление. Термины и определения. Примечание — Анод — отрицательный электрод во время разряда и положительный во время заряда.
Оставьте комментарий 6,
Анод и катод — что это и как правильно определить? Анод и катод на схеме диода
Чтобы создавать эффективные электронные схемы с диодами, требуется минимальный объем знаний об их устройстве и принципе работы. Перед началом пайки обязательно необходимо определить, где у этих элементов анод и где катод. Визуального осмотра бывает недостаточно, если электронные элементы приобретены без технической документации или выпаяны из старого оборудования. Для проверки обязательно требуется тестер с различными режимами работы и источник питания с напряжением вольт. Диодами называют электронные элементы, сопротивление которых меняется в зависимости от направления тока. Если ток подается в одну сторону плюс на плюс , он проходит легко диод открыт благодаря низкому сопротивлению.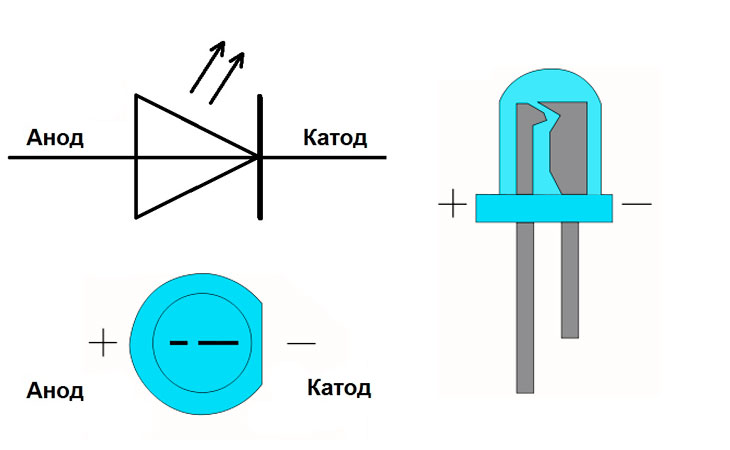
Что такое анод и катод — простое объяснение
Содержание: Электрохимия и гальваника Процесс электролиза или зарядки аккумулятора Гальванотехника В электронике Заключение. Рассмотрим окислительно-восстановительную реакцию в гальваническом элементе, тогда какие процессы протекают на его электродах? Отсюда возникает вопрос — где плюс, а где минус у батарейки? Исходя из определения, у гальванического элемента анод отдаёт электроны.
что это такое, где плюс и где минус на диоде
Классические термины из физики и химии часто встречаются в инструкциях к использованию современных приборов. Необходимо точно знать, что такое определение под собой подразумевает и как его применять к тем или иным конструкциям и явлениям.
Содержание
- Что такое анод и катод
- Анод
- Катод
- Как определить анод и катод
- Сфера применения
- Электрохимия
- Гальванотехника
- Вакуумные и полупроводниковые электроприборы
Что такое анод и катод
Потребитель сталкивается с понятиями анод и катод при зарядке и разрядке аккумулятора, зарядке и обслуживании батареи.
Понять разницу между катодом, анодом, положительным и отрицательным зарядом проще всего, вспомнив некоторые положения из электрохимии.
- Гальванические элементы – электрический ток производится благодаря текущей химической реакции. Именно на этом принципе работают батарейки и аккумуляторы. Поэтому их называют химическими источниками тока.
- Электролиз – химическая реакция, которая протекает за счет включения в систему источника электроэнергии.
В обоих случаях один из электродов несет более высокий потенциал. Этот электрод считается положительным. Электрод с более низким потенциалом и необязательно отрицательным, будет носить название отрицательный. Ток, соответственно, течет от носителя более высокого потенциала к носителю более низкого потенциала.
Да, часто
50.91%
Очень редко
27.27%
Не припоминаю
21.82%
Проголосовало: 55
Анод
По определению анодом выступает электрод, на котором протекает окислительная реакция. Это означает, что электрод служит источником электронов. В химии его же нередко именуют восстановителем.
Это означает, что электрод служит источником электронов. В химии его же нередко именуют восстановителем.
Катод
Под катодом подразумевают электрод, на котором протекает реакция восстановления. Здесь электрод забирает электроны и называется окислителем.
Принимая, что ток является движением положительно заряженных частиц, а не отрицательных, получается, что ток в растворе идет от катода к аноду. В цепи, соединяющей элементы гальванической пары, электроны идут от минуса к плюсу и с этой точки зрения катод является плюсом, а анод – минусом.
Противоречие кажущееся, ведь направление тока определяется движением положительных частиц, хотя фактически в металлической цепи его обеспечивает движение электронов.
Как определить анод и катод
Если с батарейкой все довольно просто (полюс и минус не меняются местами), то с зарядкой аккумулятора дело обстоит сложнее.
Во время зарядки разность между большим и меньшим потенциалом увеличивается, то есть потенциал положительного электрода становится выше, чем его же потенциал в покое – накапливается заряд, а потенциал отрицательного электрода становится меньше, чем он же в состоянии покоя. Отсюда вытекает, что положительный электрод выступает анодом, а отрицательный – катодом.
Отсюда вытекает, что положительный электрод выступает анодом, а отрицательный – катодом.
При использовании устройства потенциал положительного электрода (анода) всегда остается больше, чем потенциал отрицательного (катода). Но во время цикла разрядки/зарядки роль электрода меняется: при разрядке положительным становится катод, отрицательным – анод. Во время зарядки положительным выступает анод, отрицательным – катод.
Если речь идет о растворах и электрофизических реакциях в них, проще запомнить, что катионы – всегда частицы с положительным зарядом, а значит двигаются к минусу. Анионы – частицы всегда с отрицательным зарядом и двигаются к плюсу.
Валера
Голос строительного гуру
Задать вопрос
Чтобы запомнить, где плюс, где минус, используют мнемоническое правило. В словах «катод» и «минус», а также в словах «анод» и «плюс» одинаковое количество букв. В нормальном режиме работы любого электрического прибора ток вытекает из катода и втекает в анод. Даже если речь о металлической жиле, поскольку здесь направление тока определяют не смещении электронов, а смещение дырок.
Даже если речь о металлической жиле, поскольку здесь направление тока определяют не смещении электронов, а смещение дырок.
Сфера применения
В промышленности используют не только собственно гальванические элементы (для получения электрического тока), но и электрохимические реакции, которые протекают под действием тока. Самый известный – получение тонкопослойного защитного покрытия стали – из цинка, алюминия, цинкового-алюминиевых сплавов.
Электрохимия
Электролиз по своему значению противоположен работе гальванического элемента: реакция проходит под действием тока. При этом плюс источника питания все же именуется катодом, а минус анодом, что как бы противоречит вышесказанному. Происходит это потому, что ток от плюсового вывода источника питания уходит на плюсовой вывод аккумулятора и в этом случае последний уже никак не может быть катодом. В результате электроды аккумулятора при зарядке меняются местами, потому что реакция идет в обратном направлении.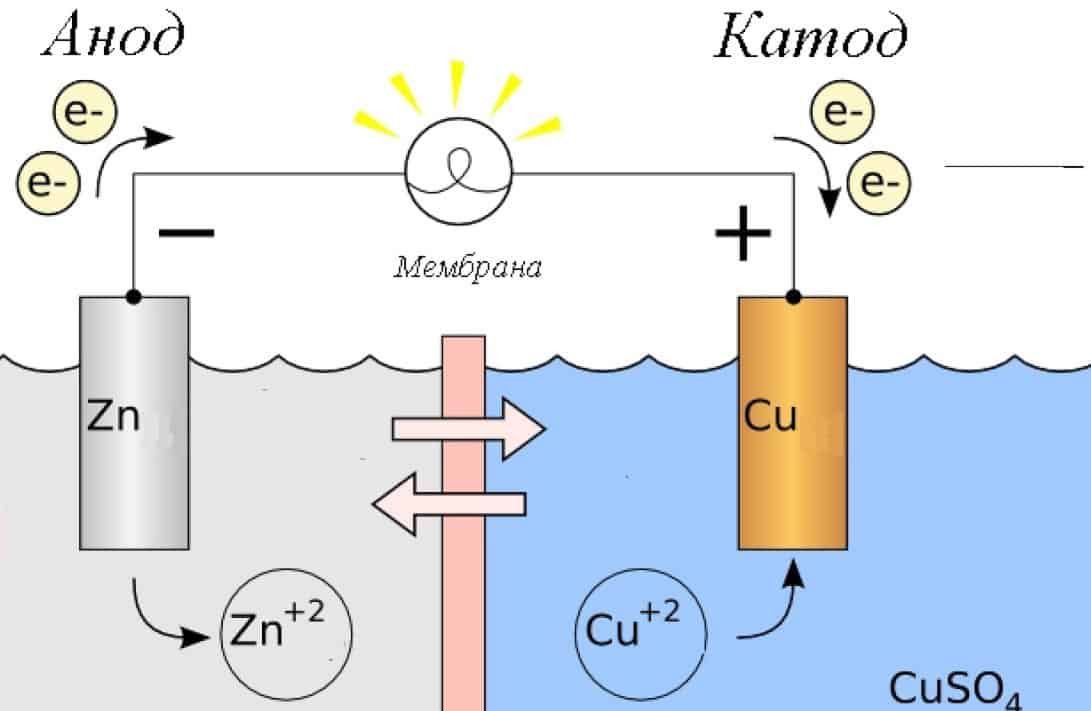
Гальванотехника
Посеребрение, золочение, хромирование, оцинковка – наиболее известные способы использования процесса осаждения вещества. Принцип действия таких установок одинаков: изделие погружают в электролитическую ванную, в которой оно выступает катодом. На его поверхности осаждаются ионы металла – катионы. Чтобы изделие стало катодом, к нему подключают плюсовой вывод источника питания.
Вакуумные и полупроводниковые электроприборы
Понятие катода и анода, а точнее плюса и минуса в вакуумных и полупроводниковых приборах связано с возможностью протекания тока только в одном направлении или в двух. Полупроводник допускает только прямое течение тока, а при наложении напряжения обратного типа ток здесь течет, но крайне незначительно. Для резистора же вопрос не принципиален: он пропускает ток в обоих направлениях.
Катодом и анодом называют выводы диода – ножки. К плюсу батареи подключается анод. Называется он так, потому что у диода в ток любом случае втекает в анод. Светодиод и даже вакуумный подключается точно так же: анод к плюсу, а катод к минусу.
Светодиод и даже вакуумный подключается точно так же: анод к плюсу, а катод к минусу.
У пассивных потребителей катод и анод (плюс и минус) не меняются. У активных, способных пропускать ток в обоих направлениях, разряжаться и заряжаться – плюсы и минус могут меняться. В аккумуляторе катод положительный во время разрядки и отрицательный при зарядке. Для правильного использования приборов и элементов важно помнить одно: у всех потребителей энергии – электронных деталей, электролизеров, гальванических батарей − вывод, подключаемый к плюсу, называется анодом.
Анод против Катода: В чем разница?
Если вам было сегодня много лет, когда вы узнали, что такое анод и катод, вы не одиноки.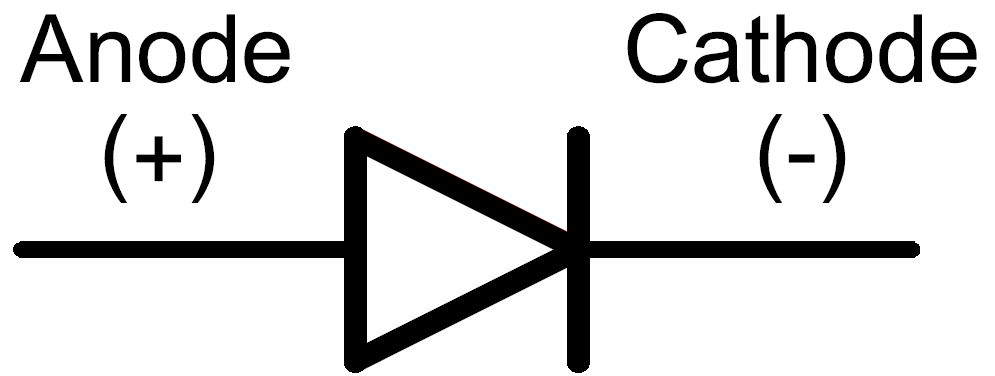 Большинство из нас редко имеют дело с этими терминами, если только мы не ремонтируем водонагреватель или не устанавливаем аккумуляторы для вашего автомобиля или лодки. Так что, если вы ищете статью, в которой разъясняется разница простым языком, не ищите дальше. Здесь мы обсудим, что такое анод, что такое катод, как они оба работают и где они используются.
Большинство из нас редко имеют дело с этими терминами, если только мы не ремонтируем водонагреватель или не устанавливаем аккумуляторы для вашего автомобиля или лодки. Так что, если вы ищете статью, в которой разъясняется разница простым языком, не ищите дальше. Здесь мы обсудим, что такое анод, что такое катод, как они оба работают и где они используются.
Начнем!
Анод и катод в батареях: обзор
Попытка понять, как работают батареи, может показаться изучением другого языка. Ниже мы анализируем компоненты, которые потребуются аккумулятору для зарядки и излучения энергии (в понятной форме).
Анод
Анод — это отрицательный электрод, одна из основных частей батареи. Обычно он сделан из металла, который окисляется и посылает электроны катоду (положительному электроду). Это электрохимическая реакция, в результате которой образуются электроны (то есть электричество).
Материал анода для ионно-литиевых аккумуляторовКак работает анод?
Анод представляет собой окисляющийся металл, такой как цинк или литий, что означает, что он теряет электроны. Он находится в растворителе электролита и медленно разрушается по мере движения электронов по проводнику к катоду.
Он находится в растворителе электролита и медленно разрушается по мере движения электронов по проводнику к катоду.
Проводник (будь то металлическая проволока или трубка) — это то, как мы получаем электричество, вырабатываемое анодом, и, в конечном счете, то, как батарея питает наши устройства. Как только анод полностью разрушается, батарея умирает (или теряет заряд).
Материалы, пригодные для изготовления анодов
Аноды могут изготавливаться из различных материалов. К ним относятся цинк, литий, графит или платина. Хороший анод должен быть эффективным восстановителем, обладать хорошей проводимостью, стабильностью и высоким кулоновским выходом (выходом электрической энергии).
Катод
Как и анод, катод также является одним из электродов в батарее. Однако катод называют положительным электродом, потому что он не теряет электроны, а приобретает их. Следовательно, аноды окисляются (теряют электроны), а катоды восстанавливаются (приобретают электроны).
Как работает катод?
По сути, катод предназначен для приема электронов от анода. И анод, и катод погружены в раствор электролита, и электричество проходит по проводнику от отрицательной к положительной части вашей батареи. Это, в двух словах, то, как батарея вырабатывает электричество.
Чтобы увидеть, как работает катод, щелкните здесь, чтобы посмотреть короткое, но фантастическое видео, объясняющее этот процесс.
Материалы, подходящие для катодов
Катод может быть любым материалом, если это эффективный окислитель, стабильный при контакте с электролитом. Из оксидов металлов получаются отличные катодные материалы, поскольку они также обладают полезным рабочим напряжением. К ним относятся оксид меди, оксид лития и графический оксид.
Как отличить анод от катода?
Анод и катод. Другими словами: как вы отличите их друг от друга на вашей батарее?
На самом деле это очень просто. Большинство аккумуляторов для жилых автофургонов, автомобилей и даже бытовых аккумуляторов имеют знак плюс (+) и минус (-) на каждом конце. Поскольку анод является отрицательным электродом (и, следовательно, теряет электроны), знак минус относится к аноду. С другой стороны, знак плюс относится к катоду, потому что это положительный электрод (и, таким образом, он получает электроны).
Большинство аккумуляторов для жилых автофургонов, автомобилей и даже бытовых аккумуляторов имеют знак плюс (+) и минус (-) на каждом конце. Поскольку анод является отрицательным электродом (и, следовательно, теряет электроны), знак минус относится к аноду. С другой стороны, знак плюс относится к катоду, потому что это положительный электрод (и, таким образом, он получает электроны).
Почему важно знать разницу между анодом и катодом батареи
Важно понимать разницу между анодом и катодом, потому что вы можете точно понять, как работают ваши батареи, независимо от того, находитесь ли вы на лодке или водите прогулочный автомобиля или даже просто заменить батарейки в пульте дистанционного управления. Независимо от того, устанавливаете ли вы свою собственную солнечную установку или заменяете батареи, вы будете уверены в своих способностях правильно установить источник питания вашего устройства.
Это также полезно, когда вы запускаете машину. Вы когда-нибудь ломали голову, пытаясь понять, куда вам нужно прикрепить зажимы кабеля усилителя? Теперь вы знаете: один подключается к отрицательному концу (анод), а другой — к положительному концу (катод).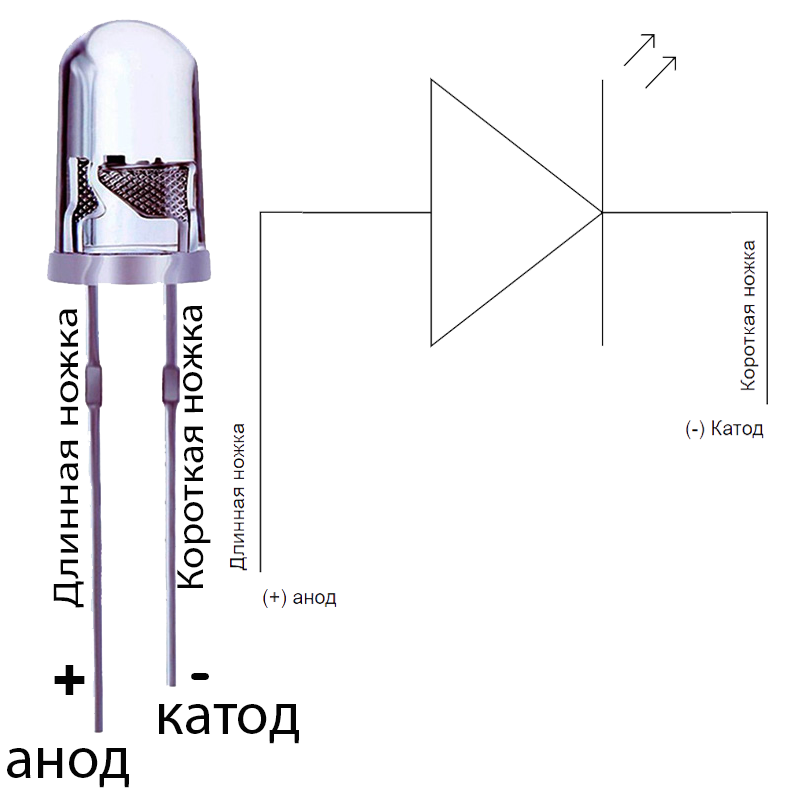
Другие места Аноды и катоды играют роль
Аноды и катоды играют роль не только в батареях, но и в других местах. Например, на кораблях есть «жертвенные аноды», которые действуют как защитное средство для катода, который является исходным материалом, который необходимо защищать от коррозии.
Вы также найдете аноды в бытовых приборах. Водонагреватели имеют жертвенные анодные стержни, которые продлевают срок службы водонагревателя. По сути, анодный стержень притягивает минералы, содержащиеся в воде, и разрушает сам резервуар. Отсюда и название «жертвенный».
Аноды также могут помочь защитить резервуары для жидкости и трубы от коррозии — всегда для защиты катода (то есть важного материала, который производители хотят сохранить).
Анод против катода: Заключительные мысли
Большинство из нас понятия не имеют, что такое анод или катод, просто потому, что мы не имеем дело с этими терминами в повседневной жизни. Однако, если у вас есть автомобиль, транспортное средство для отдыха, лодка, любите возиться или просто хотите узнать, как все работает, полезно ознакомиться с анодами и катодами.
В конце концов, они есть в ваших батареях, водонагревателе и многих других местах в вашей повседневной жизни!
Есть вопросы по анодам и катодам? Оставьте их в комментариях ниже.
физическая химия – положительный или отрицательный анод/катод в электролитическом/гальваническом элементе
спросил
Изменено 2 года, 8 месяцев назад
Просмотрено 582k раз
$\begingroup$
В гальваническом элементе анод считается отрицательным, а катод считается положительным. Это кажется разумным, поскольку анод является источником электронов, а катод — местом, куда текут электроны.
Однако в электролитической ячейке анод считается положительным, а катод теперь отрицательным. Однако реакция все еще похожа, в результате чего электроны от анода текут к положительному выводу батареи, а электроны от батареи текут к катоду.
Однако реакция все еще похожа, в результате чего электроны от анода текут к положительному выводу батареи, а электроны от батареи текут к катоду.
Так почему знак катода и анода меняется при рассмотрении электролизера?
- физико-химия
- электрохимия
$\endgroup$
$\begingroup$
Анод – это электрод, на котором протекает реакция окисления
\begin{align} \ce{Красный -> Бык + e-} \end{align}
имеет место, когда катод является электродом, на котором протекает реакция восстановления
\begin{align} \ce{Бык + e- -> Красный} \end{align}
. Вот как определяются катод и анод.
Гальванический элемент
Так вот, в гальваническом элементе реакция протекает без помощи внешнего потенциала. Поскольку на аноде идет реакция окисления, в результате которой образуются электроны, в ходе реакции накапливается отрицательный заряд до тех пор, пока не будет достигнуто электрохимическое равновесие. Таким образом, анод отрицательный.
Таким образом, анод отрицательный.
На катоде, с другой стороны, происходит реакция восстановления, которая потребляет электроны (оставляя положительные (металлические) ионы на электроде) и, таким образом, приводит к накоплению положительного заряда в ходе реакции до электрохимического достигается равновесие. Таким образом, катод положительный.
Электролитическая ячейка
В электролитической ячейке вы прикладываете внешний потенциал, чтобы заставить реакцию идти в противоположном направлении. Теперь рассуждения обратные. На отрицательном электроде, где вы создали высокий электронный потенциал с помощью внешнего источника напряжения, электроны «выталкиваются» из электрода, тем самым уменьшая окисленные частицы $\ce{Ox}$, поскольку уровень энергии электронов внутри электрода (Ферми уровень) выше энергетического уровня НСМО $\ce{Ox}$, и электроны могут понизить свою энергию, занимая эту орбиталь — у вас, так сказать, очень реактивные электроны. Таким образом, отрицательный электрод будет тем, где будет происходить реакция восстановления, и, следовательно, это будет катод.
На положительном электроде, где вы создали низкий электронный потенциал с помощью внешнего источника напряжения, электроны «всасываются» в электрод, оставляя после себя восстановленные частицы $\ce{Red}$, потому что уровень энергии электронов внутри электрода (Ферми Уровень) ниже энергетического уровня ВЗМО $\ce{Red}$. Таким образом, положительный электрод будет тем, где будет происходить реакция окисления, и, следовательно, это анод.
Сказка об электронах и водопадах
Поскольку существует некоторая путаница в отношении принципов, по которым работает электролиз, я попытаюсь объяснить это с помощью метафоры. Электроны перетекают из области с высоким потенциалом в область с низким потенциалом подобно тому, как вода падает с водопада или течет по наклонной плоскости. Причина та же: вода и электроны могут таким образом понизить свою энергию. Теперь внешний источник напряжения действует как две большие реки, соединенные с водопадами: одна на большой высоте, которая ведет к водопаду — это будет отрицательный полюс, а другая на низкой высоте, которая ведет от водопада — это будет плюс. полюс. Электроды будут похожи на точки реки незадолго до или после водопадов на этой картинке: катод подобен краю водопада, где вода падает, а анод — точке, куда вода падает.
полюс. Электроды будут похожи на точки реки незадолго до или после водопадов на этой картинке: катод подобен краю водопада, где вода падает, а анод — точке, куда вода падает.
Хорошо, что происходит при реакции электролиза? На катоде у вас есть ситуация на большой высоте. Так электроны текут к «краю своего водопада». Они хотят «упасть», потому что за их спиной река тянется к краю, оказывая какое-то «давление». Но куда они могут упасть? Другой электрод отделен от них раствором и обычно диафрагмой. Но есть молекулы $\ce{Ox}$ с пустыми состояниями, которые энергетически ниже состояния электрода. Эти пустые состояния подобны небольшим прудам, лежащим на более низкой высоте, куда может упасть немного воды из реки. Таким образом, каждый раз, когда такая молекула $\ce{Ox}$ приближается к электроду, электрон пользуется возможностью прыгнуть к ней и превратить ее в $\ce{Red}$. Но это не означает, что электроду внезапно не хватает одного электрона, потому что река немедленно заменяет «вытолкнутый» электрон. И источник напряжения (источник реки) не может исчерпать электроны, потому что он получает свои электроны из розетки.
И источник напряжения (источник реки) не может исчерпать электроны, потому что он получает свои электроны из розетки.
Теперь анод: На аноде у вас ситуация с малой высотой. Так что здесь река лежит ниже всего остального. Теперь вы можете представить ВЗМО-состояния молекул $\ce{Red}$ в виде небольших барьерных озер, лежащих на большей высоте, чем наша река. Когда молекула $\ce{Red}$ приближается к электроду, это как будто кто-то открывает шлюз плотины барьерного озера. Электроны перетекают из ВЗМО в электрод, создавая молекулу $\ce{Ox}$. Но электроны не остаются, так сказать, в электроде, их уносит река. И поскольку река представляет собой такое обширное образование (много воды) и обычно впадает в океан, добавление небольшого количества «воды» не сильно меняет реку. Он остается прежним, неизменным, так что каждый раз, когда открывается шлюз, вода из барьерного озера падает на одно и то же расстояние.
$\endgroup$
9
$\begingroup$
Электрод, на котором происходит окисление, называется анодом, а электрод, на котором происходит восстановление, называется катодом.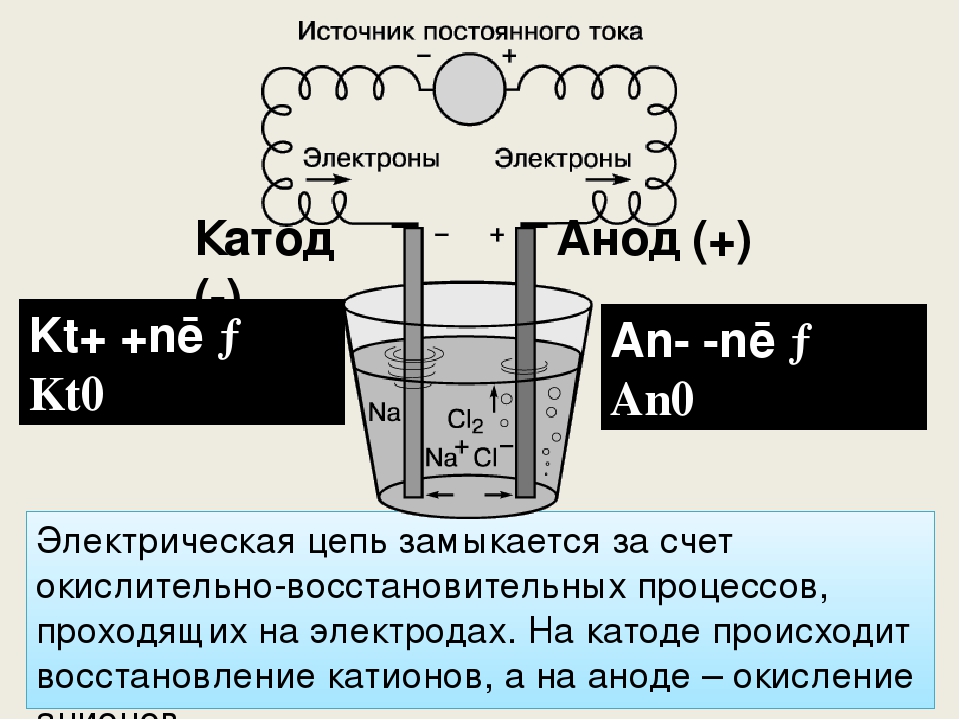 -} $, а в 9- \длинная правая стрелка\; Бык }$.
-} $, а в 9- \длинная правая стрелка\; Бык }$.
Реакции восстановления и окисления всегда связаны, поэтому один электрод действует как источник электронов, а другой — как приемник. В гальваническом элементе общая реакция протекает самопроизвольно, и ток течет от анода к катоду. С другой стороны, в электролитической ячейке мы управляем реакцией неспонтанно, применяя внешний потенциал (например, используя источник питания).
Я думаю, что это изображение должно прояснить работу обоих типов клеток, процессы, происходящие на каждом электроде, и соглашение о знаках.
Хотя он иллюстрирует специфическую реакцию, вы можете распространить его на другие системы.
Источником изображения является Электролиз I в Chemistry.LibreTexts.
$\endgroup$
0
$\begingroup$
Я не эксперт и не ученый, но из того, что я читаю во всех этих объяснениях, и того, что я замечаю на иллюстрации, становится очевидным.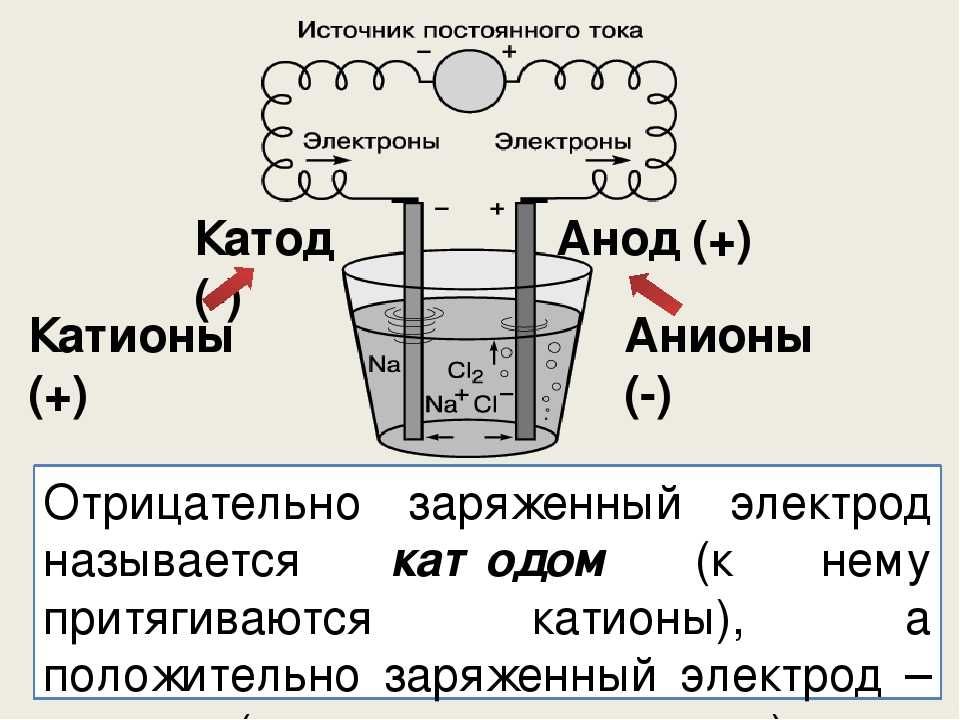 .. по крайней мере, для меня… что, как мне кажется, может прояснить полярность переключение между гальваническим элементом и электролитическим элементом для этого пользователя.
.. по крайней мере, для меня… что, как мне кажется, может прояснить полярность переключение между гальваническим элементом и электролитическим элементом для этого пользователя.
Как установлено и понятно, источник электронов и перенос ионов течет от отрицательного полюса (анод) и принимается положительным полюсом (катодом) (намеренно используя самые основные термины) анод здесь отрицательный, потому что поток исходит ИЗ электролита в лампочку, для которой, если бы клеммы лампочки были помечены, они соответствовали бы электролиту в другой ячейке, так как сила, исходящая от лампочки, толкает поток к катоду ячейки, и катод ячейки вытягивается из колбы.
В электролитической ячейке «электролит» берет на себя роль лампочки гальванической ячейки, так как электроны ПОСЫЛАЮТСЯ К нему из источника питания, и сам по себе не является ИСТОЧНИКОМ потока, но ПОДЛЕЖИТ К силе от источника потока.
ТАК так же, как анод гальванического элемента посылает на лампочку, а электролит помечен как нагрузка гальванического элемента, и передает свою поступающую отрицательную силу от источника тока, и это проталкивает электролит подобно потоку ИЗ лампочка.
Может быть проще, если вы заметите, что ИСТОЧНИК питания НЕ является электролитом и технически, черная клемма источника питания является ИСТИННЫМ анодом (Передача), а красная сторона — ИСТИННЫМ Катодом (Прием), но при идентификации реактивное вещество погружено/окружено электролитическим веществом, анод отдает свои ионы, которые затем присоединяются к катоду, который их получает.
Поэтому метки в электролитической ячейке указывают не на «источник потока», а на реакцию вовлеченных веществ из-за силы/потока, воздействующей на них от источника питания, но не являющегося источником питания, и поэтому не должен быть маркирован как АС один… и вариантов их маркировки всего два, и так как он не может быть изменен в источнике питания, он может быть изменен только в месте контакта с электролитом!
По крайней мере, это то, что я понял, просмотрев комментарии и иллюстрации.
Я искренне надеюсь, что это поможет прояснить причину смены меток для этого пользователя и любых других, которые борются с концепцией существования из-за того, что источник тока должен быть помечен как — Анод и + Катод.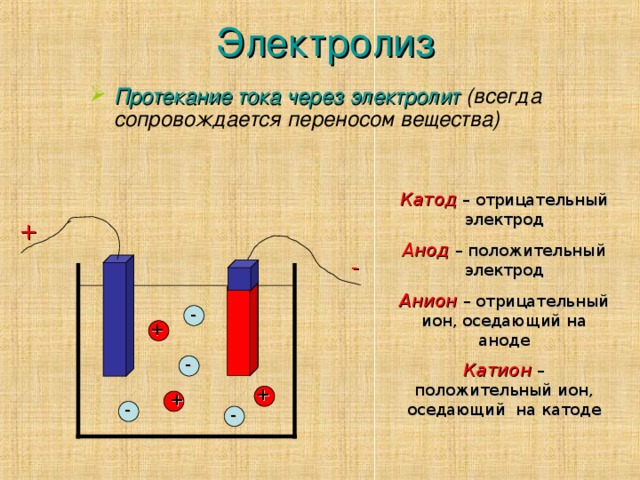 .. заставляя объект ток играет против, несмотря на их полюса и из-за направления потока.
.. заставляя объект ток играет против, несмотря на их полюса и из-за направления потока.
$\endgroup$
$\begingroup$
Знаки (+) и (-) относятся к потоку электронов в источнике питания. В гальваническом (гальваническом) элементе сама ячейка является источником питания. В электролитической ячейке ячейка подключена к внешнему источнику питания. Таким образом, в то время как обозначение анода и катода напрямую связано с направлением потока электронов в ячейке, то, как (+) и (-) относятся к аноду и катоду, зависит от того, идет ли реакция к равновесию или нет (в случае перезаряжаемых батарей, независимо от того, разряжаете вы батарею или заряжаете ее). В зависимости от направления реакции меняются метки анода и катода, а метки (+) и (-) остаются прежними.
Пример иллюстрирует это. Вот две свинцово-кислотные батареи, соединенные вместе таким образом, что заряженная батарея заряжает разряженную:
Обозначения (+) и (-) относятся к направлению движения электронов, если они разряжаются (конечно, разряженные батареи). аккумулятор дальше разряжаться не может, так что экспериментально не скажешь). Метки анода и катода относятся к конкретной ситуации. Поэтому, если вы подключите источник питания с более высоким напряжением к заряженной батарее вместо разряженной батареи, вы будете заряжать ее дальше. Это обратит химическую реакцию в этой батарее, и метки анода и катода придется поменять местами.
аккумулятор дальше разряжаться не может, так что экспериментально не скажешь). Метки анода и катода относятся к конкретной ситуации. Поэтому, если вы подключите источник питания с более высоким напряжением к заряженной батарее вместо разряженной батареи, вы будете заряжать ее дальше. Это обратит химическую реакцию в этой батарее, и метки анода и катода придется поменять местами.
В другом сценарии вы можете взять две 12-вольтовые батареи и соединить их последовательно (соедините (+) одной с (-) другой). Это даст вам 24-вольтовую батарею, и если вы подключите к ней потребитель, катод будет (+), а анод будет (-) для них обоих.
Для свинцово-кислотных аккумуляторов знаки (+) и (-) никогда не меняются, поэтому можно постоянно маркировать электроды. В концентрационной ячейке (+) и (-) зависят от концентрации окислительно-восстановительных соединений в двух половинных ячейках, поэтому вы не можете пометить их «постоянным маркером».
$\endgroup$
$\begingroup$
Анод – это электрод, на котором происходит полуреакция окисления.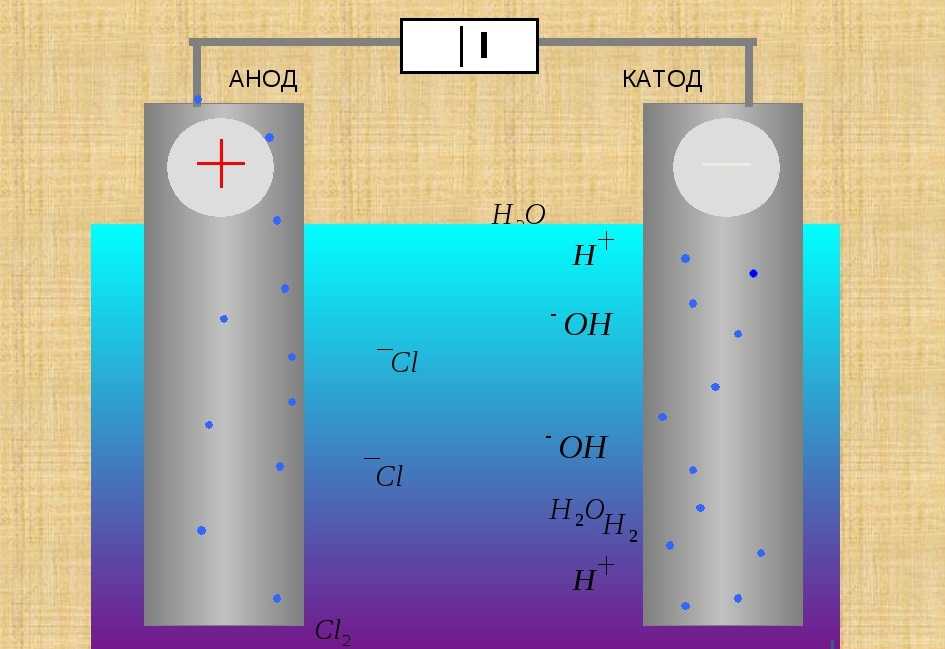
В гальваническом элементе реакция протекает самопроизвольно, внешний потенциал не приложен, и когда материал анода окисляется, анод становится отрицательным электродом. В электролитической ячейке реакцией управляет внешний потенциал, анод — это электрод, на котором происходит реакция окисления, следовательно, на этот раз это электрод с положительным потенциалом.
$\endgroup$
1
$\begingroup$
Я просто добавляю хороший мнемонический инструмент, как запомнить соглашение об именах:
Анод = анабазис (от греческого ana = «вверх», bainein = «шагать или маршировать»), электроны будут двигаться вверх от электрод к проволоке = окисление .
Ксенофонт, Анабасис, «Марш вверх по стране»
Катод = катабазис (путешествие вниз), электроны будут двигаться вниз от провода к электроду = восстановление
Термины анабазис/катабазис применяются и в других областях.

 Назначение диода. Определяем полярность светодиода. Где плюс и минус у LED
Назначение диода. Определяем полярность светодиода. Где плюс и минус у LED